RDC Nº 142, de 17 de março de 2017
publicado em 17/03/2017
Ministério da Saúde - AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA/DIRETORIA COLEGIADA
RESOLUÇÃO - RDC Nº 142, DE 17 DE MARÇO DE 2017
Dispõe sobre a regularização de produtosde higiene pessoal descartáveis destinadosao asseio corporal, que compreendem escovase hastes para higiene bucal, fios efitas dentais, absorventes higiênicos descartáveis,coletores menstruais e hastes flexíveis.
A Diretoria Colegiada da Agência Nacional de VigilânciaSanitária, no uso da atribuição que lhe confere o art. 15, III e IValiado ao art. 7º, III, e IV, da Lei nº 9.782, de 26 de janeiro de 1999,e ao art. 53, V, §§ 1º e 3º do Regimento Interno aprovado nos termosdo Anexo I da Resolução da Diretoria Colegiada - RDC n° 61, de 3de fevereiro de 2016, resolve adotar a seguinte Resolução da DiretoriaColegiada, conforme deliberado em reunião realizada em 07de março de 2017, e eu, Diretor-Presidente, determino a sua publicação.
Art.1º Fica aprovado o Regulamento Técnico que estabelecea definição, a classificação, os requisitos técnicos e de rotulagem e oprocedimento eletrônico para a regularização de escovas e hastes parahigiene bucal, fios e fitas dentais, absorventes higiênicos descartáveis,coletores menstruais e hastes flexíveis, destinados ao asseio corporal.
CAPÍTULOI
DAS DISPOSIÇÕES INICIAIS
Seção I
Objetivo
Art. 2º Esta Resolução tem como objetivo atualizar e padronizaros procedimentos necessários para a regularização de produtosde higiene pessoal descartáveis.
Seção II
Abrangência
Art. 3º Esta Resolução se aplica aos produtos de higienepessoal descartáveis, doravante denominados produtos descartáveis,que compreendem as escovas e hastes para higiene bucal, fios e fitasdentais, absorventes higiênicos descartáveis, coletores menstruais ehastes flexíveis, destinados ao asseio corporal.
Parágrafo único. Para fins de regularização sanitária, a Anvisadeverá avaliar e poderá submeter novos produtos de higienepessoal descartáveis a este regulamento técnico.
CAPÍTULO II
DOS REQUISITOS PARA REGULARIZAÇÃO
Art. 4º Os produtos descartáveis são isentos de registro e suacomercialização no território nacional fica condicionada ao procedimentode comunicação prévia à Anvisa pela empresa detentora doproduto.
§1º A regularização sanitária dos produtos descartáveis passaa ser realizada na forma eletrônica, por meio do portal eletrônico daAnvisa.
§2º Comunicação prévia é o procedimento administrativo aser aplicado para informar à Anvisa a intenção de comercialização deum produto isento de registro por meio de notificação.
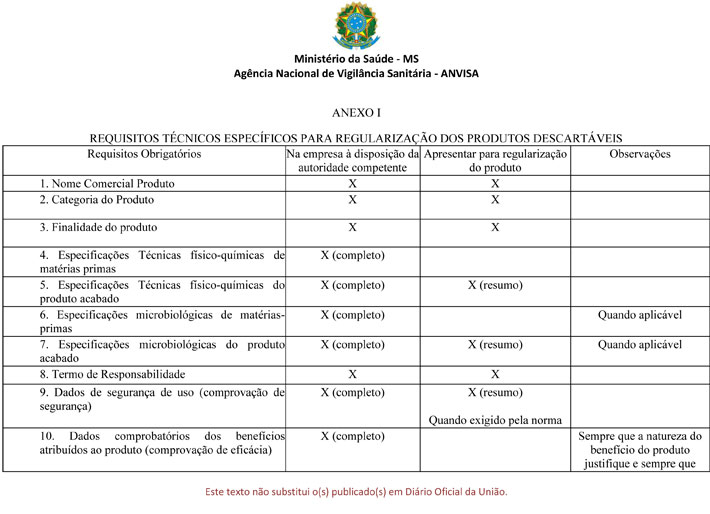
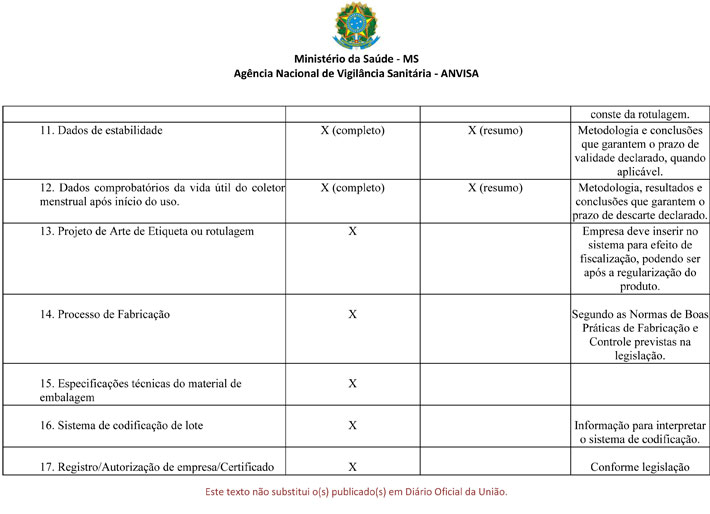
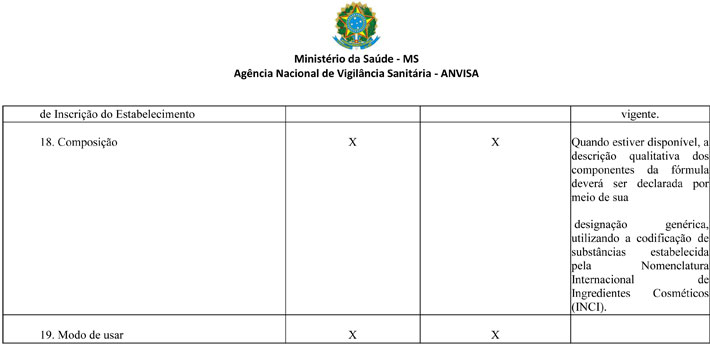
§3º Os requisitos técnicos específicos para regularização dosprodutos descartáveis, bem como a necessidade de sua apresentação àAnvisa, estão descritos na tabela constante no Anexo I desta Resolução.
§4ºA publicidade da regularização de produtos descartáveisfica assegurada por meio de divulgação no portal eletrônico da Anvisae dar-se-á ao final do procedimento de protocolo online.
§5º As orientações necessárias ao procedimento eletrônicopara a regularização dos produtos descartáveis estão disponíveis noportal eletrônico da Anvisa.
§6º O titular do produto deve comunicar à Anvisa as alteraçõesrealizadas no produto, por meio de procedimento eletrônico,mantendo as informações devidamente atualizadas.
§7º A Anvisa poderá estabelecer outras formas de comunicaçãoprévia, inclusive em formato não eletrônico, segundo interesseda administração.
Art. 5º Os documentos gerados ao final do procedimentoeletrônico devem ser mantidos na empresa.
Art. 6º A empresa deverá anexar à transação o Termo deResponsabilidade, devidamente assinado pelo Responsável técnico eRepresentante legal da empresa, conforme Anexo II.
Art. 7º A regularização de produtos descartáveis realizadanos termos desta Resolução tem validade de 10 (dez) anos e poderáser renovada por períodos iguais e sucessivos.
§1º A renovação da regularização do produto deverá serrealizada no primeiro semestre do último ano do decênio de validade.
§2ºSerá considerado caduco o processo cuja renovação nãotenha sido comunicada no prazo referido no parágrafo 1º.
§3° A renovação será realizada exclusivamente por meio demanifestação de interesse da empresa na manutenção da regularizaçãodo produto.
Art. 8° As informações apresentadas na regularização doproduto, bem como suas atualizações, são de inteira responsabilidadeda empresa titular do produto, devem atender ao disposto na legislaçãosanitária vigente e serão objeto de controle sanitário pelaAnvisa.
§1° O titular do produto deve possuir dados comprobatóriosque atestem a qualidade, a segurança e a eficácia de seus produtos ea idoneidade dos respectivos dizeres de rotulagem, bem como ocumprimento dos requisitos técnicos estabelecidos na legislação vigente,os quais deverão ser apresentados aos órgãos de vigilânciasanitária sempre que solicitados.
§2º O titular do produto deve garantir que o produto nãoconstitui risco à saúde quando utilizado durante o seu período devalidade, em conformidade com as instruções de uso e demais informaçõesconstantes na embalagem de venda do produto.
§3º O controle sanitário dos produtos descartáveis será realizadopor meio de verificação das informações prestadas na comunicaçãoprévia, monitoramento de mercado e inspeção do fabricante,em função do risco sanitário e do estabelecido no art. nº 41 daLei nº 9.782, de 26 de janeiro de 1999.
Art. 9° Para fabricar ou importar os produtos de que trataesta Resolução, as empresas devem possuir Autorização de Funcionamentona Anvisa para as atividades e classes de produtos quedeseja comercializar e devem possuir licença junto à autoridade sanitáriacompetente.
Art. 10. O cumprimento das Boas Práticas de Fabricação seráverificado no estabelecimento fabricante e ou importador medianteinspeção realizada pela autoridade sanitária competente, de acordocom a Resolução de Diretoria Colegiada - RDC nº 48, de 25 deoutubro de 2013, e suas atualizações.
Art. 11. Os produtos descartáveis que contenham ingredientesque possam migrar para a pele e ou mucosas deverão atender aosrequisitos estabelecidos nas seguintes listas de substâncias de produtosde higiene pessoal, cosméticos e perfumes:
I- lista de substâncias de ação conservante permitidas paraprodutos de higiene pessoal, cosméticos e perfumes, aprovada pelaResolução da Diretoria Colegiada - RDC nº 29, de 10 de junho de2012, e suas atualizações;
II- lista de substâncias corantes permitidas para produtos dehigiene pessoal, cosméticos e perfumes, aprovada pela Resolução daDiretoria Colegiada - RDC nº 44, de 9 de agosto de 2012, e suasatualizações;
III- lista de substâncias que os produtos de higiene pessoal,cosméticos e perfumes não devem conter exceto nas condições e comas restrições estabelecidas, aprovada pela Resolução da Diretoria Colegiada- RDC nº 03, de 18 de janeiro de 2012, e suas atualizações;
IV-lista de filtros ultravioletas permitidos para produtos dehigiene pessoal, cosméticos e perfumes, aprovada pela Resolução daDiretoria Colegiada - RDC nº 69, de 23 de março de 2016, e suasatualizações; e
V- lista de substâncias que não podem ser utilizadas emprodutos de higiene pessoal, cosméticos e perfumes, aprovada pelaResolução da Diretoria Colegiada - RDC nº 48, de 16 de março de2006, e suas atualizações.
Parágrafo único. Considera-se que fragrâncias e aromas sãoingredientes que migram para a pele e ou mucosas.
CAPÍTULO III
REQUISITOS SOBRE ROTULAGEM OBRIGATÓRIAGERAL PARA PRODUTOS DESCARTÁVEIS
Art.12. Os produtos descartáveis devem atender a rotulagemobrigatória geral de acordo com os itens elencados no Anexo III.
Art.13. Quando a embalagem for pequena e não permitir ainclusão de advertências e restrições de uso e ou instrução de uso,estas deverão ser veiculadas em folheto anexo.
§1° Na ocorrência da hipótese de que trata o caput, a embalagemdeverá conter as seguintes indicações: "Advertências e restriçõesde uso: ver folheto anexo" e ou "Instrução de uso: ver folhetoanexo".
§2° Caso o produto contenha embalagem primária e secundária,sendo uma das embalagens pequena de forma que nãopermita a inclusão de advertências e restrições de uso, será permitidaa substituição destas informações pela descrição "Advertências e restriçõesde uso: ver embalagem externa" ou "Advertências e restriçõesde uso: ver embalagem interna".
Art. 14. No caso de produtos importados, é obrigatório queconstem na rotulagem todos os dizeres de rotulagem listados noAnexo III no idioma oficial do Brasil (português), sem prejuízo desua inscrição paralela em outros idiomas.
§1° Excetua-se do disposto no caput a composição do produto.Quando estiver disponível, a descrição qualitativa dos componentesda fórmula deverá ser declarada por meio de sua designaçãogenérica, utilizando a codificação de substâncias estabelecida pelaNomenclatura Internacional de Ingredientes Cosméticos (INCI).
§2° Se o rótulo original não contiver a informação requerida,será aceita adequação mediante um sobre rótulo ou etiqueta quecontenha a informação faltante.
CAPÍTULO IV
REQUISITOS TÉCNICOS ESPECÍFICOS PARA REGULARIZAÇÃODE ESCOVAS PARA HIGIENE BUCAL
Seção I
Definição
Art. 15. Para efeito desta Resolução, define-se escova parahigiene bucal como um instrumento mecânico, que pode ou nãopossuir componentes elétricos, utilizado para realizar a higiene dedentes, gengiva, língua, aparelhos ortodônticos e dentaduras.
Seção II
Classificação
Art. 16. Para efeito desta Resolução, as escovas para higienebucal podem ser classificadas de acordo com a finalidade de uso e oufaixa etária e ou rigidez da área encerdada:
I- quanto à finalidade de uso: manual, elétrica, unitufo, interdental,para dentadura, pós-cirúrgica, ortodôntica e especial parahigiene da língua;
II- quanto à indicação da faixa etária: de uso adulto ouinfantil, conforme especificado nos dizeres de rotulagem; e
III- quanto à rigidez da área encerdada: extra macia, macia,média e dura.
Seção III
Material
Art. 17. Todo o material que compõe a escova para higienebucal deve ser atóxico e adequado para seu uso, garantindo a robustezfísica do produto e a saúde do usuário.
Seção IV
Embalagem e Rotulagem Específica
Art. 18. A escova para higiene bucal deverá ser embalada demodo a preservar a qualidade do produto.
Art. 19. Na rotulagem das escovas para higiene bucal deverãoconstar:
I- a indicação de substituição da escova a cada 3 (três) mesesapós iniciar o uso ou conforme orientação do dentista;
II - a indicação de que o produto não é perecível, em substituiçãoa indicação do prazo de validade, ou indicação do prazo devalidade, se aplicável;
III- para produtos infantis: a indicação de uso infantil, aapresentação da faixa etária a que se destinam e a indicação de que ouso deve ser supervisionado por adulto;
IV - a indicação de que o tipo de escova deve ser orientadapelo dentista;
V - a indicação quanto à rigidez da área encerdada; e
VI - cuidados de conservação e local de armazenamento apóso uso.
Seção V
Ensaios
Art. 20. Os seguintes ensaios devem ser realizados conformedisposto abaixo e mantidos na empresa à disposição da autoridadecompetente:
I - medida da altura/diâmetro da cerda: deverá ser realizadacom instrumentos ópticos de precisão ou outros aparelhos com precisãode leitura de, no mínimo, 0,1 mm (um décimo de milímetro);
II - medida da rigidez da área encerdada: deverá ser realizadaconforme a Norma ISO 22254 ("Dentistry - Manual toothbrushes Resistanceof tufted portion to deflection") ou suas atualizações;
III - tensão para remover o tufo: deverá ser realizada conformea Norma ISO 20126 ("Dentistry - Manual toothbrushes - GeneralRequirements and Test Methods") ou suas atualizações;
IV - ensaios para filamentos radiais: deverão ser realizadospara as escovas interdentais conforme a norma ISO 16409:2006("Manual interdental brushes") ou suas atualizações;
V - forma da extremidade da cerda: deverá ser verificada pormeio de microscópio óptico sob campo escuro com leitura máxima deampliação de 50 (cinquenta) vezes. As pontas das cerdas devemapresentar acabamento, podendo ser lisas, plumadas, planas, arredondadase polidas e 80% das cerdas aplicadas na escova devemapresentar acabamento mínimo aceitável; e
VI - escovas elétricas: deverão ser avaliadas conforme anorma ISO 20127 ("Dentistry - Powered toothbrushes - General Requirementsand Test Methods") ou suas atualizações.
Seção VI
Requisitos Microbiológicos
Art. 21. As escovas para higiene bucal, por serem compostaspor materiais sintéticos e anidros, não apresentam suscetibilidade aocrescimento microbiológico, devendo sua embalagem garantir proteçãocontra contaminação externa.
CAPÍTULO V
REQUISITOS TÉCNICOS ESPECÍFICOS PARA REGULARIZAÇÃODE HASTES PARA HIGIENE BUCAL
Seção I
Definição
Art. 22. Para efeito desta Resolução, define-se haste parahigiene bucal como um instrumento mecânico, que pode ou nãopossuir componentes elétricos e cerdas, utilizado para realizar a higieneda língua.
Seção II
Material
Art. 23. Todo o material que compõe a haste para higienebucal deve ser atóxico e adequado para seu uso, garantindo a robustezfísica do produto e a saúde do usuário.
Seção III
Embalagem e Rotulagem Específica
Art. 24. A haste para higiene bucal deverá ser embalada demodo a preservar a qualidade do produto.
Art. 25. Na rotulagem das hastes para higiene bucal deverãoconstar:
I- a indicação de substituição da haste a cada 3 (três) mesesapós iniciar o uso ou conforme orientação do dentista;
II - a indicação de que o produto não é perecível, em substituiçãoa indicação do prazo de validade, ou indicação do prazo devalidade, se aplicável;
III- para produtos infantis: a indicação de uso infantil, aapresentação da faixa etária a que se destinam e a indicação de que ouso deve ser supervisionado por adulto; e
IV- cuidados de conservação e local de armazenamento apóso uso.
Seção IV
Ensaios
Art. 26. Os seguintes ensaios devem ser realizados parahastes para higiene bucal com cerdas e mantidos na empresa à disposiçãoda autoridade competente:
I - medida da altura/diâmetro da cerda: deverá ser realizadacom instrumentos ópticos de precisão ou outros aparelhos com precisãode leitura de, no mínimo, 0,1 mm (um décimo de milímetro);
II - medida da rigidez da área encerdada: deverá ser realizadaconforme a Norma ISO 22254 ("Dentistry - Manual toothbrushes Resistanceof tufted portion to deflection") ou suas atualizações;
III - tensão para remover o tufo: deverá ser realizada conformea Norma ISO 20126 ("Dentistry - Manual toothbrushes - GeneralRequirements and Test Methods") ou suas atualizações; e
IV - forma da extremidade da cerda: deverá ser verificadapor meio de microscópio óptico sob campo escuro com leitura máximade ampliação de 50 (cinquenta) vezes. As pontas das cerdasdevem apresentar acabamento, podendo ser lisas, plumadas, planas,arredondadas e polidas e 80% (oitenta por cento) das cerdas aplicadasna escova devem apresentar acabamento mínimo aceitável.
Seção V
Requisitos Microbiológicos
Art. 27. As hastes para higiene bucal, por serem compostaspor materiais sintéticos e anidros, não apresentam suscetibilidade aocrescimento microbiológico, devendo sua embalagem garantir proteçãocontra contaminação externa.
CAPÍTULO VI
REQUISITOS TÉCNICOS ESPECÍFICOS PARA REGULARIZAÇÃODE ABSORVENTES HIGIÊNICOS DESCARTÁVEISDESTINADOS AO ASSEIO CORPORAL
Seção I
Definições
Art. 28. Para efeito desta Resolução são adotadas as seguintesdefinições:
I - produtos absorventes descartáveis de uso externo: artigosdestinados ao asseio corporal, aplicados diretamente sobre a pele,com a finalidade de absorver ou reter excreções e secreções orgânicas,tais como urina, fezes, leite materno e as de natureza menstruale intermenstrual; e
II - produtos absorventes descartáveis de uso intravaginal:artigos destinados a absorver ou reter excreções e secreções menstruaise intermenstruais, aplicados por inserção vaginal.
Parágrafo único. Estão compreendidos no grupo de produtosde que trata o inciso I os absorventes higiênicos femininos de usoexterno, as fraldas para bebês, as fraldas para adultos, os absorventeshigiênicos para incontinência e os absorventes de leite materno.
Seção II
Material
Art. 29. Os produtos absorventes descartáveis deverão sercompostos de fibras de algodão hidrófilo e ou outros materiais absorventesque não contenham quaisquer ingredientes farmacologicamenteativos.
Parágrafo único. Os produtos absorventes descartáveis deuso externo podem ainda conter ingredientes como fragrâncias e inibidoresde odores. Estes ingredientes não podem ser adicionados emabsorventes de uso interno.
Seção III
Requisitos de Segurança
Art. 30. O titular do produto deve garantir a segurança doproduto acabado por meio da avaliação dos seguintes requisitos:
I - Ficha de Informação de Segurança do Produto Químico(FISPQ) e outras informações relacionadas à segurança de cada matéria-primautilizada;
II - para fragrâncias, laudo de inocuidade da matéria-primaemitido pelo fornecedor, garantindo sua segurança, em conformidadecom os padrões estabelecidos por órgãos regulamentadores competentes,tais como a IFRA - Associação Internacional de Fragrâncias;e
III - para absorventes higiênicos intravaginais, além dos requisitosprevistos nos incisos I e II, deverão ser realizados testes decitotoxicidade e irritação da mucosa vaginal no produto acabado.
Parágrafo único. Nos casos em que as informações descritasnos incisos I e II não estejam disponíveis ou sejam inconclusivas, asegurança deverá ser garantida por meio da realização dos seguintesensaios no produto acabado:
I - irritação cutânea primária;
II - irritação cutânea repetida; e
III - sensibilização dérmica.
Art. 31. O titular do produto deverá possuir parecer técnicosobre a segurança do produto com base nos requisitos descritos noart. 30 e apresentar à Anvisa resumo que ateste a segurança de uso doproduto acabado.
Seção IV
Requisitos Microbiológicos
Art. 32. O titular do produto deve garantir os seguinteslimites microbiológicos para o produto acabado:
I - produtos absorventes descartáveis de uso externo: asavaliações microbiológicas deverão responder aos seguintes limites deaceitabilidade para uma amostra de 10g (dez gramas): ausência deEscherichia coli, Pseudomonas aeruginosa, Staphylococcus aureus,Candida albicans e, no caso de absorventes para os seios, ausência deEscherichia coli, Pseudomonas aeruginosa, Staphylococcus aureus,Candida albicans e Clostridium sp; e
II - produtos absorventes descartáveis de uso intravaginal: asavaliações microbiológicas deverão responder aos seguintes limites deaceitabilidade para uma amostra de 10g (dez gramas): ausência deEscherichia coli, Pseudomonas aeruginosa, Staphylococcus aureus,Clostridium sp e Candida albicans.
§ 1º Para os produtos de que trata o inciso I, a contagem demicrorganismos aeróbicos mesófilos não deve ultrapassar 1000 UFC(mil unidades formadoras de colônias) por grama de amostra e acontagem de fungos e leveduras não deve ultrapassar 100 UFC (cemunidades formadoras de colônia) por grama de amostra.
§ 2º Para os produtos de que trata o inciso II, a contagem demicrorganismos aeróbios mesófilos não deve ultrapassar 500 UFC(quinhentas unidades formadoras de colônia) por grama de amostra ea contagem de fungos e leveduras não deve ultrapassar a 100 UFC(cem unidades formadoras de colônia) por grama de amostra.
Seção V
Rotulagem Específica
Art. 33. Na rotulagem de produtos absorventes descartáveisde uso intravaginal deverão constar:
I - instruções que orientem claramente a usuária sobre aSíndrome do Choque Tóxico (SCT);
II - modo de uso;
III - orientações quanto à necessidade de uso do tamanhoadequado a cada fluxo menstrual;
IV - descrição das características dos produtos de sua marcaquanto aos tamanhos e tipo de fluxo menstrual, definidos em funçãoda quantidade de absorção em gramas;
V - frequência de troca do produto;
VI - importância da higiene pessoal, especialmente de lavaras mãos antes e após a inserção de um absorvente intravaginal;
VII - informação sobre a necessidade de utilizar somente umabsorvente intravaginal de cada vez;
VIII - orientação para a usuária se certificar de que o absorventefoi removido a cada troca do produto e quando a menstruaçãoterminar; e
IX - orientação para a usuária procurar auxílio médico emcaso de dificuldade para retirada total do produto.
CAPÍTULO VII
REQUISITOS TÉCNICOS ESPECÍFICOS PARA REGULARIZAÇÃODE COLETORES MENSTRUAIS
Seção I
Definição
Art. 34. Para efeito desta Resolução, define-se coletor menstrualcomo um dispositivo intravaginal utilizado para coletar o fluxomenstrual.
Seção II
Material
Art. 35. Todo o material que compõe o coletor menstrualdeve ser atóxico e adequado para seu uso.
Parágrafo único. Os coletores menstruais devem ser isentosde ingredientes como fragrâncias e inibidores de odores.
Seção III
Requisitos de Segurança
Art. 36. O titular do produto deve garantir a segurança pormeio da avaliação dos seguintes requisitos no produto acabado:
I - testes de citotoxicidade de acordo com a ISO 10993-5;
II - irritação da mucosa vaginal em humanos; e
III - sensibilização dérmica.
Parágrafo único. Os testes descritos nos incisos II e III,quando realizados em humanos, devem ter um mínimo de 30 (trinta)voluntários.
Art. 37. O titular do produto deverá possuir parecer técnicosobre a segurança do produto com base nos requisitos descritos noart. 36 e apresentar à Anvisa resumo que ateste a segurança de uso doproduto acabado.
Seção IV
Requisitos Microbiológicos
Art. 38. O titular do produto deve garantir na avaliaçãomicrobiológica os seguintes limites de aceitabilidade para uma amostrade 10g (dez gramas) do produto acabado: ausência de Escherichiacoli, Pseudomonas aeruginosa, Staphylococcus aureus, Clostridium spe Candida albicans.
Parágrafo único. A contagem de microrganismos aeróbiosmesófilos não deve ultrapassar 500 UFC (quinhentas unidades formadorasde colônia) por grama de amostra e a contagem de fungos eleveduras não deve ultrapassar a 100 UFC (cem unidades formadorasde colônia) por grama de amostra.
Seção V
Rotulagem Específica
Art. 39. Na rotulagem de produtos coletores menstruais deverãoconstar:
I - instruções que orientem claramente a usuária sobre SCT(Síndrome do Choque Tóxico);
II - modo de uso contendo a frequência de remoção doproduto para descarte do conteúdo menstrual;
III - orientações quanto à necessidade de uso do tamanhoadequado a cada fluxo menstrual;
IV - descrição das características dos produtos de sua marcaquanto aos tamanhos e tipo de fluxo menstrual;
V - tempo para descarte do coletor menstrual, com base emensaios que determinem que o produto mantém suas propriedades,considerando as condições de uso do produto;
VI - importância da higiene pessoal, especialmente de lavaras mãos antes e após a inserção o coletor menstrual;
VII - orientação para a usuária se certificar de que o coletorfoi removido dentro do prazo estipulado pelo fabricante;
VIII - orientação para a usuária procurar auxílio médico emcaso de dificuldade para retirada do produto;
IX- indicação dos cuidados de conservação;
X - indicação da embalagem adequada e local de armazenamentoapós o uso; e
XI - orientação para a usuária com prolapso, retroversão ouanteflexão do útero consultar um médico antes de iniciar o uso doproduto.
CAPÍTULO VIII
REQUISITOS TÉCNICOS ESPECÍFICOS PARA REGULARIZAÇÃODE FIOS E FITAS DENTAIS
Seção I
Definição
Art. 40. Para efeito desta Resolução, definem-se fios e fitasdentais como fio ou fita, de nylon, polipropileno (PP), politetrafluoretileno(PTFE) ou outro material apropriado, podendo ser recobertopor ingredientes facilitadores de deslizamento, saborizantese/ou outros, destinados a realizar a higiene oral entre os dentes, emaparelhos ortodônticos e/ou próteses, com o objetivo de removerresíduos de alimentos e/ou placa, evitando o acúmulo da placa bacterianae consequentemente a formação de cáries e problemas degengivas.
§ 1º É permitida a adição de flúor aos fios e fitas dentaisdesde que não exceda a concentração máxima permitida de 0,15%(quinze centésimos por cento).
§ 2º A regularização dos fios e fitas dentais destinados aopúblico infantil deve seguir a presente norma.
Seção II
Material
Art. 41. Todo material que compõe os fios e fitas dentaisdeve ser atóxico e adequado para seu uso.
Seção III
Embalagem e Rotulagem Específica
Art. 42. Os fios e fitas dentais deverão ser embalados demodo a preservar a qualidade do produto.
Art. 43. Na rotulagem dos fios e fitas dentais deverá constar:
I- instruções quanto à correta utilização do produto com afinalidade de garantir a eficácia e segurança de seu uso;
II - no caso de fio e fita dental acrescidos de flúor, indicaçãodo composto de flúor utilizado, sua concentração em ppm (parte pormilhão) e inclusão da frase "Não usar em crianças menores de 2anos";
III- indicação de que o uso em crianças deve ser supervisionadopor adulto; e
IV - indicação da espessura do fio ou fita dental.
Seção IV
Requisitos de Segurança
Art. 44. O titular do produto deve garantir a segurança doproduto acabado por meio da avaliação dos seguintes requisitos:
I - Ficha de Informação de Segurança Produto Químico(FISPQ) e outras informações relacionadas à segurança de cada matéria-primautilizada; e
II - para aromatizantes, laudo de inocuidade da matériaprimaemitido pelo fornecedor, garantindo sua segurança, em conformidadecom os padrões estabelecidos por órgãos regulamentadorescompetentes, tais como a IFRA - Associação Internacional de Fragrâncias.
SeçãoV
Requisitos Microbiológicos
Art. 45. O titular do produto deve garantir os limites microbiológicospara o produto acabado em conformidade com o regulamentotécnico específico que estabelece os parâmetros de controlemicrobiológico para os produtos de higiene pessoal, cosméticose perfumes, aprovado pela Resolução nº 481, de 23 de setembro de1999, e suas atualizações.
CAPÍTULO IX
REQUISITOS TÉCNICOS ESPECÍFICOS PARA REGULARIZAÇÃODE HASTES FLEXÍVEIS
Seção I
Definição
Art. 46. Para efeito desta Resolução, definem-se hastes flexíveiscomo artigos de higiene pessoal compostos de uma haste flexívelcom as extremidades cobertas com fibra de algodão hidrófilo ououtros materiais absorventes, não estéreis, utilizados principalmentepara auxiliar o asseio corporal.
Seção II
Material
Art. 47. Todo o material que compõe as hastes flexíveis deveser atóxico e adequado para seu uso.
Seção III
Embalagem e Rotulagem Específica
Art. 48. As hastes flexíveis deverão ser embaladas de modoa preservar a qualidade do produto.
Art. 49. Na rotulagem de hastes flexíveis deverá constar aindicação de que:
I - o produto não deve ser inserido no canal do ouvidodevido ao risco de perfuração do tímpano;
II - crianças não devem usar o produto sem a supervisão deum adulto; e
III - o produto não deve ser inserido profundamente nasnarinas para evitar lesões.
Seção IV
Requisitos Microbiológicos
Art. 50. O titular do produto deve garantir os limites microbiológicospara o produto acabado em conformidade com o regulamentotécnico específico que estabelece os parâmetros de controlemicrobiológico para os produtos de higiene pessoal, cosméticose perfumes, aprovado pela Resolução nº 481, de 23 de setembro de1999, e suas atualizações.
CAPÍTULO X
DAS DISPOSIÇÕES FINAIS E TRANSITÓRIAS
Art. 51. Os produtos descartáveis regularizados de acordocom a Portaria n° 1.480, de 31 de dezembro de 1990, a Portaria nº 97,de 26 de Junho de 1996, a Resolução Diretoria Colegiada - RDC nº10, de 21 de outubro de 1999 e a Resolução da Diretoria Colegiada- RDC nº 7, de 10 de fevereiro de 2015, poderão ser fabricados até 24
(vinte e quatro) meses após a publicação desta Resolução e comercializadosaté o fim do prazo de validade.
§1º Os produtos que se encontram regularizados deverão sercadastrados conforme procedimentos descritos no art. 4º desta Resolução,no prazo máximo de 24 (vinte e quatro) meses após sua publicação.
§2º Os produtos novos já podem ser regularizados conformeprocedimentos descritos no art. 4º desta Resolução a partir de suapublicação.
§3º Os produtos novos ainda poderão ser regularizados pormeio do processo de comunicação prévia por carta até o prazo máximode 180 (cento e oitenta) dias após a publicação dessa Resoluçãoe comercializados até o fim do seu prazo de validade.
§4º Os produtos regularizados conforme o disposto no parágrafo3º deste artigo deverão ser cadastrados conforme procedimentosdescritos no art. 4º desta Resolução em até 180 (cento eoitenta) dias após sua publicação.
§5º Os produtos cadastrados conforme procedimentos descritosno art. 4º desta Resolução deverão atender a todos os requisitosestabelecidos pela mesma.
Art. 52. A autenticidade e veracidade das informações prestadasà Anvisa são de responsabilidade do titular do produto, sendoque qualquer irregularidade detectada pela Anvisa, em contrariedadeao disposto na legislação sanitária pertinente, constitui infração sanitária,nos termos da Lei nº 6.437, de 20 de agosto de 1977, semprejuízo das responsabilidades civil, administrativa e penal cabíveis, eresultará no cancelamento da comunicação prévia de comercializaçãodo produto nos termos desta Resolução.
Art. 53. Ficam revogadas a Portaria nº 1. 480, de 1990, aPortaria nº 97, de 1996, e o art. 2° da Resolução da Diretoria Colegiada- RDC nº 10, de 1999.
Art. 54. O art. 1° da Resolução da Diretoria Colegiada RDCnº 10, de 1999, passa a vigorar com a seguinte redação:
"Art. 1° As mamadeiras, chupetas, mordedores e bicos nãosão passíveis de registro na Agência Nacional de Vigilância Sanitária- Anvisa, estando, porém, sujeitos ao regime de vigilância sanitáriapara os demais efeitos da Lei nº 6.360, de 23 de setembro de 1976, doDecreto nº 8077, de 14 de agosto de 2013, e legislação correlatacomplementar." (NR)
Art.55. Esta Resolução entra em vigor na data de sua publicação.
JARBAS BARBOSA DA SILVA JR.
ANEXO I
REQUISITOS TÉCNICOS ESPECÍFICOS PARA REGULARIZAÇÃO DOS PRODUTOS DESCARTÁVEIS
ANEXO II

ANEXO III
REQUISITOS SOBRE ROTULAGEM OBRIGATÓRIA GERAL PARA PRODUTOS DESCARTÁVEIS
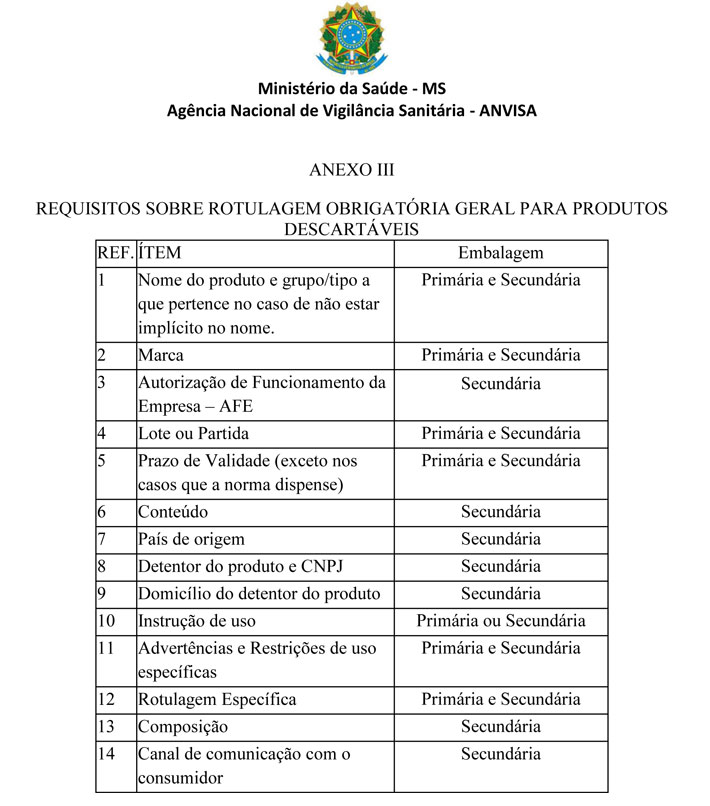
1 - Quando não existir embalagem secundária toda a informação requerida deve figurar na Embalagem Primária.
2- Quando estiver disponível, a descrição qualitativa dos componentes da fórmula deverá ser declarada por meio de sua designação genérica, utilizando a codificação de substâncias estabelecida pela Nomenclatura Internacional de Ingredientes Cosméticos (INCI).
Este conteúdo não substitui o publicado na versão certificada.


Deixar comentário
Para comentar é preciso fazer login no sistema.