RDC Nº 81, de 5 de novembro de 2008
publicado em 05/11/2008
Ministério da Saúde - MS - Agência Nacional de Vigilância Sanitária - ANVISA
RESOLUÇÃO DA DIRETORIA COLEGIADA - RDC Nº 81, DE 5 DE NOVEMBRO DE 2008 (*) (Publicada em DOU nº 216, de 06 de novembro de 2008)
(Republicada em DOU nº 219, de 11 de novembro de 2008)
(Revogadas as disposições aplicáveis à Lista "C4", às substâncias e aos medicamentos antirretrovirais pela Resolução – RDC nº 103, de 31 de agosto de 2016)
Dispõe sobre o Regulamento Técnico de Bens e Produtos Importados para fins de Vigilância Sanitária.
A Diretoria Colegiada da Agência Nacional de Vigilância Sanitária, no uso da atribuição que lhe confere o inciso IV do art. 11 do Regulamento aprovado pelo Decreto nº 3.029, de 16 de abril de 1999, e tendo em vista o disposto no inciso II e nos §§ 1º e 3º do art. 54 do Regimento Interno aprovado nos termos do Anexo I da Portaria nº 354 da ANVISA, de 11 de agosto de 2006, republicada no DOU de 21 de agosto de 2006, em reunião realizada em 11 de setembro de 2008, e
considerando o disposto nas Leis nº 6.360, de 23 de setembro de 1976, nº 6.368, de 21 de outubro de 1976, nº 8.078, de 11 de setembro de 1990, nº 8.080, de 19 de setembro de 1990, nº 9.434, de 4 de fevereiro de 1997, nº 9.782, de 26 de janeiro de 1999, nº 9.787, de 10 de fevereiro de 1999, no Decreto-lei nº 986, de 21 de outubro de 1969, nos Decretos nº 79.094, de 5 de janeiro de 1977, nº 87, de 15 de abril de 1991, nº 2.268, de 30 de junho de 1997, e nas Resoluções do Grupo Mercado Comum - GMC, internalizadas no país;
considerando a necessidade de promover a revisão do controle e fiscalização de bens e produtos importados sob vigilância sanitária, bem como harmonizar a terminologia empregada de comércio exterior;
considerando a necessidade de prescrever obrigações das pessoas, físicas ou jurídicas, de direito público ou privado, envolvidas nessas atividades,
adota a seguinte Resolução da Diretoria Colegiada e eu, Diretora-Presidente, substituta, determino a sua publicação:
Art. 1º Aprovar Regulamento Técnico de Bens e Produtos Importados para fins de Vigilância Sanitária, conforme Capítulos desta Resolução.
§ 1º Aprovar critérios de modelos para fins de autorização de importação de que trata esta Resolução, a serem disponibilizados no endereço eletrônico da ANVISA, www.anvisa.gov.br.
§ 2º Aprovar a comprovação documental para fins da autorização de importação de que trata esta Resolução, conforme Capítulos desta Resolução.
Art. 2º Para efeitos de regularização de serviços de importação de bens e produtos de que trata a Resolução-RDC nº 61, de 19 de março de 2004, § 1º, do artigo 1º, passa a vigorar com a seguinte redação:
"Art. 1º
.........................................................................................................
§ 1º "Consideram-se serviços de importação procedida por intermediação predeterminada àqueles prestados por pessoa jurídica que promova despacho aduaneiro de mera importação de bem e produto sujeito à vigilância sanitária, adquirida no exterior, em razão de contrato firmado com terceiro, empresa autorizada/licenciada junto ao Sistema Nacional de Vigilância Sanitária - SNVS, detentora da regularização do produto perante o órgão de vigilância sanitária pertinente." (NR)
Art. 3º A identificação das mercadorias conforme tipo de procedimento administrativo e Nomenclatura Comum Mercosul - NCM -, constantes do Capítulo XXXIX desta Resolução, serão disponibilizadas no sítio eletrônico www.anvisa.gov.br, e produzirão seus efeitos legais para sua classificação na importação de mercadorias.
Art. 3º A Nomenclatura Comum do Mercosul (NCM) de mercadorias sujeitas a tratamento administrativo pela Anvisa serão disponibilizadas no Portal da Agência na internet. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
Parágrafo único. O importador deverá selecionar o procedimento administrativo adequado ao tipo de mercadoria, quando realizar o peticionamento e a instrução do processo de importação. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
Art.4º O descumprimento ou inobservância no disposto nesta Resolução configura infração de natureza sanitária, nos termos da Lei nº 6.437, de 1977.
Art. 5º Revoga-se a Resolução RDC nº 350, de 28 de dezembro de 2005 e a Resolução RDC nº 217, de 15 de dezembro de 2006 e as disposições em contrário.
Art. 6º Esta Resolução entra em vigor na data de sua publicação.
MARIA CECÍLIA MARTINS BRITO
ANEXO
REGULAMENTO TÉCNICO DE BENS E PRODUTOS IMPORTADOS PARA FINS DE VIGILÂNCIA SANITÁRIA
CAPÍTULO I
TERMINOLOGIA BÁSICA
1. Para os efeitos do disposto neste Regulamento serão adotadas as definições deste Capítulo.
1.1. Amostra: representação por quantidade, fragmentos ou partes de qualquer matéria-prima, produto ou demais bens de que trata este Regulamento, estritamente necessário para dar a conhecer sua natureza, espécie e qualidade.
1.2. Análise Fiscal: aquela efetuada em bens ou produtos de que tratam este Regulamento, em caráter de rotina, para a apuração de infração ou verificação de sua conformidade com os padrões estabelecidos na legislação sanitária pertinente.
1.3. Análise de Controle: aquela cuja colheita da amostra dos bens ou produtos com vistas à importação, ocorre previamente à sua liberação para consumo no território nacional, e destina-se à comprovação ou verificação da sua conformidade com respectivo padrão de identidade e qualidade.
1.4. Autorização de embarque: autorização a ser concedida pela ANVISA à importação de bens e produtos, sujeita à anuência previamente a data do seu embarque no exterior.
1.5. Autoridade Sanitária: autoridade que tem diretamente a seu cargo, a aplicação das medidas sanitárias apropriadas de acordo com a legislação e regulamentação pertinentes.
1.6. Bagagem: os objetos, novos ou usados, destinados ao uso ou consumo pessoal do viajante, que, pela quantidade, natureza ou variedade, são compatíveis com as circunstâncias de sua viagem, não permitindo presumir importação para fins comerciais ou industriais.
1.6.1. Bagagem Acompanhada: aquela que o viajante traz consigo, no mesmo meio de transporte em que viaja, não sujeita a conhecimento de carga ou documento equivalente.
1.6.2. Bagagem Desacompanhada: aquela que chega ao país, sujeita a conhecimento de carga ou documento equivalente.
1.7. Bioequivalência: demonstração de equivalência farmacêutica entre produtos apresentados sob a mesma forma farmacêutica, contendo idêntica composição qualitativa e quantitativa de princípio ativo ou de princípios ativos, e que tenham comparável biodisponibilidade, quando estudados sob um mesmo desenho experimental.
1.8. Biodisponibilidade: indicador de velocidade e extensão de absorção de um princípio ativo em uma forma de dosagem, com base em sua curva concentração/tempo na circulação sistêmica ou sua excreção na urina.
1.9. Conhecimento de Carga (embarque): documento emitido, na data de embarque do bem ou produto, pelo transportador ou consolidador, constitutivo do contrato de transporte internacional e prova da disposição do bem ou produto para o importador (Carga embarcada aérea - Air Waybill /AWB, Carga embarcada aquática -
Bill Landing /BL e Carga embarcada terrestre: Conhecimento de Transporte Internacional por Rodovia /CTR).
1.10. Controle da Qualidade: medidas ou conjunto de medidas destinadas a verificar condições de atividade, pureza, eficácia e segurança de bens e produtos sob vigilância sanitária, por lote ou outro critério de representação de controle, conforme o caso, de acordo com a legislação pertinente.
1.11. Desembaraço Aduaneiro de importação: ato final do despacho aduaneiro.
1.12. Despacho Aduaneiro de Importação: ato em procedimento fiscal que verifica a exatidão dos dados declarados pelo importador em relação aos bens e produtos importados, a título definitivo ou não, com vista ao seu desembaraço aduaneiro, de acordo com a legislação pertinente.
1.13. Despacho Antecipado: modalidade de despacho aduaneiro de bens e produtos em que o registro da declaração de importação - DI pode ser feito na unidade de despacho, antes da chegada dos bens e produtos.
1.14. Destinatário da remessa: Pessoa à qual é dirigido o envio postal ou expresso.
1.15. Detentor do Documento de regularização do Produto na ANVISA: designação dada ao titular do registro, do cadastro, da autorização de modelo, do comunicado, da notificação ou do protocolo pertinente do bem ou produto perante a ANVISA.
1.16. Embalagem: invólucro, recipiente ou qualquer forma de acondicionamento, removível ou não, que se destina a cobrir, empacotar, envasar, proteger ou manter, especificamente ou não, os bens e produtos importados.
1.17. Embalagem Externa: aquela utilizada exclusivamente para a proteção de bens e produtos nas operações de movimentação (embarque, desembarque e transporte) e armazenagem.
1.18. Embalagem Primária: acondicionamento que está em contato direto com o bem ou produto e que pode se constituir em recipiente, envoltório ou qualquer outra forma de proteção, removível ou não, que se destina a envasar ou manter, cobrir ou empacotar.
1.19. Embalagem Secundária: envoltório destinado a conter a(s) embalagem(ns) primária(s).
1.20. Empresa de Remessa Expressa, "Courier": aquela que tem como atividade preponderante à prestação de serviços de transporte internacional expresso, porta a porta, de remessa expressa destinada a terceiros, em fluxo regular e contínuo.
1.21. Encomenda Aérea Internacional: forma de transporte de bens e produtos por empresas aéreas, sob encomenda, sujeita a controle sanitário.
1.22. Ensaio de proficiência: material utilizado em programas para determinação do desempenho de ensaios ou medições específicos por meio de comparações inter laboratoriais.
1.23. Entrega Fracionada: importação por um único importador que, por razões de volume ou peso do bem ou produto, não pode ser realizada em apenas um veículo transportador.
1.24. Exportador: pessoa, física ou jurídica, responsável pela remessa de bens e produtos de outro país para o território nacional.
1.25. Fabricante: pessoa jurídica responsável pela unidade fabril onde os bens e produtos foram processados, e tendo sido elaborados em mais de um país, a identificação acessória das pessoas jurídicas responsáveis pelas unidades fabris onde ocorreram seus processamentos.
1.26. Fiscalização Sanitária: procedimentos ou conjunto de procedimentos de atos de análise de documental técnica e administrativa, e de inspeção física de bens ou produtos importados, com a finalidade de eliminar ou prevenir riscos à saúde humana, bem como intervir nos problemas sanitários decorrentes do meio ambiente, da produção e da circulação de bens que, direta ou indiretamente, se relacionam com a saúde pública.
1.27. Importação: entrada no território nacional de bens ou produtos procedentes do exterior.
1.28. Importador por intermediação predeterminada: pessoa jurídica que promove, em seu nome, operação de comércio exterior de importação de bens e produtos sob vigilância sanitária adquiridos por outra empresa detentora da regularização do produto no Sistema Nacional de Vigilância Sanitária, ou autorizada para a atividade de importar matéria-prima com emprego na industria farmacêutica.
1.29. Importador: pessoa física ou jurídica responsável pela entrada de bem ou produto procedente do exterior no território nacional.
1.30. Inspeção Física: conjunto de medidas destinadas a verificar o atendimento da legislação sanitária vigente.
1.31. Instituição de pesquisa: organização, pública ou privada, legitimamente constituída e habilitada na qual são realizadas investigações científicas.
1.32. Licenciamento de Importação: requerimento por via eletrônica junto ao SISCOMEX (Módulo Importação), pelo importador ou seu representante legal, para procedimentos de licenciamento não-automático de verificação de atendimento de exigências para importação de bens e produtos sob vigilância sanitária.
1.33. Local de Entrada: porto, aeroporto, unidade aduaneira ou ponto de fronteira alfandegado declarado pela autoridade aduaneira competente para o trânsito de veículos e realização de operações de carga, descarga, armazenagem ou passagem de bens e produtos sob vigilância sanitária procedentes do exterior.
1.34. Local de Desembaraço: recinto alfandegado onde são realizados o despacho e o desembaraço aduaneiro.
1.35. Loja Franca: loja instalada preferencialmente na zona primária do porto ou aeroporto alfandegado onde se encontra a embarcação ou aeronave, com a finalidade de fornecer as empresas aéreas ou marítimas produtos, nacional ou estrangeira, destinadas a consumo de bordo, ou comercializá-las a passageiros, em viagem internacional, contra pagamento em moeda estrangeira conversível, de acordo com a legislação pertinente.
1.36. Lote: quantidade de um produto obtido em um ciclo de produção de etapas contínuas e que se caracteriza por sua homogeneidade.
1.37. Mala Diplomática ou Consular: volume não sujeito a limites de tamanho e peso, bem como a restrições quanto a sua abertura ou retenção pela autoridade aduaneira, remetido e conduzido, respectivamente, por procedimentos próprios e instrumentos estabelecidos, conforme o caso, que contém:
a) documentos diplomáticos ou consulares, apresentados sob qualquer meio físico;
b) material destinado a uso oficial da representação do Estado acreditado, notadamente papel timbrado, envelopes, selos, carimbos, caderneta de passaporte, insígnias de condecorações;
c) objetos e equipamentos destinados a uso oficial da representação do Estado acreditado, notadamente equipamentos de informática e de comunicação, protegidos pelo sigilo ou cuja remessa e despacho aduaneiro, no regime comum de importação ou de exportação, possam comprometer a segurança daqueles.
1.38. Bens ou Produtos Sob Vigilância Sanitária: materiais, matérias-primas, insumos, partes e peças, produtos acabados, produtos a granel, produtos semi elaborados e produtos in natura, e demais sob vigilância sanitária de que trata a Lei nº 9.782, de 1999, compreendendo, dentre outros, as seguintes classes de bens e produtos:
a) alimento: é toda substância ou mistura de substâncias, no estado sólido, líquido, pastoso ou qualquer outra forma adequada, destinada a fornecer ao organismo humano os elementos normais, essenciais à sua formação, manutenção e desenvolvimento;
b) cosméticos, produtos de higiene pessoal e perfumes: preparações constituídas por substâncias naturais ou sintéticas, de uso externo nas diversas partes do corpo humano, como pele, sistema capilar, unhas, lábios, órgãos genitais externos, dentes e membranas mucosas da cavidade oral, com o objetivo exclusivo ou principal de limpeza, perfume, alteração de sua aparência e ou correção de odores corporais, bem como de proteção, manutenção ou beneficiamento de seu estado;
c) saneante domissanitário: substância ou preparações que tenham finalidade e utilidade de higienização, desinfestação e desinfecção de domicílios, ambientes coletivos ou públicos, lugares de uso comum e tratamento da água, compreendendo: inseticida, raticida, desinfetante, detergente e seus congêneres e outros;
d) padrão e material de referência:
d.1) material de referência: material que tem um ou mais valores de propriedades que são suficientemente homogêneos e bem estabelecidos, para ser usado na calibração de um aparelho, na avaliação de um método de medição ou atribuição de valores a materiais e em programas para determinação do desempenho de ensaios ou medições específicos por meio de comparações inter-laboratoriais;
d.2) padrão de referência:
d.2.1) primário - uma substância cujo elevado grau de pureza e autenticidade foram demonstrados por meio de testes analíticos;
d.2.2) secundário - substância de qualidade e pureza estabelecidos, comparadas a um padrão primário;
e) produtos para diagnóstico in vitro: reagentes, padrões, calibradores, controles e materiais, junto com as instruções para seu uso, que contribuem para realizar uma determinação qualitativa, quantitativa ou semiquantitativa de uma amostra biológica humana e que não estejam destinados a cumprir função anatômica, física ou terapêutica alguma, que não sejam ingeridos, injetados ou inoculados em seres humanos e que são utilizados unicamente para prover informação sobre amostras obtidas do organismo humano;
f) produto médico: aparelhos, instrumentos e acessórios usados em medicina, odontologia e atividades afins, bem como em educação física, em embelezamento ou em correção estética;
f.1) acessório: Produto fabricado exclusivamente com o propósito de integrar um produto médico, outorgando a esse produto uma função ou característica técnica complementar;
g) produto médico usado: produto médico que após seu uso não foi submetido a qualquer processo de reforma ou revisão para colocá-lo nas condições técnicas e operacionais previstas quando de sua regularização perante a ANVISA;
h) produto médico recondicionado: produto médico que, após seu uso, foi submetido a processo de reforma ou revisão, inclusive substituição de componentes, partes e peças, e calibração, testes de qualidade, re-esterilização ou etiquetagem, entre outros serviços necessários para colocá-lo nas condições técnicas e operacionais previstas quando de sua regularização perante a ANVISA, sob responsabilidade expressa da empresa detentora do seu registro;
i) produtos odorizantes de ambientes: produtos de composição aromática a base de substâncias naturais ou sintéticas, que em concentração e veículos apropriados, destina-se principalmente a odorização de ambientes;
j) medicamento: todo produto farmacêutico, tecnicamente obtido ou elaborado, com finalidade profilática, curativa, paliativa ou para fins de diagnóstico;
l) peças de vestuários: quaisquer peças usadas de roupa de uso pessoal, inclusive calçados, importadas por meio de doação internacional;
m) roupas de uso hospitalar: produtos médicos constituídos de quaisquer peças de vestuário, em tecido de algodão ou sintético, a serem utilizados em pessoas e ambientes médico-hospitalar;
n) artefatos de materiais têxteis e sintéticos: quaisquer peças de roupa de cama e banho e outras peças de uso em ambientes, como cortinas, cobertores, lençóis, fronhas, almofadas, etc., importados por meio de doação internacional;
o) matéria-prima: substâncias ativas ou inativas que se empregam na fabricação dos medicamentos e demais produtos sob vigilância sanitária mesmo que permaneçam inalteradas, experimentem modificações ou sejam eliminadas durante o processo de fabricação;
p) matéria-prima alimentar: substância de origem vegetal ou animal, em estado bruto, que, para ser utilizada como alimento, sofre tratamento e ou transformação de natureza física, química ou biológica;
q) produto alimentício: alimento derivado de matéria-prima alimentar ou de alimento in natura adicionado, ou não, de outras substâncias permitidas obtidas por processo tecnológico adequado;
r) ingrediente: quaisquer substâncias, incluídos os aditivos alimentares, empregada na fabricação ou preparação de um alimento e que permanece no produto final, ainda que de forma modificada;
s) insumo: droga ou ingrediente de qualquer natureza, destinado à fabricação de produtos e seus recipientes;
t) células e tecidos: são materiais de natureza humana para fins terapêuticos, incluindo pele, tecidos músculo-esquelético, valva cardíaca, células progenitoras hematopoéticas, células e tecidos germinativos e pré embriões, córneas e outras células e tecidos humanos.
1.39. Movimentação de Bens e Produtos sob Vigilância Sanitária: práticas de embarque, desembarque, transbordo, transporte e armazenagem de bens ou produtos importados em pátios, edificações e demais instalações de terminais aqüaviários, portos organizados, aeroportos e recintos alfandegados.
1.40. Nomenclatura Comum MERCOSUL - Sistema Harmonizado - NCM: nomenclatura utilizada para a obtenção das alíquotas do imposto de importação e outras disposições, no âmbito do MERCOSUL.
1.41. País(es) e local(is) de Fabricação: aquele(s) local(is) e País(es) onde o bem ou produto foi processado e quando elaborada em mais de um localidade e país, a identificação acessória das unidades fabris onde ocorreram seus processamentos.
1.42. País de Procedência: país onde o bem ou produto importado se encontra fisicamente no momento de sua aquisição e de onde sai para o Brasil, independente do país de fabricação e do ponto de embarque final;
1.43. Peso Bruto: peso total do bem ou produto, incluindo seus recipientes, embalagens e demais envoltórios.
1.44. Peso Líquido: peso do bem ou produto livre de qualquer envoltório ou acondicionamento.
1.45. Pesquisa Científica ou Tecnológica: aquela cujos resultados são aplicados no setor saúde e voltados, em última instância, para melhoria da saúde de indivíduos ou grupos populacionais.
1.45.1. Pesquisa Cientifica de Interesse Sanitário: pesquisa cujo objeto não envolva ser humano, porém o seu desenvolvimento poderá oferecer risco(s) à saúde individual ou coletiva.
1.46 Pesquisa envolvendo seres humanos: pesquisa que, individual ou coletivamente, envolva o ser humano, de forma direta ou indireta, em sua totalidade ou partes dele, incluindo o manejo de informações ou materiais.
1.46.1. Pesquisa Clínica: qualquer investigação em seres humanos, envolvendo intervenção terapêutica com produtos registrados ou passíveis de registro, objetivando descobrir ou verificar os efeitos farmacodinâmicos, farmacocinéticos, farmacológicos, clínicos e/ou outros efeitos do(s) produto(s) investigado(s) e/ou identificar eventos adversos ao(s) produto(s) em investigação, averiguando sua segurança e/ou eficácia, que irão subsidiar o seu registro ou a alteração deste junto a ANVISA.
1.47. Produto Acabado/ Terminado: aquele que passa por todas as fases de produção e acondicionamento, pronto para a comercialização e ou entrega ao consumo.
1.48. Produto a Granel: qualquer produto que tenha passado por todas as etapas de produção, sem incluir o processo de embalagem.
1.49. Produto in Natura: alimento de origem vegetal ou animal, que prescinde para seu consumo imediato, apenas, a remoção da parte não-comestível e os tratamentos indicados para a sua perfeita higienização e conservação.
1.50. Produto Semi-Elaborado: mistura de substância que requerem posteriores processos de produção em estabelecimentos autorizados pela autoridade sanitária, antes de sua comercialização ou entrega ao consumo.
1.51. Recintos Alfandegados:
I - de zona primária, os pátios, armazéns, terminais e outros locais destinados à movimentação e ao depósito de bens ou produtos importados ou destinados à exportação, que devam movimentar-se ou permanecer sob controle aduaneiro, assim como as áreas reservadas à verificação de bagagens destinadas ao exterior ou dele procedentes e as dependências de lojas francas;
II - de zona secundária, os entrepostos, depósitos, terminais ou outras unidades destinadas ao armazenamento de bens e produtos nas condições do inciso anterior, assim como as dependências destinadas ao depósito de remessas postais internacionais sujeitas ao controle aduaneiro.
1.52. Regimes Aduaneiros Especiais:
a) Admissão Temporária: aquele que permite a importação de bens e produtos, submetidas à identificação e termo de responsabilidade, por prazo determinado de permanência no país justificado mediante comprovação por meio idôneo e adequado para essa finalidade, com suspensão total do pagamento de tributos, ou proporcional o pagamento ao tempo de permanência, no caso de utilização econômica, passível de anuência prévia para obtenção de licença de importação, de acordo com o Decreto nº 4.543, de 26 de dezembro de 2002, Livro IV, Capítulo III (Regulamento Aduaneiro);
b) Depósito Especial - DE: aquele que permite a estocagem, com suspensão do pagamento de impostos, de partes, peças, componentes e materiais de reposição ou manutenção, para veículos, máquinas, equipamentos, aparelhos e instrumentos, estrangeiros, nacionalizados ou não, empregados nas atividades de:
b.1) diagnose, cirurgia, terapia e pesquisas médicas realizadas por hospitais, clínicas de saúde e laboratórios;
b.2) análise e pesquisa científica, realizadas em laboratórios.
c) Drawback: aquele de incentivo à exportação, aplicado, na forma do Decreto nº 4.543, de 26 de dezembro de 2002, no Livro IV, Capítulo IV, nas modalidades de suspensão, isenção e restituição total ou parcial de tributos;
d) Entreposto Aduaneiro na Importação: aquele que permite a armazenagem de bens e produtos estrangeiros em recinto alfandegado de uso público, ou permanência em feira, congresso, mostra ou evento semelhante realizada em recinto de uso privativo,
previamente alfandegado para esse fim, por prazo determinado, com suspensão do pagamento de impostos incidentes na importação;
e) Trânsito Aduaneiro: regime que permite o transporte de bens e produtos, sob controle aduaneiro, de um ponto a outro do território aduaneiro, ou seja, do local de entrada do bem ou produto ao local de desembaraço.
1.53. Remessa Postal Internacional: bens e produtos sob vigilância sanitária transportada por meio de encomenda internacional pela Empresa Brasileira de Correios e Telégrafos - ECT.
1.54. Remessa Expressa: documento ou encomenda internacional transportada por via aérea, por empresa de "courier", que requer rapidez no translado e recebimento imediato por parte do destinatário.
1.55. Representante Legal: pessoa física ou jurídica investida de poderes legais para praticar atos em nome do agente regulado, preposta de gerir ou administrar seus negócios no âmbito da ANVISA.
1.56. Responsável Legal: pessoa física designada em estatuto, contrato social ou ata, incumbida de representar, ativa e passivamente, nos atos judiciais e extrajudiciais, o agente regulado pessoa jurídica.
1.57. Responsável Técnico: pessoa física legalmente habilitada para o exercício profissional de atividade nas diversas etapas do processo de produção e prestação de serviços nas empresas, em cada estabelecimento.
1.58. Rótulo: identificação impressa ou litografada, bem como os dizeres pintados ou gravados a fogo, pressão, etiqueta ou decalque, aplicados diretamente sobre recipientes, embalagens, invólucros, envoltórios, cartuchos ou qualquer outro protetor de embalagem interno ou externo.
1.59. Sistema Integrado de Comércio Exterior - SISCOMEX: instrumento administrativo que integra as atividades de registro, acompanhamento e controle das operações de comércio exterior, mediante fluxo único, computadorizado de informações.
1.60. Tabela de Tratamento Administrativo: aquela que define a NCM e os destaques de Capítulo, Posição e de NCM referentes aos bens ou produtos sujeitos à anuência previa e expressa da ANVISA.
1.61. Terminais Alfandegados de Uso Público: instalação destinada à prestação dos serviços públicos de movimentação e armazenagem de bens e produtos que estão sob controle aduaneiro, não localizado em área de porto ou aeroporto:
a) Estação Aduaneira de Fronteira (EAF): situa-se em zona primária de ponto alfandegado de fronteira ou em área contígua;
b) Terminal Retroportuário Alfandegado (TRA): situa-se em zonas contíguas às de porto organizado ou instalação portuária, alfandegados;
c) Estação Aduaneira de Interior (EADI) ou Porto Seco: situa-se em zonas secundárias.
1.62. Vigilância Sanitária: conjunto de ações capazes de eliminar, diminuir ou prevenir riscos à saúde e de intervir nos problemas sanitários decorrentes do meio ambiente, da produção e circulação de bens e da prestação de serviços de interesse da saúde, abrangendo:
a) controle de bens de consumo que, direta ou indiretamente, se relacionam com a saúde, compreendida todas as etapas e processos, da produção ao consumo; e
b) controle da prestação de serviços que se relacionam, direta ou indiretamente, com a saúde.
CAPÍTULO II
DISPOSIÇÕES GERAIS DE IMPORTAÇÃO
A importação de bens ou produtos sob vigilância sanitária deverá ser precedida de expressa manifestação favorável da autoridade sanitária, na forma deste Regulamento.
1. Somente será autorizada à importação, entrega ao consumo, exposição à venda ou à saúde humana a qualquer título, de bens e produtos sob vigilância sanitária, que atendam as exigências sanitárias de que trata este Regulamento e legislação sanitária pertinente.
1.1. Os bens e produtos sob vigilância sanitária, destinados ao comércio, à indústria ou consumo direto, deverão ter a importação autorizada desde que estejam regularizados formalmente perante o Sistema Nacional de Vigilância Sanitária no tocante à obrigatoriedade, no que couber, de registro, notificação, cadastro, autorização de modelo, isenção de registro, ou qualquer outra forma de controle regulamentada pela Agência Nacional de Vigilância Sanitária.
1.2. A autorização de importação de bens e produtos sob vigilância sanitária por pessoa física ou jurídica dar-se-á obrigatoriamente a partir do cumprimento de diretrizes técnico-administrativas e de requerimento por meio de peticionamento, eletrônico ou manual, disponibilizados e regulamentados pela ANVISA.
1.2.1. Na hipótese de requerimento por meio de peticionamento manual, é obrigatória a apresentação da Guia de Recolhimento da União (GRU), da Secretaria do Tesouro Nacional e do seu respectivo comprovante de pagamento, conforme disposto na legislação, bem como no instrumento de procuração do importador, com delegação de poderes perante a ANVISA, ao representante legal responsável pelo desembaraço.
(Incluído pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1.3. As informações integrantes do peticionamento, eletrônico ou manual, de que trata o subitem anterior relativas à importação de bens e produtos, na forma deste Regulamento, deverão corresponder fidedignamente às constatadas quando da sua inspeção e fiscalização sanitária.
2. Em caráter emergencial ou temporário, considerando o contexto epidemiológico internacional, humano, animal ou vegetal, ou a implantação de programas de saúde pública relacionados ao controle sanitário de bens e produtos e de pessoas físicas ou jurídicas envolvidas nos processos de fabricação e prestação de serviço, a autoridade sanitária poderá proibir a importação ou entrada dos bens ou produtos de que trata o subitem 1.38 do Capítulo I deste Regulamento.
3. Caberá ao importador e/ou detentor da regularização do produto a obrigação pelo cumprimento e observância das normas regulamentares e legais, medidas, formalidades e exigências ao processo administrativo de importação, em todas as suas etapas, desde o embarque no exterior até a liberação sanitária no território nacional.
3.1. Incluir-se-á no disposto neste item a obrigação de adotar medidas idôneas, próprias e junto a terceiros contratados para a importação de bens ou produtos sob vigilância sanitária, que evitem ou impeçam prejuízo à saúde.
3.2. O disposto neste item não eximirá o terceiro contratado de cumprir e observar as normas regulamentares e legais, medidas, formalidades e exigências previstas neste Regulamento.
4. Na importação de bens e produtos sob vigilância sanitária com classificação tarifária - NCM/SH - não prevista no Capítulo XXXIX deste regulamento, a autoridade sanitária estará desobrigada de efetuar perante o SISCOMEX operações de exigência, autorização de embarque e de deferimento ou indeferimento no Licenciamento de importação.
4.1. O disposto neste item não exime a fiscalização sanitária.
5. Os prazos para as medidas, formalidades e exigências previstas neste Regulamento contar-se-ão a partir do primeiro dia útil a contar da data do seu recebimento.
6. A importação de bens ou produtos em Regime Especial de Drawback deverá atender o disposto neste Regulamento.
CAPÍTULO III
MODALIDADES DE IMPORTAÇÃO
SEÇÃO I
DO SISCOMEX - MÓDULO IMPORTAÇÃO
Subseção I
Das Disposições Gerais
1. A importação de bens e produtos sujeitos ao licenciamento não automático no Sistema Integrado de Comércio Exterior - SISCOMEX, dispostos no Capítulo XXXIX deste Regulamento, destinada à pessoa física ou jurídica, de direito público ou privado, sujeitar-se-á obrigatoriamente a prévia e expressa anuência da ANVISA por meio de deferimento da licença de importação, como entidade integrante do sistema.
2. O importador de bens e produtos sob vigilância sanitária além de cumprir as exigências sanitárias previstas neste Regulamento para as diferentes finalidades de importação, deverá apresentar à autoridade sanitária competente da ANVISA o pleito de fiscalização e liberação sanitária da importação, por meio de petição para fiscalização e liberação sanitária de que trata o subitem 1.2. do Capítulo II deste Regulamento.
Subseção II
Do Registro do Licenciamento de Importação
3. O registro do licenciamento de importação deverá ser feito pelo importador ou seu representante legal, habilitado, por meio do SISCOMEX, Módulo Importação.
3.1. O importador será responsável perante a autoridade sanitária competente pela classificação do produto na Tabela de Tratamento Administrativo, do SISCOMEX.
3.2. O importador de bens e produtos sujeitos a licenciamento não automático ficará obrigado a registrar mediante o preenchimento dos campos da "Ficha do Fornecedor" da Licença de Importação-LI, no SISCOMEX, as informações relacionadas ao fabricante e exportador.
3.3. O importador de aparelhos, instrumentos e acessórios integrantes da classe de produto médico ficará obrigado a registrar nos campos da "ficha mercadoria", da Licença de Importação-LI, no SISCOMEX, as informações referentes à:
a) identificação do produto, nome, especificação (cada especificação deverá corresponder a um item) e modelo ou apresentação comercial, assim como das partes e acessórios que o acompanhem;
b) condição do produto, se novo ou recondicionado.
3.4. O importador deverá obrigatoriamente registrar no campo "informações complementares" da Licença de Importação-LI: (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) número ou código da regularização da empresa importadora no tocante a Autorização de Funcionamento de Empresa especificando atividade(s) quando se tratar de importação de produtos pertencentes as classes de medicamentos, cosméticos, perfumes, produtos de higiene pessoal, saneantes, produtos médicos, produtos para diagnóstico in vitro, matéria-prima e insumos destinados à industria farmacêutica; bem como as importações terceirizadas sob status de conta e ordem; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) número ou código da regularização da empresa importadora de alimento no tocante a Licença/Alvará de Funcionamento junto ao órgão sanitário competente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3.5. No campo da "ficha mercadoria" da Licença de Importação - LI, a regularização do produto e respectiva validade no Sistema Nacional de Vigilância Sanitária - SNVS.
3.5. Quando se tratar de importação de produtos sob vigilância sanitária passíveis de regularização perante a Anvisa, o importador deverá registrar no campo apropriado da petição para fiscalização e liberação sanitária, eletrônica ou manual, o número da regularização do produto, bem como o número do lote, ou de partida ou de série ou part number. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
4. A importação de produtos destinados à indústria e comércio deverá efetuar-se á, exclusivamente, por meio de registro no SISCOMEX, Módulo Importação, respeitadas as diretrizes para as demais finalidades de importação previstas nos demais Capítulos deste Regulamento.
5. A importação de bens e produtos quando sujeito a licenciamento não automático-LI - SISCOMEX, dispostas em Nomenclatura Comum do MERCOSUL - NCM, deverá atender aos procedimentos administrativos e exigências documentais integrantes do Capítulo XXXIX deste Regulamento.
5. A importação de bens e produtos, quando sujeita a licenciamento não automático-LI - SISCOMEX, disposta em Nomenclatura Comum do MERCOSUL (NCM), deverá atender aos procedimentos administrativos e exigências documentais integrantes deste Regulamento. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
Subseção III
Da Autorização de Embarque do Licenciamento de Importação
6. Não será concedida autorização de embarque ou deferimento do Licenciamento de Importação-LI, de bens e produtos integrantes dos procedimentos administrativos descritos no Capítulo XXXIX, que não atendam às exigências sanitárias dispostas neste Regulamento ou em outros diplomas legais sanitários em vigência.
7. A análise técnica sanitária da ANVISA para fins de autorização de embarque no exterior em licenciamento de importação de bem ou produto sob vigilância sanitária perderá seus efeitos, para os fins deste Regulamento, 120 (cento e vinte) dias após sua anuência pela autoridade sanitária.
7.1. Excluir-se-á do disposto neste item à análise técnica para fins de autorização de embarque no exterior em licenciamento de importação de bens ou produtos sob vigilância sanitária, vinculadas a programas públicos de saúde ou pesquisa cientifica, tecnológica e de inovação (na forma da Lei) que perderá seus efeitos, para fins deste Regulamento, 360 (trezentos e sessenta) dias a contar do seu protocolo na ANVISA.
Subseção IV
Do Deferimento do Licenciamento de Importação
8. O deferimento do Licenciamento de Importação pela ANVISA implicará na fiscalização dos bens e produtos antes do desembaraço aduaneiro, a critério da autoridade sanitária competente ou sempre que assim for exigido por força deste Regulamento. (Revogado pela Resolução – RDC nº 228, de 23 de maio de 2018)
9. O deferimento do Licenciamento de Importação dar-se-á após cumprimento, pelo importador, das exigências sanitárias ou nos casos previstos nos Capítulos deste Regulamento.
Subseção V
Do Licenciamento de Importação Substitutivo
10. A anuência do Licenciamento de Importação Substitutivo pela autoridade sanitária ocorrerá a partir de contexto fiscal, se conclusivo e satisfatório, vinculado ao licenciamento de importação que o precedeu, desde que a alteração que facultou esse registro substitutivo - SISCOMEX - Módulo Importação, tenha sido informada e não se apresente em desacordo com a fiscalização e/ou conclusão da fiscalização sanitária antecedente.
10.1. Para os casos de substituição do LI, decorrentes de alterações específicas em informações de caráter monetário, cambial e tributário, sem implicações para a fiscalização sanitária e cujo embarque já tenha sido autorizado no LI substituído, fica o LI substitutivo dispensado de nova manifestação do setor técnico competente.
Subseção VI
Da Validade do Processo de Importação
11. O processo de importação/DATAVISA que contém a Petição de que trata o Capítulo II, subitem 1.2, findo o prazo de até 150 (cento e cinquenta) dias a contar do seu protocolo na ANVISA deverá ser indeferido e arquivado, junto ao Sistema de Informações DATAVISA.
12. O processo de importação, de que trata o subitem 7.1, que contém a Petição de que trata o Capítulo II, subitem 1.2., findo o prazo estabelecido deverá ser indeferido e arquivado junto ao Sistema de Informações DATAVISA.
SEÇÃO II
DA REMESSA EXPRESSA, REMESSA POSTAL E ENCOMENDA AÉREA INTERNACIONAL
13. A importação de bens ou produtos por meio de remessa expressa, remessa postal ou encomenda aérea internacional, destinada à pessoa física ou jurídica, de direito público ou privado, sujeitar-se-á obrigatoriamente às exigências sanitárias previstas neste Regulamento, outras normas sanitárias, ou determinadas pela autoridade sanitária.
13.1. Constituir-se-á exigência sanitária a fiscalização sanitária antes do desembaraço aduaneiro e entrega para fins de exposição ou consumo humano.
13.2. Fica autorizada, no desenvolvimento da vigilância sanitária em recintos alfandegados instalados em empresas que operem remessa postal ou remessa expressa, a utilização dos recursos técnicos disponibilizados por equipamentos scanners, com vistas à visualização e à percepção de produtos sob vigilância sanitária.
13.2.1. A visualização de que trata o subitem anterior deverá servir como orientação para o implemento de comportamentos fiscais de maior precisão, na impossibilidade de cobertura fiscal diária em 100% dos bens ou produtos sob suas competências.
14. Será vedada a entrada no território nacional de:
a) bens e produtos proibidos previstos no Procedimento 1A deste Regulamento e em demais atos normativos externados pelas Diretorias que integram a Direção Colegiada da ANVISA.
b) bens e produtos desprovidos de identificação em suas embalagens primária e/ou secundária originais.
15. A autoridade sanitária competente, em exercício no local de desembaraço, está autorizada a conceder rechaço sanitário imediato do bem, material ou produto sob importação, que não teve a sua nacionalização autorizada, por não atendimento as exigências sanitárias em vigência no território nacional.
15.1. Excetuar-se-ão do disposto os bens, materiais ou produtos cujas operações de manejo para fins de rechaço, coloquem em risco a saúde de pessoas sob transporte internacional ou ocupacionalmente expostas.
16. Os bens ou produtos sob vigilância sanitária de que trata este Capítulo não podem caracterizar-se, em quantidade importada ou freqüência de importação, com fins de comércio ou revenda.
Subseção I
Remessa Expressa
17. A empresa de remessa expressa responsável pela importação do bem ou produto sob vigilância sanitária deverá apresentar à autoridade sanitária competente da ANVISA o pleito, por meio de petição, para fiscalização e liberação sanitária de que trata o subitem 1.2. do Capítulo II deste Regulamento, acompanhado dos seguintes documentos:
a) conhecimento de carga embarcada vinculado à importação - MAWB e HAWB.
b) Guia de Recolhimento da União, da Secretaria do Tesouro Nacional - GRU, conforme previsto em legislação sanitária pertinente.
17.1. O documento de que trata o item anterior, alínea "a", deverá ser apresentado na sua forma original carbonada ou eletrônica, o qual ficará retido.
17.2. Serão consideradas informações obrigatórias para fins de análise técnica da importação pela autoridade sanitária e de apresentação obrigatória, nos casos de importações realizadas por pessoa jurídica:
a) nome comercial, quando se tratar de produto acabado ou a granel, quando couber;
b) nome do princípio ativo base da formulação de medicamento;
c) o nome comum ou o nome técnico, químico ou biológico do bem ou produto, quando se tratar de insumo ou de matéria-prima destinados à produção de medicamentos, cosméticos, perfumes, produtos de higiene pessoal, saneantes e produtos para diagnóstico in vitro;
d) o nome da matéria-prima alimentícia;
e) finalidade da importação, conforme Quadro I do Capítulo XL, deste Regulamento, nos casos de importação por pessoa jurídica;
f) classe do produto, em conformidade com o item 1.38 do Capítulo I deste Regulamento;
g) natureza do produto, conforme Quadro II do Capítulo XL, deste Regulamento, nos casos de importação por pessoa jurídica;
h) condição do produto médico (novo ou recondicionado);
i) nome da empresa transportadora e quando couber o CNPJ;
j) nome, CNPJ ou CPF e endereço completo do importador do produto; l) nome e endereço completo do remetente do produto.
17.3 Serão consideradas informações complementares, a critério da autoridade sanitária, para fins de análise técnica conclusiva da importação, nos caso de importação realizada por pessoa física para uso próprio ou individual em quantidade e freqüência que não configure comércio:
a) nome comercial quando se tratar de produto acabado quando couber; b) nome do princípio ativo base da formulação de medicamento;
c) finalidade da importação, conforme Quadro I do Capítulo XL, deste Regulamento;
d) classe do produto, em conformidade com o subitem 1.38 do Capítulo I deste Regulamento;
e) natureza do produto, conforme Quadro II do Capítulo XL, deste Regulamento; f) condição do produto médico (novo ou recondicionado);
g) nome, CNPJ ou CPF e endereço completo do destinatário do produto; h) nome e endereço completo do remetente do produto.
Subseção II
Remessa Postal
18. Deverão constar obrigatoriamente na embalagem externa da remessa postal, as informações referentes à identificação geral do(s) bem(s) ou produto(s) sob vigilância sanitária importado e o nome e endereço do destinatário.
19. Serão consideradas informações complementares, a critério da autoridade sanitária, para fins de análise técnica conclusiva da importação:
a) nome comercial quando se tratar de produto acabado quando couber; b) nome do princípio ativo base da formulação de medicamento;
c) finalidade da importação, conforme Quadro I do Capítulo XL, deste Regulamento;
d) classe do produto, em conformidade com o subitem 1.38 do Capítulo I deste Regulamento;
e) natureza do produto, conforme Quadro II do Capítulo XL, deste Regulamento;
Este texto não substitui o(s) publicado(s) em Diário Oficial da União.
Ministério da Saúde - MS
Agência Nacional de Vigilância Sanitária - ANVISA
f) condição do produto médico (novo ou recondicionado);
g) nome, CNPJ ou CPF e endereço completo do destinatário do produto; h) nome e endereço completo do remetente do produto.
Subseção III
Encomenda Aérea Internacional
20. A empresa que opere em serviço de transporte aéreo regular responsável pela importação de encomenda aérea internacional de medicamentos e alimentos de uso contínuo ou nutricional especial, destinados a pessoa física residente no País, deverá apresentar o bem ou produto à autoridade sanitária competente da ANVISA, acompanhado dos seguintes documentos:
a) declaração para fins de despacho aduaneiro pertinente;
b) receituário em conformidade com o item 4, Seção II, Capítulo XII; c) fatura ou nota de aquisição;
d) autorização do destinatário para fins do despacho aduaneiro.
SEÇÃO III
DA DECLARAÇÃO SIMPLIFICADA DE IMPORTAÇÃO NÃO ELETRÔNICA
21. A importação de bem ou produto destinado à pessoa física ou jurídica, de direito público ou privado, cujo desembaraço aduaneiro se fizer por meio de Declaração Simplificada de Importação - DSI, não eletrônica, sujeitar-se-á obrigatoriamente às exigências sanitárias previstas neste Regulamento e outras determinadas pela autoridade sanitária.
21.1. Constituir-se-á exigência sanitária a fiscalização sanitária antes do desembaraço aduaneiro e entrega para fins de exposição ou consumo humano.
22. Além de dar cumprimento as exigências sanitárias previstas neste Regulamento para as diferentes finalidades de importação, o importador deverá apresentar à autoridade sanitária competente da ANVISA o pleito de fiscalização e liberação sanitária da importação, por meio de petição para fiscalização e liberação sanitária de que trata o subitem 1.2. do Capítulo II deste Regulamento, acompanhado, no que couber, dos seguintes documentos:
a) conhecimento de carga embarcada vinculado à importação - MAWB e HAWB, no que couber;
b) Guia de Recolhimento da União, da Secretaria do Tesouro Nacional - GRU, conforme previsto em legislação sanitária pertinente.
22.1. O documento de que trata o item anterior, alínea "a", deverá ser apresentado na sua forma original carbonada ou eletrônica, o qual ficará retido.
22.2. Serão consideradas informações obrigatórias para fins de análise técnica da importação pela autoridade sanitária e de apresentação obrigatória:
a) nome comercial, quando se tratar de produto acabado ou a granel, quando couber;
b) nome do princípio ativo base da formulação de medicamento;
c) o nome comum ou o nome técnico, químico ou biológico do produto, quando se tratar de insumo ou de matéria-prima destinados à produção de medicamentos, cosméticos, produtos de higiene pessoal, saneantes e produtos para diagnóstico in vitro;
d) o nome da matéria-prima alimentícia;
e) finalidade da importação, conforme Quadro I do Capítulo XL, deste Regulamento;
f) classe do produto, em conformidade com o subitem 1.38 do Capítulo I deste Regulamento;
g) natureza do produto, conforme Quadro II do Capítulo XL, deste Regulamento;
h) nome da empresa transportadora e quando couber CNPJ;
i) nome, CNPJ ou CPF e endereço completo do importador do produto; j) nome e endereço completo do remetente do produto.
SEÇÃO IV
DA BAGAGEM ACOMPANHADA E DESACOMPANHADA
(Revogada pela Resolução - RDC nº 28, de 28 de junho de 2011)
23. Os produtos acabados pertencentes às classes de medicamentos, alimentos, produtos médicos, produtos para diagnóstico in vitro, cosméticos, produtos de higiene pessoal e saneantes procedentes do exterior e transportados ou destinados à pessoa física, por meio de bagagem acompanhada ou desacompanhada, sujeitar-se-ão obrigatoriamente às exigências sanitárias previstas neste Regulamento e outras determinadas pela autoridade sanitária, no local de desembaraço no território nacional. (Revogado pela Resolução - RDC nº 28, de 28 de junho de 2011)
24. Fica autorizada, no desenvolvimento da vigilância sanitária, a utilização dos recursos técnicos disponibilizados por equipamentos scanners, com vistas à visualização e à percepção de bens e produtos sob vigilância sanitária. (Revogado pela Resolução - RDC nº 28, de 28 de junho de 2011)
24.1. A visualização de que trata o item anterior deverá servir como orientadora de comportamentos fiscais de maior precisão, fundamentalmente quando da impossibilidade de cobertura fiscal diária em 100% dos produtos sob suas competências fiscais. (Revogado pela Resolução - RDC nº 28, de 28 de junho de 2011)
25. Será vedada a entrada no território nacional de bagagem acompanhada ou desacompanhada de bem e produto procedente do exterior e transportada por pessoa física, descaracterizada como de consumo pessoal ou individual. (Revogado pela Resolução - RDC nº 28, de 28 de junho de 2011)
25.1. A entrada de bens e produtos pertencentes às classes de medicamentos e alimentos de uso contínuo ou nutricional especial, bem como de produtos para diagnóstico in vitro e produtos médicos, destinadas a consumo pessoal somente será autorizada mediante a apresentação perante a autoridade sanitária de prescrição do profissional pertinente, conforme o disposto no Capítulo XII, Seção II. (Revogado pela Resolução - RDC nº 28, de 28 de junho de 2011)
25.2. Excetua-se do disposto os casos previstos na importação de que trata o Capítulo XXXIV. (Revogado pela Resolução - RDC nº 28, de 28 de junho de 2011)
26. Será vedada a entrada no território nacional de: (Revogado pela Resolução - RDC nº 28, de 28 de junho de 2011)
a) células e tecidos destinados para fins terapêuticos não autorizados pela área técnica competente da sede da ANVISA; (Revogado pela Resolução - RDC nº 28, de 28 de junho de 2011)
b) bens e produtos proibidos previstos no Procedimento 1-A deste Regulamento e em demais atos normativos externados pelas Diretorias que integram a Direção Colegiada da ANVISA. (Revogado pela Resolução - RDC nº 28, de 28 de junho de 2011)
c) bens e produtos desprovidos de identificação em suas embalagens primária e/ou secundária originais. (Revogado pela Resolução - RDC nº 28, de 28 de junho de 2011)
27. Em casos de interdição e/ou apreensão, a critério da autoridade sanitária em exercício fiscal no terminal de desembaraço aduaneiro de bagagem, poderá ser autorizada para fim exclusivo de manutenção de tratamento clínico a entrada no território nacional, de parte desse bem ou produto importado. (Revogado pela Resolução - RDC nº 28, de 28 de junho de 2011)
CAPÍTULO IV
EMPRESAS
1. Somente poderão importar os bens e produtos de que tratam este Regulamento as empresas autorizadas pela ANVISA para essa atividade.
1.1. Excluir-se-ão do disposto neste item às empresas importadoras de alimentos, matérias-primas alimentares ou produtos alimentícios, que deverão apresentar na chegada do bem ou produto, documento oficial de regularização da empresa expedido pela autoridade estadual ou municipal.
1.1.1 No caso de terceirização da atividade de armazenagem será obrigatória a apresentação à autoridade sanitária no local de desembaraço, do contrato e regularização da empresa que promoverá a armazenagem, conforme boas práticas de armazenagens previstas na legislação sanitária pertinente.
1.2. Está desobrigada de regularização na ANVISA no tocante a Autorização de Funcionamento, a empresa que exercer a atividade de importar matéria-prima que integrará processos fabris de produtos pertencentes às classes de cosméticos, perfumes, produtos de higiene pessoal, produtos médicos e produtos para diagnóstico in vitro e saneantes.
Observação: Vide o art. 5º, IV da Resolução – RDC nº 16, de 1º de abril de 2014. 2. É vedada a importação de:
2.1. matéria-prima e de insumo farmacêuticos destinados à fabricação de medicamentos por empresa não detentora de Autorização de Funcionamento ou Autorização Especial de Funcionamento, no que couber;
CAPÍTULO V
BENS E PRODUTOS
1. Os bens e produtos sob vigilância sanitária deverão apresentar- se, quando da chegada no território nacional:
a) em conformidade com os Padrões de Identidade e Qualidade - PIQ, exigidos pela legislação sanitária pertinente;
b) com prazo de validade e em vigência, conforme legislação pertinente;
c) com embalagem primária e secundária identificadas em conformidade com as Boas Práticas de Fabricação – BPF
d) com embalagem externa identificada para transporte, movimentação e armazenagem.
2. Consistirá identificação obrigatória da embalagem externa de cada volume de produtos importados de que trata este item:
a) nome comercial, quando se tratar de produto acabado ou a granel, quando couber;
b) nome do princípio ativo base da formulação, quando se tratar de importação exclusiva de medicamento;
c) nome comum ou nome técnico, químico ou biológico do produto, quando se tratar de insumo ou de matéria-prima destinados à produção de medicamentos, cosméticos, perfumes, produtos de higiene pessoal, saneantes e produtos para diagnóstico in vitro e produtos médicos;
d) nome da matéria-prima alimentícia;
e) número ou código do lote ou partida de produção dos produtos embalados; f) nome do fabricante, cidade e País;
g) cuidados especiais para armazenagem, incluindo os relacionados com a manutenção da identidade e qualidade do bem ou produto, como temperatura, umidade, luminosidade, entre outros.
2.1. Excluir-se-ão do atendimento às exigências integrantes do subitem anterior:
a) o produto cuja identificação obrigatória na embalagem externa for regulamentada, na forma deste Regulamento, e em legislação sanitária específica;
b) o produto de que trata os Procedimentos 1 e 1-A, do Capítulo XXXIX, deste Regulamento.
3. As peças de vestuário usadas e artefatos de materiais têxteis e sintéticos usados ou não, objeto de doações internacionais destinadas à pessoa jurídica, de direito público ou privado, quando de sua importação, deverão apresentar-se protegidas e identificadas por embalagem externa.
3.1. Consistirá identificação obrigatória da embalagem externa dos bens ou produtos de que tratam este item:
a) especificação das peças de vestuário de uso pessoal;
b) identificação do país de origem,
c) país e cidade de procedência;
d) identificação do destinatário;
e) identificação quanto ao estado do bem ou produto, se novo, usado ou recondicionado.
4. Será proibida a importação de produtos acabados, semi-elaborado ou a granel ou matéria-prima, para fins industriais, comerciais, de distribuição em feiras ou eventos, pesquisa de mercado e doação internacional, com prazo de validade a expirar-se nos próximos 30 (trinta) dias a partir de sua liberação sanitária.
4.1. Excluir-se-á do disposto neste item, o produto importado acabado, semi elaborado ou a granel para fim industrial ou o produto acabado importado para fim comercial, cujo prazo definido quando de sua aprovação junto a ANVISA ou pelo seu fabricante, seja inferior a 180 (cento e oitenta) dias.
5. É vedada a importação de insumos farmacêuticos destinados à fabricação de medicamentos que ainda não tiveram a sua eficácia terapêutica avaliada pela ANVISA.
5.1. Excetua-se deste item à importação de amostras com a estrita finalidade de pesquisas, desenvolvimento de formulações e trabalhos médicos e científicos.
CAPÍTULO VI
CADASTRO - DESPACHANTE ADUANEIRO
(Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
1. Será obrigatório o cadastro do despachante aduaneiro, perante a Coordenação de Vigilância Sanitária de Portos, Aeroportos e Fronteiras do Estado onde ocorrerá o desembaraço aduaneiro, que, satisfeitas as condições da legislação pertinente, efetivará a competente certificação. (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
2. O cadastro dar-se-á mediante a apresentação dos seguintes documentos e informações: (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
a) cópia da inscrição da pessoa jurídica no Cadastro Nacional de Pessoa Jurídica - CNPJ; (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
b) cópia do contrato social ou ata de constituição, registrado perante a Junta Comercial, e de suas alterações, quando for o caso, com a informação obrigatória e explícita dos objetivos da atividade requerida; (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
c) instrumento de procuração do importador que deverá ser apresentado na sua forma original e cópia, para sua autenticação, ou previamente autenticado, o qual ficará retido, não podendo ter prazo de vigência superior a 12 (doze) meses contados da sua assinatura. O referido instrumento deverá conter na delegação de poderes perante a Agência Nacional de Vigilância Sanitária - ANVISA, obrigatoriamente as seguintes sub-alíneas: (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
c.1) "peticionamento de fiscalização e liberação sanitária para importação de produtos sob vigilância sanitária"; (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
c.2) "acompanhamento das etapas da inspeção sanitária de bens ou produtos sob vigilância sanitária"; (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
c.3) "recepção de amostras de contraprova de produtos sob vigilância sanitária para análises fiscal ou de controle"; (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
c.4) "tomar ciência de termos legais e outros documentos relacionados à fiscalização de produtos sob vigilância sanitária, e apresentação dos meios de defesa, como impugnação, produção de provas e interposição de recursos"; (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
E adicionalmente, as sub-alíneas: (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
c.5) "subscrição de Termo de Guarda e Responsabilidade para autorização da saída de produtos sob vigilância sanitária da área alfandegada com ressalva"; (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
c.6) "efetivação da inutilização de produtos sob vigilância sanitária na forma da legislação sanitária". (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
d) documento subscrito pelo representante legal do importador com relação nominal dos funcionários legalmente habilitados à execução dos poderes delegados no instrumento de procuração de que trata a alínea anterior, com cópia dos respectivos documentos de Cadastro de Pessoa Física - CPF. (Revogado pela Resolução – RDC nº 74, de 02 de maio de 2016)
CAPÍTULO VII
IMPORTAÇÃO TERCEIRIZADA
1. Serão consideradas, para efeito deste Capítulo, importações terceirizadas:
1.1. entre empresas regularizadas na ANVISA no tocante à autorização de funcionamento para as atividades de importar ou importar e fabricar;
1.2. importação procedida por intermediação predeterminada;
1.3. por órgãos e instituições públicas de saúde pública e organismo internacional multilateral.
2. Aplicar-se-á o disposto neste Capítulo à importação de produtos na forma de produtos acabados ou em estágio intermediário, etapa de semi-elaborado e a granel, de seu processo de produção ou de fabricação.
2.1.Excetua-se do disposto no item anterior os bens ou produtos disciplinados por legislação específica.
3. Somente será permitida a importação de produtos, em estágio intermediário de seu processo de produção ou de fabricação, se a empresa detentora do documento de regularização do produto perante a ANVISA for autorizada para as atividades de importar e fabricar.
4. O ingresso no território nacional dar-se-á obrigatoriamente por meio de registro no Sistema Integrado de Comércio Exterior - SISCOMEX.
5. Caberá ao detentor da regularização do produto perante ANVISA:
a) a obrigação pelo cumprimento e observância das normas regulamentares e legais, medidas, formalidades e exigências ao processo administrativo de importação de que trata este Capítulo, em todas as suas etapas, desde o embarque no exterior até a liberação sanitária no território nacional.
b) a execução de ensaios laboratoriais para verificação da garantia e manutenção da identidade e qualidade do produto importado, acabado ou em estágio intermediário de seu processo de produção ou de fabricação, etapas de produto semi-elaborado e a granel, em ambiente laboratorial adequado instalado no território nacional, integrante do cadastro de Autorização de Funcionamento ou Autorização de Funcionamento Especial autorizado pela ANVISA;
c) o cumprimento das Boas Práticas nas operações vinculadas ao transporte, movimentação e armazenagem dos produtos de que trata este Capítulo;
d) a responsabilidade pelas informações exigidas, ainda que prestadas por terceiro, quanto aos bens ou produtos importados.
5.1. Incluir-se-á no disposto neste item à obrigação de adotar medidas idôneas, próprias e junto a terceiros contratados para a importação dos produtos de que trata esse Capítulo, que evitem ou impeçam prejuízo à saúde.
5.2. O disposto neste item não eximirá a empresa terceirizada de cumprir e observar as normas regulamentares e legais, medidas, formalidades e exigências previstas neste Regulamento.
6. Para os fins de recolhimento da Taxa de Fiscalização de Vigilância Sanitária, considerar-se-á o porte da pessoa jurídica detentora da regularização do produto perante a ANVISA.
7. A importação terceirizada dar-se-á mediante a anuência da autoridade sanitária em face da apresentação a cada importação no local de desembaraço da seguinte documentação:
a) Petição para Fiscalização e Liberação sanitária de que trata o subitem 1.2 do Capítulo II deste Regulamento;
b) declaração da pessoa jurídica detentora da regularização do produto junto a ANVISA autorizando a importação, em sua forma original e cópia, para autenticação, ou previamente autenticada, a qual ficará retida, que deverá:
i) estar vinculada a uma única e exclusiva pessoa jurídica, ficando vedado o repasse dessa autorização;
ii) possuir validade jurídica, inclusive não podendo ter prazo de vigência superior a 90 (noventa) dias contados da sua assinatura;
iii) ser subscrita pelo seu responsável legal ou representante legal, e pelo seu responsável técnico, com reconhecimento de firma em cartório;
iv) expressar o compromisso de observância e cumprimento das normas e procedimentos estabelecidos pela legislação sanitária, bem como de ciência das penalidades as quais ficará sujeito, nos termos da Lei nº 6.437, de 20 de agosto de 1977.
c) instrumento de representação da pessoa jurídica detentora da regularização do produto junto a ANVISA a favor do responsável legal ou representante legal, em sua forma original e cópia, para autenticação, ou previamente autenticado, o qual ficará retido.
d) Autorização de Importação por intermediação predeterminada, conforme Capítulo VIII;
7. A importação terceirizada dar-se-á mediante a anuência da autoridade sanitária, face à apresentação, a cada importação, da seguinte documentação: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação sanitária de que trata o subitem 1.2 do Capítulo II desta Resolução; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) declaração da pessoa jurídica detentora da regularização do produto junto à ANVISA, autorizando a importação, e deverá obrigatoriamente: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
i) estar vinculada a 1 (uma) única e exclusiva pessoa jurídica, ficando vedado o repasse dessa autorização; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
ii) possuir validade jurídica, não podendo ter prazo de vigência superior a 90 (noventa) dias contados da sua assinatura; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
iii) ser subscrita pelo seu responsável legal ou representante legal, e pelo seu responsável técnico; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
iv) expressar compromisso de observância e cumprimento das normas e procedimentos estabelecidos pela legislação sanitária, bem como de ciência das penalidades as quais ficará sujeito, nos termos da Lei nº 6.437, de 20 de agosto de 1977. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de Importação por intermediação predeterminada, conforme Capítulo VIII. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
8. A importação promovida por órgãos e instituições públicas não detentores da regularização de bens ou produtos perante a ANVISA, estão isentas da apresentação da documentação constante nas alíneas "c "e "d", do item 7.
9. Na hipótese de importação de produtos acabados pertencentes à classe de alimentos, a pessoa jurídica deverá atender ao disposto no Capítulo IV deste Regulamento, quanto aos critérios referentes às empresas autorizadas para essa atividade.
CAPÍTULO VIII
AUTORIZAÇÃO DE IMPORTAÇÃO PROCEDIDA POR INTERMEDIAÇÃO PREDETERMINADA
AUTORIZAÇÃO DE IMPORTAÇÃO POR INTERMEDIAÇÃO PREDETERMINADA
1. DADOS DO CONTRATANTE DETENTOR DA REGULARIZAÇÃO DO PRODUTO:
1.1 - CNPJ Nº:
1.2 - RAZÃO SOCIAL:
1.3 - ENDEREÇO COMPLETO:
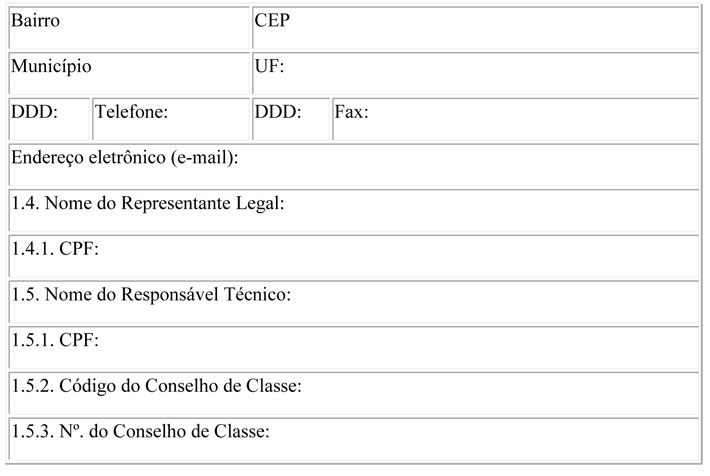
1.6 - LICENÇA SANITÁRIA DE FUNCIONAMENTO:

1.7- AFE Nº:
1.8 - AE Nº:
2. RELAÇÃO DE BENS OU PRODUTOS SOB IMPORTAÇÃO PROCEDIDA POR INTERMEDIAÇÃO PREDETERMINADA:
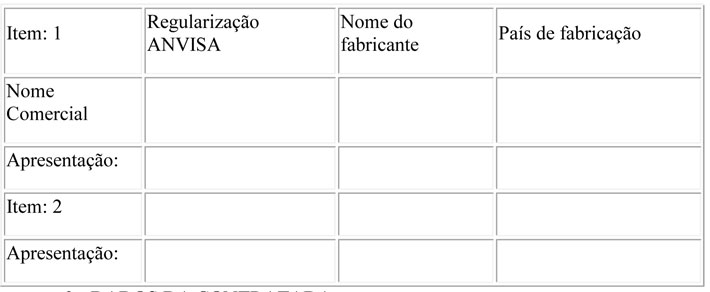
3 - DADOS DA CONTRATADA: 3.1 - CNPJ Nº:
3.2 - RAZÃO SOCIAL:
3.3 - AFE Nº :
3.4 - ENDEREÇO COMPLETO:


CAPÍTULO IX
IMPORTAÇÃO POR UNIDADE HOSPITALAR OU ESTABELECIMENTO DE ASSISTÊNCIA À SAÚDE (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
1. A importação direta por unidade hospitalar ou estabelecimento de assistência à saúde que preste serviço de terapêutica e diagnóstico, de produtos pertencentes às classes de medicamentos, produtos médicos e produtos para diagnóstico in vitro deverá ser precedida, quando do seu embarque no exterior, de registro de Licenciamento de Importação no SISCOMEX, conforme Capítulo III, Subseção II.
1. A importação direta por unidade hospitalar ou estabelecimento de assistência à saúde que preste serviço de terapêutica e diagnóstico, de produtos pertencentes às classes de medicamentos, produtos médicos e produtos para diagnóstico in vitro deverá ser precedida de registro de Licenciamento de Importação no SISCOMEX, conforme Capítulo III, Seção I, Subseção II. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
1.1. O Licenciamento de Importação de que trata este Capítulo deverá ser submetido à autoridade sanitária, em exercício no local do desembaraço do produto, mediante a apresentação de requerimento, por meio da Petição para Fiscalização e Liberação Sanitária de Importação, de que trata o subitem 1.2., Capítulo II deste Regulamento, atendidas as seguintes exigências:
a) O produto deve estar regularizado perante a ANVISA, quando da sua chegada no território nacional;
b) apresentação pela importadora do documento de seu licenciamento pelo órgão de vigilância sanitária, ou Alvará Sanitário, junto ao Estado, Distrito Federal ou Município;
c) A empresa deve estar regularizada perante a ANVISA, quanto a Autorização Especial de Funcionamento para atividade de importar medicamentos submetidos a controle especial, nos termos da Portaria SVS/MS nº 344, de 1998;
d) declaração da pessoa jurídica detentora da regularização do produto, junto a ANVISA autorizando a importação, que será apresentada na sua forma original e cópia, para sua autenticação, ou previamente autenticada, a qual ficará retida, devendo ainda:
i) estar vinculada a uma única e exclusiva pessoa jurídica, ficando vedado o repasse dessa autorização;
ii) possuir validade jurídica, inclusive não podendo ter prazo de vigência superior a 90 (noventa) dias contados da sua assinatura;
iii) ser subscrita pelo seu responsável legal ou representante legal, e pelo seu responsável técnico, com reconhecimento de firma em cartório;
iv) expressar o compromisso de observância e cumprimento das normas e procedimentos estabelecidos pela legislação sanitária, bem como de ciência das penalidades as quais ficará sujeito, nos termos da Lei nº 6.437, de 20 de agosto de 1977.
1.1 O Licenciamento de Importação de que trata este Capítulo deverá ser submetido à autoridade sanitária, por meio da Petição para Fiscalização e Liberação Sanitária de Importação de que trata o subitem 1.2. do Capítulo II desta Resolução, e deverão ser atendidas as seguintes exigências: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
a) O produto deve estar regularizado perante a ANVISA, quando da sua chegada no território nacional; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) (Revogada pela Resolução – RDC nº 383, de 12 de maio de 2020)
b) apresentação pela importadora do documento de seu licenciamento por órgão de vigilância sanitária competente, ou Alvará Sanitário, junto ao Estado, Distrito Federal ou Município; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) (Revogada pela Resolução – RDC nº 383, de 12 de maio de 2020)
c) A empresa deve estar regularizada perante a ANVISA, quanto a Autorização Especial de Funcionamento (AE) para atividade de importar medicamentos submetidos a controle especial, nos termos da Portaria SVS/MS nº 344, de 12 de maio de 1998; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) (Revogada pela Resolução – RDC nº 383, de 12 de maio de 2020)
d) declaração da pessoa jurídica detentora da regularização do produto, junto a ANVISA autorizando a importação, devendo: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) (Revogada pela Resolução – RDC nº 383, de 12 de maio de 2020)
i) estar vinculada a 1 (uma) única e exclusiva pessoa jurídica, ficando vedado o repasse dessa autorização; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
ii) possuir validade jurídica, não podendo ter prazo de vigência superior a 90 (noventa) dias contados da sua assinatura; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
iii) ser subscrita pelo seu responsável legal ou representante legal, e pelo seu responsável técnico; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
iv) expressar compromisso de observância e cumprimento das normas e procedimentos estabelecidos pela legislação sanitária, bem como de ciência das penalidades as quais ficará sujeito, nos termos da Lei nº 6.437, de 20 de agosto de 1977. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
2. Excluir-se-ão da obrigatoriedade de que trata o subitem 1.1., alínea "b", as importações de produtos adquiridos diretamente por instituições públicas integrantes da estrutura organizacional do Sistema Único de Saúde. (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
3. As importações de medicamentos, alimentos especiais e produtos médicos não regularizados na ANVISA destinadas a tratamento clínico, deverão submeter-se a parecer prévio da área técnica competente e apreciação e autorização pela Diretoria Colegiada da ANVISA. (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
3.1. A importação de que trata este item deverá ser subsidiada por relatório técnico justificando a indicação terapêutica ou diagnóstica, assinado pelo profissional responsável;
3.1. A importação de que trata este item deverá ser subsidiada por relatório técnico-científico contendo justificativa da necessidade da importação; evidência técnico-científica baseada em compêndios oficiais que comprovem eficácia e segurança do medicamento; e comprovante de registro do medicamento no país de origem ou no país em que é comercializado. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
3.1.1. Excluir-se-á do disposto no subitem anterior a importação destinada à instituição publica integrante do Sistema Único de Saúde que deverá apresentar declaração justificando a importação assinada pelo Responsável ou Representante Legal. (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
3.2. A importação de que trata este item dar-se-á em conformidade com o disposto no Capítulo XXXIX deste Regulamento. (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
4. Será proibido qualquer ato de comércio dos produtos de que trata este Capítulo. (Revogado pela Resolução – RDC nº 383, de 12 de maio de 2020)
CAPÍTULO X
DOAÇÃO INTERNACIONAL DESTINADA A INSTITUIÇÕES FILANTRÓPICAS HABILITADAS
SEÇÃO I
DAS DISPOSIÇÕES GERAIS
1. A doação internacional de que trata este Capítulo relacionado à importação de bens ou produtos pertencentes às classes de medicamentos, alimentos, perfumes, cosméticos, produtos de higiene pessoal, saneantes, produtos para diagnóstico in vitro, produtos médicos, peças de vestuário usadas e artefatos de materiais têxteis e sintéticos, usados, destinada à pessoa jurídica, de direito público ou privado, deverá submeter-se a parecer favorável da autoridade sanitária competente da ANVISA e atender as exigências estabelecidas na legislação sanitária.
1.1. Somente poderão ser objeto de doação internacional de que tratam este Capítulo os bens ou produtos na forma de produto acabado.
2. A solicitação de parecer da autoridade sanitária competente da ANVISA dar se-á pela pessoa jurídica de direito público ou privado, destinatária da doação, previamente ao embarque do bem ou produto no exterior, conforme Seção I, Capítulo III e Petição para Fiscalização Sanitária disposto no subitem 1.2., Capítulo II deste Regulamento, instruída com a documentação disposta no Capítulo XI, junto ao setor técnico competente da Gerencia Geral de Portos, Aeroportos, Fronteiras e Recintos Alfandegados - GGPAF/ ANVISA.
2.1. O deferimento do licenciamento de importação registrado no SISCOMEX e liberação sanitária do bem ou produto, ocorrerão no local de desembaraço aduaneiro do bem ou produto.
2.2. Estará desobrigada de solicitação prévia ao embarque a importação exclusiva de peças de vestuário usadas e artefatos de materiais têxteis e sintéticos, usados.
2.3. Excetua-se das exigências deste item as importações de bens e produtos por doação internacional destinadas a colaborar na avaliação e desenvolvimento de pesquisa, conforme disposto em Regulamento pertinente.
3. A importação de bens ou produtos, de que trata este Capítulo, regularizados junto à ANVISA, por pessoa não detentora de sua regularização, sujeitar-se-á à apresentação de declaração da pessoa jurídica detentora da regularização do produto junto a ANVISA, autorizando a importação.
3.1 A declaração da pessoa jurídica detentora da regularização do produto, junto a ANVISA autorizando a importação, será apresentada em sua forma original e cópia, para sua autenticação, ou previamente autenticada, a qual ficará retida, devendo ainda:
i) estar vinculada a uma única e exclusiva pessoa jurídica, ficando vedado o repasse dessa autorização;
ii) possuir validade jurídica, inclusive não podendo ter prazo de vigência superior a 90 (noventa) dias contados da sua assinatura;
iii) ser subscrita pelo seu responsável legal ou representante legal, e pelo seu responsável técnico, com reconhecimento de firma em cartório;
iv) expressar o compromisso de observância e cumprimento das normas e procedimentos estabelecidos pela legislação sanitária, bem como de ciência das penalidades as quais ficará sujeito, nos termos da Lei nº 6.437, de 20 de agosto de 1977
4. O não cumprimento das exigências de que trata este Capítulo, no prazo estabelecido pela autoridade sanitária, implicará no impedimento à nacionalização dos bens ou produtos sob doação internacional.
5. Será vedada a importação por meio de doação internacional de bens ou produtos sob vigilância sanitária com a embalagem primária violada ou em estado de "em uso" e de produto médico usado, incluindo roupas para uso hospitalar.
6. A constatação em inspeção física ou análise documental quando da chegada no território nacional de produto em desacordo com as informações prestadas pelo registro de importação e petição de fiscalização e liberação, implicará na adoção de medidas restritivas ou punitivas.
SEÇÃO II
DA LIMPEZA E HIGIENIZAÇÃO DO VESTUÁRIO OU ARTEFATOS DE MATERIAIS TÊXTEIS E SINTÉTICOS
7. As peças de vestuário e artefatos de materiais têxteis e sintéticos, usados, deverão apresentar-se limpas e higienizadas quando de sua chegada ao território nacional.
7.1. A critério da autoridade sanitária poderá ser exigida a realização de procedimentos de higienização, no território nacional em estabelecimento destinado à finalidade proposta, podendo o licenciamento de importação no SISCOMEX ser deferido com ressalva, e a saída do bem ou produto do recinto alfandegado ser autorizada, mediante a sujeição do importador à Termo de Guarda e Responsabilidade.
7.2. A ressalva de que trata o subitem anterior deverá ser registrada no campo referente à situação da Licença de Importação no SISCOMEX com o seguinte texto: "BEM OU PRODUTO SOB EXIGÊNCIA SANITÁRIA. A LIBERAÇÃO À EXPOSIÇÃO OU ENTREGA AO CONSUMO DAR-SE-Á MEDIANTE MANIFESTAÇÃO EXPRESSA DA AUTORIDADE SANITÁRIA".
7.3. O importador dos bens ou produtos deverá apresentar à autoridade sanitária documento expedido por empresa executora de serviços de limpeza e higienização, que comprove sua prestação, contendo a descrição da metodologia empregada, bem como os produtos utilizados.
7.4. A liberação dos bens ou produtos para exposição ou entrega ao consumo humano somente ocorrerá depois de satisfeitas às exigências sanitárias.
CAPÍTULO XI
DOAÇÃO INTERNACIONAL DE BENS E PRODUTOS
Documentação pré-embarque:
1- Petição de Fiscalização e Liberação sanitária pertinente;
2- Licenciamento de Importação, cópia;
3- Guia de Recolhimento da União, conforme previsto em legislação sanitária pertinente.
4- Informação sobre a regularização do produto no Sistema Nacional de Vigilância Sanitária, quando couber;
5- Declaração concedida pelo detentor do documento de regularização do produto na ANVISA, autorizando a terceirização da importação, quando couber;
6- Lista dos bens e produtos importados, quando se tratar de doações pertencentes às classes de medicamentos, produtos médicos, produtos para diagnóstico in vitro e alimentos, devendo ser obrigatoriamente informado, para cada nome comercial, sua respectiva classe, categoria, apresentação, data de vencimento do prazo de validade e o(s) respectivo(s) nº(s) de lote(s).
7- Declaração, assinada e com reconhecimento de firma em cartório, do responsável legal da pessoa jurídica destinatária da importação no SISCOMEX, informando sobre a finalidade de uso e a identificação dos locais de armazenagem e/ou distribuição do bem ou produto importada, no território nacional.
∙ Documentação pós-embarque:
1- Petição de Fiscalização e Liberação sanitária pertinente;
2- Licenciamento de Importação, cópia;
3- Autorização de acesso para inspeção física (IN SRF 206, de 25/09/2002, ou norma técnica que a venha substituir), quando couber;
4- Conhecimento de Carga embarcada (AWB, BL, CTR), original e cópia;
5- Certificado ou documento comprovante de higienização do bem ou produto quando se tratar de vestimentas e roupas de uso pessoal ou de utensílios usados;
6- Termo de Guarda e Responsabilidade, quando couber;
7-Termo de Responsabilidade, assinado e com reconhecimento de firma em cartório, pelo responsável técnico da Pessoa Jurídica, importadora no SISCOMEX, assumindo a responsabilidade por quaisquer danos a saúde dos usuários, decorrentes da utilização dos bens ou produtos importados, no território nacional;
8- Lista dos bens ou produtos importados, quando se tratar de doações pertencentes às classes de medicamentos, produtos médicos, produtos para diagnóstico in vitro e alimentos, devendo ser obrigatoriamente informado, para cada nome comercial, sua respectiva classe, categoria, apresentação, data de vencimento do prazo de validade e o(s) respectivo(s) nº(s) de lote(s).
CAPÍTULO XII
IMPORTAÇÃO POR PESSOA FÍSICA
SEÇÃO I
DAS DISPOSIÇÕES GERAIS
1. A importação de produtos acabados e em embalagem original sob vigilância sanitária, por pessoa física, para consumo pessoal, sujeitar-se-á à manifestação prévia ao desembaraço pela autoridade sanitária.
1.1. Considera-se importação para consumo pessoal a entrada no território nacional dos produtos em quantidade e freqüência compatíveis com duração e finalidade da sua estadia e/ou tratamento, ou desde que não se caracterize comércio ou prestação de serviços a terceiros.
1.2. É vedada a importação de produtos de que trata este item com a embalagem primária e/ou secundária violada e /ou avariada, ou em "estado de uso".
1.3. Exclui-se do disposto do subitem anterior os produtos integrantes de bagagem acompanhada, na qual a pessoa física, viajante, encontra-se fazendo uso.
2. A importação de bens e produtos pertencentes às classes de produtos médicos destinados à prestação de serviços a terceiros dar-se-á obrigatoriamente por meio do SISCOMEX.
3. Considerado o contexto epidemiológico internacional, humano, animal ou vegetal, ou a implementação de programas de saúde pública relacionados ao controle sanitário de bens ou produtos e empresas envolvidas em todas as etapas de produção, distribuição, importação, transporte e armazenagem de bens e produtos sob vigilância sanitária, poderá ser proibida em caráter emergencial e transitório sua importação ou entrada a qualquer título no território nacional por pessoa física.
SEÇÃO II
DA IMPORTAÇÃO PARA CONSUMO PESSOAL DE MEDICAMENTOS E ALIMENTOS, DE USO CONTÍNUO OU NUTRICIONAL ESPECIAL, PRODUTOS MÉDICOS E PRODUTOS PARA DIAGNÓSTICO IN VITRO.
4. A importação de bens e produtos pertencentes às classes de medicamentos e alimentos de uso contínuo ou nutricional especial, bem como de produtos para diagnóstico in vitro e produtos médicos, destinadas a consumo pessoal somente será autorizada mediante a apresentação perante a autoridade sanitária de prescrição do profissional pertinente, o qual ficará retida, se atendidas às seguintes condições:
a) estar escrita em vernáculo oficial, ou, se em outro idioma, poderá ser solicitada a tradução assinada por signatário devidamente identificado através do nome, endereço e número do Cadastro de Pessoa Física - CPF.
b) conter informações referentes ao nome e domicílio do paciente, posologia ou modo de uso do bem ou produto, com indicação da periodicidade do tratamento e limitado no máximo a 180 dias, quando se tratar de uso contínuo;
c) conter a data e assinatura do profissional, seu domicílio ou endereço profissional.
4.1. O receituário quando expedido por profissional com exercício laboral brasileiro deverá conter ainda informações referentes ao número de inscrição no Conselho Profissional.
4.2. Inclui-se no disposto neste Capítulo a importação de medicamentos sujeitos a controle especial, a base de substâncias das listas "C1" e "C4" de que trata a Portaria SVS/MS nº 344, de 1998 e suas atualizações, deverá estar acompanhada de receita médica e de documento fiscal comprobatório da sua aquisição, em quantidade para consumo individual e nas condições previstas nas alíneas do item 4.
4.2.2. A modalidade de trânsito de passagem, bagagem acompanhada, está desobrigada de apresentação de comprovante de aquisição.
4.3. A importação de produtos para consumo pessoal deverá ser compatível com a receita, inclusive quanto à apresentação do produto prescrito.
SEÇÃO III
DA IMPORTAÇÃO PARA CONSUMO PESSOAL DE COSMÉTICOS, PRODUTOS DE HIGIENE PESSOAL, PERFUMES, SANEANTES E ALIMENTOS.
5. A importação de produtos pertencentes às classes de cosméticos, produtos de higiene pessoal, perfumes, saneantes e alimentos destinadas a consumo pessoal somente será efetivada mediante inspeção física a critério da autoridade sanitária e atendidas as seguintes condições:
a) apresentar-se em conformidade com o disposto nas alíneas b, c e d, item 1, Capítulo V;
b) em compatibilidade com as circunstâncias da viagem e/ou em quantidade, natureza ou variedade que não permitam presumir importação com fins comerciais ou industriais.
SEÇÃO IV
DA IMPORTAÇÃO DE PRODUTOS MÉDICOS PARA PRESTAÇÃO DE SERVIÇOS A TERCEIROS
6. A importação por pessoa física, de produtos médicos destinados à prestação de serviços, no estágio de produto acabado, dar-se-á obrigatoriamente por meio do SISCOMEX e Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2 do Capítulo II, deste Regulamento, devidamente preenchido;
6.1 Adicionalmente deverão ser apresentados os seguintes documentos: a) declaração firmada pelo importador, contendo:
i) número da inscrição no Conselho de Classe Profissional;
ii) endereço do local de instalação ou guarda do produto;
iii) especificações do produto, como nome comercial, complemento do nome, seu código identificador e do fabricante, nome do detentor da sua regularização perante a ANVISA e respectivo número de registro de regularização;
iv) compromisso de responsabilidade administrativa, civil e penal por danos diretos ou indiretos a saúde individual, coletiva e pública decorrentes do uso do bem e produto;
v) compromisso de não comercialização do produto.
b) licença do estabelecimento, ou alvará sanitário, ou documento oficial correspondente expedido pela autoridade competente, do local onde o produto será instalado ou guardado, quando do seu não uso que deverá ser apresentado na sua forma original e cópia, para autenticação, a qual ficará retida.
7. Na importação de bens e produtos sob registro, cadastro ou autorização de modelo na ANVISA, deverá ser apresentada declaração da pessoa jurídica detentora do documento de regularização do produto junto a ANVISA autorizando a importação.
7.1. A declaração de que trata o item anterior deverá ser apresentada na sua forma original e cópia, para sua autenticação, ou previamente autenticada, a qual ficará retida, devendo ainda:
a) estar vinculada a uma única e exclusiva pessoa jurídica, ficando vedado o repasse dessa autorização;
b) ser subscrita pelo seu responsável legal ou representante legal, e pelo seu responsável técnico, com reconhecimento de firma em cartório;
8. A Importação de que trata esta Seção de bens e produtos sob registro, cadastro ou autorização de modelo na ANVISA, será autorizada e deferida pela autoridade sanitária em exercício no local de desembaraço aduaneiro mediante o cumprimento do disposto no item 7 e fiscalização sanitária satisfatória.
9. Será proibida a alteração de finalidade da importação e comercialização dos bens e produtos de que trata este Capítulo.
Capítulo XII
Importação por Pessoa Física
(Redação dada pela Resolução - RDC nº 28, de 28 de junho de 2011)
1. Fica dispensada de autorização pela autoridade sanitária, no local de entrada ou desembaraço aduaneiro, a importação de produtos acabados pertencentes às classes de medicamentos, produtos para saúde, alimentos, saneantes, cosméticos, produtos de higiene pessoal e perfumes, realizadas por pessoa física e destinadas a uso próprio.
(Redação dada pela Resolução - RDC nº 28, de 28 de junho de 2011)
1.1 Incluem-se no disposto neste item, os bens e produtos integrantes de bagagem acompanhada ou desacompanhada de viajante procedente do exterior. (Redação dada pela Resolução - RDC nº 28, de 28 de junho de 2011)
1.2 Considera-se para uso próprio a importação de produtos em quantidade e freqüência compatíveis com a duração e a finalidade de tratamento, ou que não caracterize comércio ou prestação de serviços a terceiros. (Redação dada pela Resolução - RDC nº 28, de 28 de junho de 2011)
1.3 Excetua-se do disposto neste item a importação de medicamentos à base de substâncias constantes na Portaria SVS/MS nº 344, de 12 de maio de 1998, e suas atualizações, que deverá obedecer ao disposto na Resolução de Diretoria Colegiada - RDC n° 63, de 9 de setembro de 2008, e suas atualizações, e ainda os medicamentos com restrições de uso descritas em regulamento específico. (Redação dada pela Resolução - RDC nº 28, de 28 de junho de 2011)
2. A importação por pessoa física de produtos para saúde destinados à prestação de serviços a terceiros, será realizada exclusivamente por SISCOMEX e deverá atender às exigências previstas nos procedimentos correspondentes de importação previstos no Capítulo XXXIX da Resolução de Diretoria Colegiada - RDC n° 81, de 5 de novembro de 2008. (Redação dada pela Resolução - RDC nº 28, de 28 de junho de 2011)
3. Será vedada a entrada no território nacional de: (Redação dada pela Resolução - RDC nº 28, de 28 de junho de 2011)
3.1. células e tecidos destinados a fins terapêuticos não autorizados pela área técnica competente da ANVISA; e (Redação dada pela Resolução - RDC nº 28, de 28 de junho de 2011)
3.2. produtos desprovidos de identificação em suas embalagens primária e/ou secundária originais, importados por remessa expressa, postal ou encomenda aérea internacional. (NR) (Redação dada pela Resolução - RDC nº 28, de 28 de junho de 2011)
CAPÍTULO XIII
REQUERIMENTO DE RECONHECIMENTO DE FINALIDADE PARA ISENÇÃO DE IMPOSTO DE IMPORTAÇÃO PARA MATERIAL MÉDICO HOSPITALAR
1. Para fins de caracterizar a compatibilidade da natureza, qualidade e quantidade do bem ou produto às finalidades essenciais do importador para isenção do imposto de importação, nos termos do Decreto nº 4.543, de 2002, caberá ao importador submeter requerimento à autoridade sanitária competente da sede da ANVISA.
1.1. O requerimento de que trata este item deverá ser preenchido conforme Petição de Reconhecimento de Finalidade para Isenção de Imposto de Importação, de acordo que trata o subitem 1.2 do Capítulo II, deste Regulamento, e deverá ser instruído pela documentação descrita pelo Capítulo XIV, deste Regulamento.
1.2. Considerar-se-á material médico-hospitalar para os fins deste Capítulo, os bens ou produtos sob vigilância sanitária, destinados à prevenção, diagnóstico, tratamento e reabilitação da saúde humana, individual ou coletiva.
2. A importação de bens ou produtos de que trata este Capítulo por pessoa não detentora de sua regularização junto à ANVISA, sujeitar-se-á a apresentação de autorização da pessoa jurídica detentora da regularização do bem ou produto junto a ANVISA, para cada importação.
2.1 A declaração da pessoa jurídica detentora da regularização do produto, junto a ANVISA autorizando a importação, será apresentada na sua forma original e cópia, para sua autenticação, ou previamente autenticada, a qual ficará retida, devendo ainda:
i) estar vinculada a uma única e exclusiva pessoa jurídica, ficando vedado o repasse dessa autorização;
ii) possuir validade jurídica, inclusive não podendo ter prazo de vigência superior a 90 (noventa) dias contados da sua assinatura;
iii) ser subscrita pelo seu responsável legal ou representante legal, e pelo seu responsável técnico, com reconhecimento de firma em cartório;
iv) expressar o compromisso de observância e cumprimento das normas e procedimentos estabelecidos pela legislação sanitária, bem como de ciência das penalidades as quais ficará sujeito, nos termos da Lei nº 6.437, de 20 de agosto de 1977.
3. Quando do exame do requerimento, poderá a autoridade sanitária solicitar exigências ao importador por prazo determinado para cumprimento.
3.1. O não cumprimento das exigências de que trata este item, no prazo estabelecido, implicará ao importador no indeferimento do requerimento de isenção de imposto de importação.
4. Caberá ao importador requerente após manifestação favorável da ANVISA para isenção do imposto, a obrigação de cumprir e fazer cumprir a finalidade declarada do bem ou produto, quando da sua utilização ou exposição no território nacional.
CAPÍTULO XIV
DOCUMENTAÇÃO DE INSTRUÇÃO DO REQUERIMENTO DE RECONHECIMENTO DE FINALIDADE PARA ISENÇÃO DE IMPOSTO DE IMPORTAÇÃO
1. Petição de Fiscalização e Liberação Sanitária de Bens e Produtos Importados - ANVISA;
2. Requerimento de reconhecimento de finalidade para Isenção de Imposto de Importação para material Médico-Hospitalar nos termos deste Regulamento;
3. Guia de Recolhimento da União da Secretaria do Tesouro Nacional, conforme previsto em legislação sanitária pertinente;
4. Extrato de Licenciamento de Importação ou Licenciamento Simplificado de Importação, atualizado (cópia);
5. Informação sobre a regularização do produto na ANVISA, quando couber;
6. Declaração concedida pelo detentor do documento de regularização do produto na ANVISA, autorizando importação por terceiros, quando couber;
7. Declaração assinada pelo representante legal da Empresa, assumido o compromisso de que o bem ou produto importado será de uso exclusivo da instituição importadora, indicando o(s) local(is) de instalação, uso ou consumo do bem ou produto, no que couber;
8. Instrumento de procuração do importador com delegação de poderes perante a ANVISA, no que couber:
a) peticionamento de fiscalização e liberação sanitária;
b) acompanhamento das etapas de análise técnica para fins de concessão do ofício de reconhecimento de finalidade para isenção de imposto de importação;
c) documento subscrito pelo representante legal do interessado com relação nominal dos funcionários legalmente habilitados à execução dos poderes delegados no instrumento de procuração de que trata a alínea anterior.
d) cientificação de termos legais e outros documentos relacionados; e) apresentação dos meios de defesa, como interposição de recursos.
9. Especificar o nome e o endereço completo do recinto alfandegado onde ocorrerá o desembaraço aduaneiro.
CAPÍTULO XV
ROTULAGEM DE BEM OU PRODUTO IMPORTADO - PRODUTO ACABADO
1. Será permitida a rotulagem no território nacional, de acordo com a legislação pertinente de produtos importados regularizados formalmente junto ao Sistema Nacional de Vigilância Sanitária.
1.1. Será vedada a entrega ao consumo de produtos importados com identificação ou rotulagem em idioma estrangeiro, exceto as importações com fins não comerciais de que tratam os Capítulos IX, X, XII, XIX, XX e XXI deste Regulamento.
1.2. Os produtos de que trata este item quando expostos ou entregues ao consumo, deverão apresentar-se rotulados, lacrados ou sob selo de segurança, quando exigido em legislação sanitária pertinente, e com as informações aprovadas pela autoridade sanitária competente, quando de sua regularização no Sistema Nacional de Vigilância Sanitária.
1.3. A faculdade de que trata este item não eximirá o importador de apresentar no rótulo em idioma estrangeiro de sua embalagem, primária e/ou secundária, as seguintes informações quando de sua entrada no território nacional:
a) nome comercial, em uso no exterior;
b) nome do fabricante e local de fabricação;
c) número ou código do lote ou partida;
d) data de fabricação, quando exigida em legislação sanitária pertinente; e) data de validade ou data do vencimento, quando couber.
1.4. Para os fins do disposto no item anterior, poderá ser requerido pela autoridade sanitária a apresentação da respectiva tradução do rótulo do bem ou produto importado, subscrita pelo responsável técnico e pelo responsável ou representante legal da empresa detentora da regularização do produto junto ao Sistema Nacional de Vigilância Sanitária.
1.4.1 Nos casos de alimentos a tradução do rótulo poderá ser subscrita pelo responsável ou representante legal da empresa importadora.
1.5. No caso da ausência da informação de que trata o subitem 1.3, alínea "d", no rótulo de bens e produtos pertencentes às classes de cosméticos, perfumes e produtos de higiene pessoal, ficará o importador obrigado a apresentar à autoridade sanitária em exercício no local de desembaraço do bem ou produto no território nacional, declaração firmada pelo responsável técnico da empresa importadora, informando a data de fabricação do lote ou partida para cada produto importado.
1.6. No caso de importação de bens e produtos pertencentes às classes de cosméticos, e produtos de higiene pessoal, ficará o importador desobrigado de atender ao disposto no subitem 1.3, alínea "e".
1.7. No caso da ausência, no rótulo em idioma estrangeiro de produto importado pertencente à classe de produtos para diagnóstico in vitro, da informação de que trata do subitem 1.3, alínea "d", ficará o importador obrigado a apresentar à autoridade sanitária em exercício no local de desembaraço no território nacional, declaração firmada pelo responsável técnico da empresa importadora informando a data de fabricação do lote ou partida para cada produto importado ou laudo analítico de controle da qualidade, por lote ou partida para cada produto importado, subscrito pelo responsável técnico da empresa importadora, constando informação referente à data de fabricação.
2. A importação de produto apresentando rótulo em idioma português em desacordo com o previsto na legislação sanitária poderá ter o deferimento do licenciamento de importação no SISCOMEX com ressalva, e sua saída da área alfandegada autorizada, mediante sujeição do importador à Termo de Guarda e Responsabilidade.
2.1. A ressalva de que trata este item deverá ser registrada no campo referente à situação da Licença de Importação no SISCOMEX com o seguinte texto: "PRODUTO SOB EXIGÊNCIA SANITÁRIA. A LIBERAÇÃO À INDUSTRIALIZAÇÃO, EXPOSIÇÃO À VENDA OU ENTREGA AO CONSUMO DAR-SE-Á MEDIANTE MANIFESTAÇÃO EXPRESSA DA AUTORIDADE SANITÁRIA".
CAPÍTULO XV
ROTULAGEM DE BEM OU PRODUTO IMPORTADO - PRODUTO ACABADO
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1. Será permitida a rotulagem de produtos importados, em território nacional, observada a legislação pertinente. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1.1. Será vedada a entrega ao consumo de produtos importados com identificação ou rotulagem em idioma estrangeiro, exceto as importações com fins não comerciais de que tratam os Capítulos IX, X, XII, XIX, XX e XXI desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1.2. Os produtos de que trata este item, quando expostos ou entregues ao consumo, deverão apresentar-se rotulados conforme legislação sanitária pertinente à classe do produto. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2. A embalagem primária ou secundária ou de transporte deverá conter as seguintes informações mínimas quando de sua entrada no território nacional, conforme classe de produto à qual pertence: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.1 Alimentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Nome comercial em uso no exterior; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Nome do fabricante e local de fabricação; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Número do lote; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Data de validade. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.2 Cosméticos / Perfumes/ Produtos de Higiene: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Nome comercial em uso no exterior; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) País de fabricação; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) número ou código do lote. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.3 Saneantes: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Nome comercial em uso no exterior; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Nome do fabricante e local de fabricação; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Número do lote; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Data de validade. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.4 Produtos para Saúde: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Nome comercial em uso no exterior; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Nome do fabricante e local de fabricação; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Número ou código do lote ou part number; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Data de fabricação; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e) Data de validade. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.5 Produtos para diagnóstico in vitro: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Nome comercial em uso no exterior; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Nome do fabricante e local de fabricação; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Número ou código do lote ou part number; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Data de fabricação; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e) Data de validade. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.6 Medicamentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Nome comercial; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Nome do fabricante e Local de fabricação; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) número ou código do lote ou partida; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) data de fabricação; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e) data de validade (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3. Para os fins do disposto no item 2 deste Capítulo, poderá ser requerida pela autoridade sanitária a apresentação da respectiva tradução do rótulo do bem ou produto importado, subscrita pelo responsável técnico e pelo responsável ou representante legal da empresa detentora da regularização do produto junto ao Sistema Nacional de Vigilância Sanitária. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3.1. Nos casos de alimentos, a tradução do rótulo poderá ser subscrita pelo responsável ou representante legal da empresa importadora. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
4. No caso da ausência, no rótulo em idioma estrangeiro de produto importado pertencente à classe de produtos para diagnóstico in vitro, da informação de que trata o subitem 2.5, alínea “d” deste Capítulo, ficará o importador obrigado a apresentar declaração firmada pelo responsável técnico da empresa importadora, informando a data de fabricação do lote ou partida, para cada produto importado; ou laudo analítico de controle da qualidade, por lote ou partida, para cada produto importado, constando informação referente à data de fabricação. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5. A importação de produto com rótulo em idioma português em desacordo com o previsto na legislação sanitária poderá resultar em deferimento, com ressalva, do licenciamento de importação no SISCOMEX, bem como em saída da área alfandegada autorizada, mediante sujeição do importador a Termo de Guarda e Responsabilidade.
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5.1. A ressalva de que trata o item 5 deste Capítulo deverá ser registrada no campo referente à situação da Licença de Importação no SISCOMEX com o seguinte
texto: “PRODUTO SOB EXIGÊNCIA SANITÁRIA. A LIBERAÇÃO À INDUSTRIALIZAÇÃO, EXPOSIÇÃO À VENDA OU ENTREGA AO CONSUMO DAR-SE-Á MEDIANTE MANIFESTAÇÃO EXPRESSA DA AUTORIDADE SANITÁRIA”. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
CAPÍTULO XVI
PRODUTO EM ESTÁGIO INTERMEDIÁRIO DE PROCESSO DE PRODUÇÃO SEÇÃO I
DOS MEDICAMENTOS
1. Os produtos pertencentes à classe de medicamentos, em estágios intermediários de seu processo de produção ou fabricação, etapas de produto semi elaborado e a granel, desprovido de embalagem primária, deverão ser submetidos ao departamento técnico da empresa importadora, instalado no território nacional, para ensaios laboratoriais necessários à comprovação de sua natureza, identidade e qualidade nesses estágios de produção ou fabricação.
1.1. A importação desses produtos dar-se-á obrigatoriamente por meio do SISCOMEX - Módulo Importação.
1.2. Será permitida nos termos do Capítulo VI deste Regulamento, a terceirização da importação dos produtos de que trata esta Seção.
1.2.1 O controle da qualidade dos produtos de que trata este item poderá ser efetivada por institutos ou laboratórios oficiais, por meio de convênios ou contratos.
1.3. Exclui-se das exigências previstas neste Regulamento a apresentação de ensaios laboratoriais necessários à comprovação de sua natureza, identidade e qualidade nesses estágios de produção ou fabricação, as importações de medicamentos para fins de pesquisa clínica no território nacional.
2. A importação de que trata esta Seção somente se efetivará mediante deferimento de Licenciamento de Importação junto ao SISCOMEX com ressalva, e sua saída da área alfandegada autorizada por meio de sujeição à Termo de Guarda e Responsabilidade, por lote, registrada no campo referente ao texto da situação do licenciamento de importação: "PRODUTO SOB EXIGÊNCIA SANITÁRIA. A LIBERAÇÃO À INDUSTRIALIZAÇÃO, EXPOSIÇÃO À VENDA OU ENTREGA AO CONSUMO DAR-SE-Á MEDIANTE MANIFESTAÇÃO EXPRESSA DA AUTORIDADE SANITÁRIA". (Exigência suspensa pela Resolução - RDC nº 48, de 31 de agosto de 2012)
2.1. Constituir-se-á exigência sanitária de que trata este item, entre outras, a obrigatoriedade de apresentação de laudo analítico de controle da qualidade completo com ensaios conforme a metodologia analítica dos produtos pertencentes à classe de medicamentos, em estágios intermediários de seu processo de produção ou fabricação, etapas de produto semi-elaborado e a granel desprovidos de embalagem primária. (Exigência suspensa pela Resolução - RDC nº 48, de 31 de agosto de 2012)
2.2. O Termo de Guarda e Responsabilidade de que trata este item, no caso de importação terceirizada, deverá ser submetido à autoridade sanitária em exercício no recinto alfandegado pela empresa detentora do registro do medicamento na ANVISA, assinado pelo Representante Legal e Responsável Técnico. (Exigência suspensa pela Resolução - RDC nº 48, de 31 de agosto de 2012)
2.2.1. Ficará autorizada na forma deste item a retirada de amostra dos produtos importados sob Termo de Guarda e Responsabilidade de que trata esta Seção. (Exigência suspensa pela Resolução - RDC nº 48, de 31 de agosto de 2012)
2.2.2. A retirada de que trata este subitem limitar-se-á às quantidades necessárias e finalidade exclusiva para a análise laboratorial ou elaboração do Laudo de Controle da Qualidade. (Exigência suspensa pela Resolução - RDC nº 48, de 31 de agosto de 2012)
2.2.3. Ficará a empresa detentora do registro do produto, inclusive na importação terceirizada, obrigada a manter arquivadas as informações referentes às unidades dos produtos retiradas para fins de análise laboratorial e elaboração do Laudo de Controle da Qualidade, que deve conter o registro dessas unidades. (Exigência suspensa pela Resolução - RDC nº 48, de 31 de agosto de 2012)
3. A liberação do produto sob Termo de Guarda e Responsabilidade, dar-se-á pela autoridade sanitária, em exercício no local de seu desembaraço, mediante a satisfação das exigências sanitárias por intermédio da análise técnica satisfatória do laudo laboratorial conclusivo apresentado pelo importador. (Exigência suspensa pela Resolução - RDC nº 48, de 31 de agosto de 2012)
3.1. Para os fins da análise técnica de que trata este item, a empresa detentora do documento de regularização do produto junto a ANVISA deverá apresentar no laudo analítico de controle da qualidade realizado em território nacional, os tipos de ensaios e resultados analíticos compatíveis àqueles informados pelo fabricante e deverá ser subscrita pelo responsável técnico da empresa. (Exigência suspensa pela Resolução - RDC nº 48, de 31 de agosto de 2012)
SEÇÃO II
DOS ALIMENTOS, COSMÉTICOS, PERFUMES, PRODUTOS DE HIGIENE PESSOAL, SANEANTES, PRODUTOS MÉDICOS E PRODUTOS PARA DIAGNÓSTICO IN VITRO
4. Os produtos pertencentes às classes de alimentos, perfumes, cosméticos, produtos de higiene, saneantes, produtos para diagnóstico in vitro, produtos médicos, em estágio intermediário de seu processo de produção ou de fabricação, etapas de produto semi elaborado e a granel, deverão ser submetidos ao departamento técnico da empresa importadora instalada no território nacional, para ensaios laboratoriais, necessários à comprovação da sua natureza, identidade e qualidade.
4.1. O controle da qualidade dos bens ou produtos de que trata esta Seção poderá ser efetivada por institutos ou laboratórios oficiais, por meio de convênios ou contratos.
5. À autoridade sanitária competente, federal, estadual ou municipal, caberá o exercício da fiscalização sanitária originária, complementar ou concorrente de que trata esta Seção, de modo a garantir manutenção de sua natureza, identidade e qualidade quando da exposição ou consumo.
CAPÍTULO XVII
LAUDO ANALÍTICO DE CONTROLE DE QUALIDADE COM IRREGULARIDADE
1. A importação de produtos sob a forma de matéria-prima, produto semi elaborado, produto a granel ou produto acabado, cujo Laudo Analítico de Controle da Qualidade por lote ou partida exigido neste Regulamento, apresentar resultado analítico insatisfatório, parcial ou total, ou com registros de informações em desacordo com a documentação apresentada, não terá sua liberação sanitária autorizada.
1.1. A não liberação sanitária aplicar-se-á à importação nas demais modalidades previstas no Capítulo III deste Regulamento, sujeitando os produtos à interdição no recinto alfandegado.
CAPÍTULO XVIII
PRODUTOS MÉDICOS RECONDICIONADOS OU USADOS E FONTES RADIOATIVAS SELADAS
SEÇÃO I
DAS DISPOSIÇÕES GERAIS
1. A importação por empresas de bens ou produtos pertencentes às classes de produtos médicos, usados e recondicionados, componentes e acessórios, deverá atender o disposto em legislação sanitária pertinente.
SEÇÃO II
PRODUTOS MÉDICOS RECONDICIONADOS
2. A importação de produtos médicos recondicionados dar-se-á obrigatoriamente por meio do SISCOMEX, e atenderá as formalidades de requerimento e tramitação de acordo com o Procedimento nº 4.1, do Capítulo XXXIX, deste Regulamento e legislação sanitária pertinente.
3. A importação de produtos médicos recondicionados por empresa não detentora da regularização perante ANVISA sujeitar-se-á a apresentação de declaração da pessoa jurídica detentora da regularização do bem ou produto junto a ANVISA, autorizando a importação.
3.1 A declaração da pessoa jurídica detentora da regularização do produto, junto a ANVISA autorizando a importação, será apresentada na sua forma original e cópia, para sua autenticação, ou previamente autenticada, a qual ficará retida, devendo ainda:
i) estar vinculada a uma única e exclusiva pessoa jurídica, ficando vedado o repasse dessa autorização;
ii) possuir validade jurídica, inclusive não podendo ter prazo de vigência superior a 90 (noventa) dias contados da sua assinatura;
iii) ser subscrita pelo seu responsável legal ou representante legal, e pelo seu responsável técnico, com reconhecimento de firma em cartório;
iv) expressar o compromisso de observância e cumprimento das normas e procedimentos estabelecidos pela legislação sanitária, bem como de ciência das penalidades as quais ficará sujeito, nos termos da Lei nº 6.437, de 20 de agosto de 1977.
SEÇÃO III
PRODUTOS MÉDICOS USADOS
4. Será vedada a importação de produtos médicos usados.
4.1. A autorização para a importação pela empresa detentora de seu registro na ANVISA de produto médico usado para fins de recondicionamento no território nacional dar-se-á a partir de parecer conclusivo e satisfatório da área técnica competente da ANVISA em sua sede.
SEÇÃO IV
FONTES RADIOATIVAS SELADAS PARA USO EM SERVIÇOS DE SAÚDE
5. O importador de fontes radioativas seladas de que trata este Capítulo, além das exigências previstas no Procedimento 4.1 do Capítulo XXXIX deste Regulamento, deverá apresentar no intervalo de 60 (sessenta) dias após o deferimento do licenciamento de importação pela autoridade sanitária, declaração assinada pelo responsável legal e pelo responsável técnico, na sua forma original e cópia, para autenticação ou previamente autenticada, a qual ficará retida.
5.1. Em atendimento ao disposto nesta Seção ficam definidas as NCM sujeitas ao controle sanitário de importação complementar:
a) Código da NCM: 2844.40.20,
a.1) Descrição: Cobalto 60;
b) Código da NCM: 2844.40.90,
b.1) Descrição: Outros;
b.2) Descrição do Destaque - NCM: Rádio (Ra-226), Césio (Cs 137), Iodo (I 125), Ouro (Au-198), Estrôncio (Sr-90), Irídio (Ir-192) e demais fontes seladas para uso em serviços de saúde;
c) Código da NCM: 9022.2
c.1) Descrição: Aparelhos que utilizem radiações alfa, beta ou gama, mesmo para usos médicos, cirúrgicos, odontológicos ou veterinários, incluídos os aparelhos de radiofotografia ou radioterapia.
5.2. São informações que deverão constar da declaração de que trata este item: a) especificações da fonte: radionuclídeo, quantidade e forma;
b) finalidade do uso da fonte;
c) atividade do radionuclídeo: valor e data da medição.
d) destino da fonte: Nome da instituição, número do CNES, endereço completo do local onde se encontra instalada.
5.3. A autoridade sanitária em exercício no local onde ocorrerá o desembaraço aduaneiro deverá lavrar Termo legal de Notificação ao importador e/ou disponibilizar no Siscomex informações orientando-o para o cumprimento das exigências de que trata este item, no tocante às importações de que tratam esta Seção.
5.4. As Coordenações de Vigilância Sanitária de Portos, Aeroportos, Fronteiras e Recintos Alfandegados nos Estados e Distrito Federal deverão encaminhar à Gerência Geral de Portos, Aeroportos, Fronteiras e Recintos Alfandegados, relatório bimestral, por empresa importadora, contendo as informações apresentadas. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
CAPÍTULO XVIII
PRODUTOS MÉDICOS RECONDICIONADOS OU USADOS E FONTES RADIOATIVAS SELADAS
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) SEÇÃO I
DAS DISPOSIÇÕES GERAIS
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1. A importação, por empresas, de bens ou produtos pertencentes às classes de produtos médicos, usados e recondicionados, componentes e acessórios, deverá atender o disposto em legislação sanitária pertinente. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO II
PRODUTOS MÉDICOS RECONDICIONADOS
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2. A importação de produtos médicos recondicionados dar-se-á obrigatoriamente por meio do SISCOMEX, e atenderá as formalidades de requerimento e tramitação, de acordo com o Procedimento 4, do Capítulo XXXIX desta Resolução e legislação sanitária pertinente. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3. A importação de produtos médicos recondicionados, por empresa não detentora da regularização perante ANVISA, dependerá da apresentação de declaração da pessoa jurídica detentora da regularização do bem ou produto junto à ANVISA, autorizando a importação, devendo: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) estar vinculada a uma única e exclusiva pessoa jurídica, ficando vedado o repasse dessa autorização; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) possuir validade jurídica, inclusive não podendo ter prazo de vigência superior a 90 (noventa) dias contados da sua assinatura; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) ser subscrita pelo seu responsável legal ou representante legal, e pelo seu responsável técnico; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) expressar o compromisso de observância e cumprimento das normas e procedimentos estabelecidos pela legislação sanitária, bem como de ciência das penalidades às quais ficará sujeito, nos termos da Lei n. º 6.437, de 20 de agosto de 1977. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO III
PRODUTOS MÉDICOS USADOS
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
4. É vedada a importação de produtos médicos usados. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
4.1. A autorização para a importação, pela empresa detentora do respectivo registro na ANVISA, de produto médico usado, para fins de recondicionamento no território nacional, dar-se-á a partir de parecer conclusivo e satisfatório da área técnica competente da ANVISA em sua sede. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO IV
FONTES RADIOATIVAS SELADAS PARA USO EM SERVIÇOS DE SAÚDE (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5. O importador das fontes radioativas seladas de que trata este Capítulo, além das exigências previstas no Procedimento 4 do Capítulo XXXIX desta Resolução, deverá apresentar, no prazo de 60 (sessenta) dias contados do deferimento, pela autoridade sanitária, do licenciamento de importação, declaração, assinada pelo responsável legal e pelo responsável técnico, que contenha as seguintes informações:
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) especificações da fonte: radionuclídeo, quantidade e forma; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) finalidade do uso da fonte; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) atividade do radionuclídeo: valor e data da medição; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) destino da fonte: nome da instituição, número do CNES, endereço completo do local onde se encontra instalada. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5.1. A autoridade sanitária deverá lavrar termo legal de Notificação ao importador e/ou disponibilizar no Siscomex informações orientando-o para o cumprimento das exigências de que trata o item 5 desta Seção. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
6. Em atendimento ao disposto nesta Seção ficam definidas as NCMs sujeitas ao controle sanitário de importação complementar: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Código da NCM: 2844.40.20, (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a.1) Descrição: Cobalto 60; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Código da NCM: 2844.40.90, (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b.1) Descrição: Outros; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b.2) Descrição do Destaque - NCM: Rádio (Ra-226), Césio (Cs 137), Iodo (I 125), Ouro (Au-198), Estrôncio (Sr-90), Irídio (Ir-192) e demais fontes seladas para uso em serviços de saúde; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Código da NCM: 9022.2, (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c.1) Descrição: Aparelhos que utilizem radiações alfa, beta ou gama, mesmo para usos médicos, cirúrgicos, odontológicos ou veterinários, incluídos os aparelhos de radiofotografia ou radioterapia. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
CAPÍTULO XIX
IMPORTAÇÃO DE MATERIAIS PARA PESQUISA CIENTÍFICA DE INTERESSE SANITÁRIO
(Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017) SEÇÃO I
DAS DISPOSIÇÕES GERAIS
(Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
1. A importação de material sob vigilância sanitária destinada à pesquisa científica de interesse sanitário, por pesquisador ou entidade de pesquisa não credenciado pelo CNPq, deverá submeter-se à manifestação expressa e favorável da autoridade sanitária competente da ANVISA, previamente ao seu desembaraço, no território nacional. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
1.1. A importação de que trata este Capítulo deverá ser requerida por meio de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, item 1.2, e instruída conforme o Termo de Responsabilidade pertinente. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
2. Constituir-se-ão exigências sanitárias obrigatórias para deferimento e liberação sanitária de materiais de que trata este Capítulo o atendimento quanto aos padrões de embalagem, transporte e armazenagem informados, no que couber, pelo seu fabricante ou fornecedor e pela legislação sanitária pertinente. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
3. A importação de materiais por pessoa física vinculada à instituição de ensino e pesquisa, não credenciadas no CNPq, deverá atender o disposto neste Capítulo. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
4. A importação de amostras biológicas ou ambientais destinadas a diagnóstico laboratorial epidemiológico ou ambiental em laboratórios integrantes do Sistema Nacional de Laboratórios de Saúde Pública ou à avaliação e desenvolvimento de Programa Nacional de Saúde Pública, dar-se-á mediante aprovação prévia, ao embarque no exterior, do órgão competente do Ministério da Saúde. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
5 O material importado por pessoa física ou jurídica destinatária direta da pesquisa dar-se-á por meio do SISCOMEX, remessa expressa, remessa postal ou Declaração Simplificada de Importação - DSI não eletrônica, mediante a sujeição prévia ao desembaraço aduaneiro de fiscalização sanitária, pela autoridade sanitária competente da ANVISA. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
5.1. A importação de que trata este item eximir-se-á da obrigação prévia de autorização de embarque no exterior, salvo quando constar dos Procedimentos nº 1, nº 1-A, e nº 3, do Capítulo XXXIX deste Regulamento, devendo ser importada obrigatoriamente por meio do SISCOMEX. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
SEÇÃO II
DO MATERIAL OBJETO DA PESQUISA CIENTIFICA DE INTERESSE SANITÁRIO
(Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
6. A importação de que trata esta Seção dar-se-á além do disposto no item 1.1. deste Capítulo, da apresentação do Termo de Responsabilidade constante do Capítulo XIX-A, deste Regulamento, o qual deverá ser apresentado com firmas reconhecidas em cartório. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
SEÇÃO III
DO MATERIAL, NÃO OBJETO DA PESQUISA CIENTIFICA, IMPORTADA PARA FINS DE ACOMPANHAMENTO, AVALIAÇÃO OU
DESENVOLVIMENTO DE PESQUISA CIENTIFICA DE INTERESSE SANITÁRIO.
(Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
7. A importação de produto sob vigilância sanitária, destinada ao acompanhamento, avaliação ou desenvolvimento de pesquisa científica de interesse sanitário, deverá ocorrer por meio de Licenciamento de Importação no SISCOMEX, mediante a sujeição prévia ao desembaraço aduaneiro de fiscalização sanitária, pela autoridade sanitária competente da ANVISA. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
8. A importação de que trata esta Seção dar-se-á além do disposto no item 1.1. deste Capítulo, da apresentação do Termo de Responsabilidade constante do Capítulo XIX-B, deste Regulamento, o qual deverá ser apresentado com firma reconhecida em cartório. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
Subseção I
Dos Produtos Não Regularizados junto ao Sistema Nacional de Vigilância Sanitária – SNVS
(Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
9. A importação de produtos pertencentes às classes de produtos médicos e produtos para diagnóstico em vitro, não regularizadas na ANVISA, vinculada ao acompanhamento e avaliação do desenvolvimento de pesquisa científica de interesse sanitário, dar-se-á por meio do SISCOMEX, remessa expressa ou remessa postal e deverá submeter-se, a parecer técnico, conclusivo e satisfatório, da área técnica competente da ANVISA em sua sede, referente à autorização da Importação. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
10. Estão isentos do parecer referido no item acima, os produtos para diagnóstico in vitro que não sejam destinados ao diagnóstico em amostras humanas e que sejam utilizados exclusivamente na pesquisa científica. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
10.1. A importação de que trata este item eximir-se-á da obrigação prévia de autorização de embarque no exterior. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
Subseção II
Dos Produtos Regularizados junto ao Sistema Nacional de Vigilância Sanitária – SNVS
(Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
11. A importação de bens e produtos sob vigilância sanitária regularizados junto ao SNVS, destinados à pessoa física ou jurídica vinculada a instituição de pesquisa, para fins de acompanhamento, avaliação e desenvolvimento de pesquisa científica, ocorrerá por meio do SISCOMEX, remessa expressa ou remessa postal, para os produtos que constarem no procedimento 5 (cinco), do Capítulo XXXIX deste Regulamento e mediante a sujeição prévia ao desembaraço aduaneiro de fiscalização sanitária, pela autoridade sanitária competente da ANVISA (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
11.1. Os bens e produtos sob vigilância sanitária constantes dos demais procedimentos, do Capítulo XXXIX deste Regulamento, deveram cumprir o preconizado nos referidos procedimentos. (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
CAPÍTULO XIX-A
TERMO DE RESPONSABILIDADE
IMPORTAÇÃO VINCULADA A PESQUISA CIENTÍFICA DE INTERESSE SANITÁRIO
(Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
1 - A pessoa física/jurídica ______________________________, declara que o(s) produtos(s) abaixo relacionado(s) foi(ram) importado(s), sem fins comerciais ou industriais e destina(m)-se, exclusivamente, para pesquisa científica de interesse sanitário no território nacional, na forma do disposto no Regulamento Técnico de Vigilância Sanitária de Bens e Produtos Importados.
(Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
2 - São informações relacionadas à importação: (Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
a) o título e objeto da pesquisa científica de interesse sanitário; (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
b) o nome e endereço completo da instituição remetente; (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
c) o país de fabricação do material importado; (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
d) o país de origem do material que integra a composição do produto importado; (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
e) o país de procedência do produto importado; (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
f) o prazo de validade do produto importado, quando disponível; (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
g) endereço completo do importador; (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
h) nome e endereço completo da instituição destinatária, (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
i) nome e endereço completo do local onde irá realizar-se a pesquisa; (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
j) número do documento e identificação do órgão oficial competente que regularizou a pesquisa, quando couber; (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
l) nome e respectivo registro no conselho de classe do pesquisador da instituição responsável pela pesquisa; (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
m) licença sanitária ou documento correspondente válido, expedido pela autoridade competente do Estado, Município ou do Distrito Federal, onde se encontra instalado o laboratório analista, quando se tratar de exigência obrigatória constante em legislação pertinente; (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
n) identificação complementar da mercadoria importada, quando couber. (Revogada pela Resolução – RDC nº 172, de 8 de setembro de 2017)
Os abaixo-assinados assumem a responsabilidade sanitária, pelos danos à saúde individual ou coletiva e ao meio ambiente decorrente da alteração da finalidade de ingresso do produto no território nacional.
PROFISSIONAL RESPONSÁVEL PELA PESQUISA REPRESENTANTE LEGAL CR No.
(Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
CAPÍTULO XIX-B
TERMO DE RESPONSABILIDADE
DA IMPORTAÇÃO PARA FINS DE ACOMPANHAMENTO, AVALIAÇÃO E DESENVOLVIMENTO DE PESQUISA CIENTÍFICA DE INTERESSE SANITÁRIO.
(Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
A pessoa física/jurídica __________________________________, declara que o(s) produtos(s) abaixo relacionada(s) foi(ram) importado(s), sem fins comerciais ou industriais e destina(m)-se, exclusivamente, para pesquisa científica de interesse sanitário no território nacional, na forma do disposto no Regulamento Técnico de Vigilância Sanitária de Bens e Produtos Importados.
I
(Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017)
Os abaixo-assinados assumem a responsabilidade sanitária, pelos danos à saúde individual ou coletiva e ao meio ambiente decorrente da alteração da finalidade de ingresso do produto no território nacional.
PROFISSIONAL RESPONSÁVEL PELA PESQUISA REPRESENTANTE LEGAL CR No.
(Revogado pela Resolução – RDC nº 172, de 8 de setembro de 2017) CAPÍTULO XX
PADRÃO DE REFERÊNCIA E MATERIAL DE REFERÊNCIA DE NATUREZA BIOLÓGICA NÃO HUMANA, AMBIENTAL, QUÍMICA E FÍSICA PARA ENSAIO DE PROFICIÊNCIA
1. A importação de padrão e material de referência deverá submeter-se à fiscalização pela autoridade sanitária em exercício no local de desembaraço, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, instruída por Termo de Responsabilidade constante do Capítulo XX, deste Regulamento.
1. A importação de padrão e material de referência deverá submeter-se à fiscalização pela autoridade sanitária, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, instruída por Termo de Responsabilidade constante do Capítulo XX, desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1.1. Não será permitida a importação de padrão e material de referência para fins de ensaio de proficiência, com prazo de validade a expirar-se nos próximos 30 (trinta) dias a partir de sua autorização sanitária, no que couber.
1.2. As importações de que trata este Capítulo dar-se-ão por meio das modalidades de importação SISCOMEX e Remessa Expressa.
1.3. A importação de que trata este Capítulo estará desobrigada da autorização de embarque no exterior.
1.3.1. Excetuam-se do disposto neste subitem as importações de bens e produtos que integram os procedimentos 1, 1A, 3 e 6, do Capítulo XXXIX.
1.3.1. Excetuam-se do disposto neste subitem as importações de bens e produtos que integram os procedimentos 1 e 1A do Capítulo XXXIX. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1.4. O Termo de Responsabilidade, do Capítulo XX-A de que trata este Capítulo deverá ser apresentado com o reconhecimento de firma em cartório.
1.4. O Termo de Responsabilidade, do Capítulo XX-A, de que trata o presente Capítulo, deverá ser apresentado com assinatura do representante legal e do responsável técnico. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1.4.1. Ficarão desobrigados da exigência do reconhecimento de firma em cartório os signatários autorizados pelos responsáveis pela gestão do Sistema Nacional de Laboratórios de Saúde Pública
1.5. Será vedada a alteração da finalidade a que se destina a importação de que trata este Capítulo.
CAPÍTULO XX-A
I

CAPÍTULO XXI
PRODUTO NÃO REGULARIZADO NO SISTEMA NACIONAL DE VIGILÂNCIA SANITÁRIA - SNVS - PARA FINS DE REGISTRO, DESTINADO À PESQUISA DE MERCADO, ANÁLISE LABORATORIAL, TESTES DE CONTROLE DA QUALIDADE, AVALIAÇÃO DE EMBALAGEM OU ROTULAGEM E TESTES DE EQUIPAMENTO
SEÇÃO I –
DOS MEDICAMENTOS
1. A importação de amostras de produtos nas formas de produto acabado ou a granel, pertencentes à classe de medicamentos não regularizados que contenham em sua composição substância(s) sem comprovação de segurança e eficácia estabelecidas, destinada à análise para fins de registro, testes de controle da qualidade, estudos de estabilidade, bioequivalência e equivalência farmacêutica ou ainda testes de equipamentos participantes do processo fabril ou laboratorial, deverá submeter-se à autorização de embarque no Licenciamento de Importação - LI, pela área técnica competente da Gerência Geral de Portos, Aeroportos, Fronteiras e Recintos Alfandegados - GGPAF, em sua sede na ANVISA, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2.
1.1 - Incluir-se-ão no disposto neste item as matérias-primas e princípios ativos integrantes de formulações desses medicamentos em fase de análise técnica para registro perante ANVISA, destinadas exclusivamente à realização de ensaios de controle da qualidade, em laboratório analítico instalado no território nacional.
1. A importação de amostras de produtos acabados, a granel ou matéria-prima, pertencentes à classe de medicamentos não regularizados na ANVISA, que contenham em sua composição substância sem comprovação de segurança e eficácia estabelecida, destinadas a testes, terá a Autorização de Embarque analisada e concedida pela autoridade sanitária, no local de desembaraço aduaneiro, mediante a apresentação da Petição para Fiscalização e Liberação Sanitária. (NR) (Redação dada pela Resolução - RDC nº 28, de 28 de junho de 2011)
2. A importação de amostras de medicamentos não regularizados cuja composição integra substâncias ativas com comprovação de segurança e eficácia estabelecidas, deverá atender as exigências sanitárias previstas nos procedimentos 1, 1A, 2, 2A, 2B, 2C, 3, 5.3 e 6, no que couber, no Capítulo XXXIX.
2.1. Excetua-se do disposto neste item os documentos referentes à regularização do medicamento perante a ANVISA, previsto nos procedimentos do Capítulo XXXIX.
3. O deferimento do Licenciamento de Importação e a liberação sanitária dar-se ão em conformidade com o disposto no Capítulo XXXIX deste Regulamento, pela autoridade sanitária em exercício no local de desembaraço do produto.
4. A importação de que trata esta seção deverá ser em quantidade compatível com a finalidade informada.
5. Será vedada a importação de medicamentos não regularizados junto a ANVISA, destinados à pesquisa de mercado.
SEÇÃO II
DOS PRODUTOS MÉDICOS E PRODUTOS PARA DIAGNÓSTICO IN VITRO
6. A importação de amostras de produtos na forma de produto acabado pertencentes à classe de produtos médicos e produtos para diagnóstico in vitro, não regularizados na ANVISA, destinados à análise para fins de registro, ensino ou teste de controle da qualidade deverá submeter-se a deferimento do Licenciamento de Importação - LI, pela autoridade sanitária no local de seu desembaraço, após parecer conclusivo e satisfatório da área técnica competente da ANVISA, em sua sede, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2.
6.1. A importação do produto estará desobrigada de autorização de embarque no exterior.
6 - A importação de amostras de produtos acabados, pertencentes à classe de produtos para saúde não regularizados na ANVISA, destinadas a testes, deverá submeter-se a análise e deferimento do Licenciamento de Importação pela autoridade sanitária, no local de desembaraço aduaneiro, mediante apresentação de Petição para Fiscalização e Liberação Sanitária. (NR) (Redação dada pela Resolução - RDC nº 28, de 28 de junho de 2011)
7. Serão vedadas a comercialização e alteração de finalidade informada no procedimento a que se destina a importação de que trata esta Seção.
SEÇÃO III
DOS SANEANTES
8. A importação de amostras de produtos na forma de produto acabado pertencentes à classe de saneantes domissanitários, não regularizados junto a ANVISA, e que não estejam expressamente proibidos no território nacional, destinados a análise para fins de registro, teste de controle da qualidade, proficiência, desenvolvimento de novos produtos ou de equipamentos participantes do processo fabril ou laboratorial , deverá submeter-se a fiscalização pela autoridade sanitária no local de desembaraço do produto, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2.
8.1. Incluir-se-á no disposto neste item a importação de amostras de matérias primas, princípios ativos integrantes de formulações de saneantes não autorizados para consumo humano e em fase de análise técnica para registro perante a ANVISA, destinadas exclusivamente à realização de ensaios de controle da qualidade em laboratório analítico instalado no território nacional.
8.2. Excluir-se-á deste item o produto destinado a pesquisa de mercado, o qual será submetido a parecer da área técnica competente da ANVISA, em sua sede, previamente ao seu desembaraço.
8.3. A importação de produtos de que trata esta Seção dar-se-á por meio do Siscomex ou Remessa Expressa.
8.4. A importação do produto estará desobrigada de autorização de embarque no exterior.
9. Serão vedadas a comercialização e alteração de finalidade informada no procedimento a que se destina a importação de que trata esta Seção.
SEÇÃO IV
DOS COSMÉTICOS, PERFUMES E PRODUTOS DE HIGIENE PESSOAL
10. O disposto nesta Seção abrange a importação de amostras de produtos nas formas de produto acabado ou a granel, pertencentes à classe de cosméticos, perfumes e produtos de higiene pessoal, não regularizados junto a ANVISA, e que não estejam expressamente proibidos no território nacional, destinadas a análise laboratorial de controle da qualidade e avaliação de embalagem e rotulagem, análise para fins de registro, desenvolvimento de novos produtos e pesquisa de mercado, ensaios de segurança e eficácia.
10.1 A importação de que trata o item anterior deverá submeter-se à fiscalização pela autoridade sanitária em exercício no local de desembaraço do bem ou produto, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, instruída por Termo de Responsabilidade específico constante do Capítulo XXII, deste Regulamento.
10.2. A importação de produtos de que trata esta Seção dar-se-á por meio do SISCOMEX ou Remessa Expressa.
10.3. A importação do produto estará desobrigada de autorização de embarque no exterior.
10.4. O Termo de Responsabilidade de que trata esta Seção deverá ser apresentado com reconhecimento de firma em cartório.
11. Será facultada a importação pelo laboratório habilitado pela Rede Brasileira de Laboratórios Analíticos em Saúde - REBLAS, mediante a apresentação de declaração de autorização da pessoa jurídica interessada na realização dos ensaios e de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, instruída por Termo de Responsabilidade constante do Capítulo XXII, deste Regulamento.
11.1. O importador de que trata o item anterior ficará desobrigado da autorização de funcionamento para a atividade de importar.
12. Serão vedadas a comercialização e alteração da finalidade informada no procedimento a que se destina a importação de que trata esta Seção.
SEÇÃO V
DOS ALIMENTOS
13. A importação de amostras de matéria - prima e produto acabado, pertencentes à classe de alimentos, destinada à análise para fins de registro, teste de controle da qualidade, avaliação de embalagem ou rotulagem, desenvolvimento de novos produtos ou de equipamentos participantes do processo fabril ou laboratorial e pesquisa de mercado, deverá submeter-se à fiscalização pela autoridade sanitária em exercício no local de desembaraço do produto, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, instruída por Termo de Responsabilidade constante do Capítulo XXII, deste Regulamento.
13.1. Excetuar-se-á do disposto neste item, a importação de amostras de alimentos destinadas à análise para fins de registro, teste de controle da qualidade e de equipamentos participantes do processo fabril ou laboratorial, e pesquisa de mercado que não possuam:
a) substância ou mistura de substâncias similares regularizadas perante o Sistema Nacional de Vigilância Sanitária;
b) Padrão de Identidade e Qualidade - PIQ - aprovado em Regulamento Técnico Específico.
13.2. A importação de que trata o subitem anterior deverá ser analisada e autorizada pelo setor técnico competente na sede da ANVISA previamente a ação fiscal, a ser executada pela autoridade sanitária em exercício no local de desembaraço, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, instruída por Termo de Responsabilidade constante do Capítulo XXII, deste Regulamento.
13.3. A exigência de que trata o subitem 12.1 independerá da condição de obrigatoriedade ou não de registro do produto.
13.4. A importação de produto de que trata esta Seção dar-se-á por meio das modalidades de importação SISCOMEX ou Remessa Expressa.
13.5. A importação do produto estará desobrigada de autorização de embarque no exterior.
13.6. O Termo de Responsabilidade de que trata esta Seção deverá ser apresentado com reconhecimento de firma em cartório.
13.7. Não será autorizada a importação de amostra de alimento com obrigatoriedade de registro na ANVISA, cuja finalidade seja pesquisa de mercado.
14. Serão vedadas a comercialização e alteração da finalidade informada no procedimento a que se destina a importação de que trata esta Seção.
SEÇÃO VI
DAS DISPOSIÇÕES FINAIS
15. A Petição para Fiscalização e Liberação Sanitária de que tratam os itens 1, 5, 7 e 12 deverá ser instruída por documento apresentado com reconhecimento de firmas em cartório, responsável técnico e responsável legal da empresa importadora, onde deverão constar as seguintes informações:
a) finalidade da importação;
b) quantidade total, justificada, para o número de amostras importadas;
c) detalhamento da fórmula qualitativa e quantitativa da amostra importada, exceto quando se tratar de produtos médicos;
d) especificações técnicas da amostra importada;
e) números dos lotes, ou partidas, e número de unidades produzidas por lote; f) prazo de validade por lote das amostras importadas;
g) descrição dos testes a serem realizados no território nacional, com o resumo do protocolo justificando a quantidade solicitada, quando couber;
h) descrição da metodologia da pesquisa, se for o caso;
i) ocorrência de resíduos resultantes da operacionalização da finalidade de importação proposta, metodologia de tratamento adequados inativação;
j) dizeres do rótulo do produto, quando se tratar de alimentos;
l) nome do responsável técnico pelo produto importado e respectivas informações referentes ao Cadastro de Pessoa Física e Conselho profissional de seu registro, com identificação do número de inscrição.
15.1. A critério da autoridade sanitária poderá ser requerida, para os fins do disposto na alínea "j" do item anterior à apresentação da respectiva tradução para o idioma pátrio do rótulo do produto importado, subscrito pelo responsável técnico e pelo responsável ou representante legal da empresa importadora do produto junto ao Sistema Nacional de Vigilância Sanitária.
15.2. No caso de amostras pertencentes à classe de medicamentos, além das demais exigências previstas neste item, ficará o importador obrigado a apresentar a autoridade sanitária em exercício no local de seu desembaraço, após a chegada do produto no território nacional, o laudo analítico de controle da qualidade para cada lote de amostra importada e o Termo de Responsabilidade constante do Capítulo XXII.
15.3. O Termo de Responsabilidade de que trata o subitem anterior deverá ser apresentado com reconhecimento de firma em cartório de seus assinantes, responsável técnico e representante legal da empresa importadora.
16. A Petição de Fiscalização e Liberação Sanitária de amostras importadas de que tratam os itens 1, 5, 7, 9, e 12 deverá ocorrer junto à autoridade sanitária em exercício no local onde ocorrerá o seu desembaraço.
CAPÍTULO XXI
PRODUTO NÃO REGULARIZADO NO SISTEMA NACIONAL DE VIGILÂNCIA SANITÁRIA - SNVS - PARA FINS DE REGISTRO, DESTINADO À PESQUISA DE MERCADO, ANÁLISE LABORATORIAL, TESTES DE CONTROLE DA QUALIDADE, AVALIAÇÃO DE EMBALAGEM OU ROTULAGEM E TESTES DE EQUIPAMENTO
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) SEÇÃO I
DOS MEDICAMENTOS
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1. A importação de amostras de produtos acabados, a granel ou matéria-prima, pertencentes à classe de medicamentos não regularizados na ANVISA, destinadas a testes, deverá submeter-se a análise e deferimento do Licenciamento de Importação pela autoridade sanitária, mediante apresentação de Petição para Fiscalização e Liberação Sanitária, instruída por Termo de Responsabilidade constante do Capítulo XXII, desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2. A importação de amostras de medicamentos não regularizados deverá atender as exigências sanitárias previstas nos procedimentos 1, 1A, 2, 2A, 2B, 2C, 3, 5.3 e 6, no que couber, do Capítulo XXXIX desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.1. Excetua-se do disposto no item 2 desta Seção os documentos referentes à regularização do medicamento perante a ANVISA, previstos nos procedimentos do Capítulo XXXIX desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3. A importação de que trata esta Seção deverá ser em quantidade compatível com a finalidade informada. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
4. É vedada a importação de medicamentos não regularizados junto à ANVISA, destinados à pesquisa de mercado. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO II
DOS PRODUTOS MÉDICOS E PRODUTOS PARA DIAGNÓSTICO IN VITRO (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5. A importação de amostras de produtos acabados pertencentes a classe de produtos para saúde não regularizados na ANVISA, destinadas a testes, ensino ou treinamento, deverá submeter-se a análise e deferimento do Licenciamento de Importação pela autoridade sanitária, mediante apresentação de Petição para Fiscalização e Liberação Sanitária, instruída por Termo de Responsabilidade constante do Capítulo XXII, desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5.1. A importação do produto estará desobrigada de autorização de embarque no exterior. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
6. É vedada a comercialização das amostras de produtos de que trata esta Seção, bem como a alteração da finalidade a que se destina, informada no procedimento de importação. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO III
DOS SANEANTES
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
7. A importação de amostras de produtos, na forma de produto acabado pertencentes à classe de saneantes domissanitários, não regularizados junto à ANVISA, e que não estejam expressamente proibidos no território nacional, destinados a análise para fins de registro, teste de controle da qualidade, proficiência, desenvolvimento de novos produtos ou de equipamentos participantes do processo fabril ou laboratorial, darse-á mediante a apresentação de Petição para Fiscalização e Liberação Sanitária, prevista no Capítulo II, subitem 1.2, instruída por Termo de Responsabilidade constante do Capítulo XXII desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
7.1. Inclui-se no disposto no item 7 desta Seção a importação de amostras de matérias-primas, princípios ativos integrantes de formulações de saneantes não autorizados para consumo humano e em fase de análise técnica para registro perante a ANVISA, destinadas exclusivamente à realização de ensaios de controle da qualidade em laboratório analítico instalado no território nacional. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
7.2. Exclui-se do disposto no item 7 desta Seção produto destinado a pesquisa de mercado, o qual será submetido a parecer da área técnica competente da ANVISA em sua sede, previamente ao seu desembaraço. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
7.3. A importação dos produtos de que trata esta Seção dar-se-á por meio do Siscomex ou de Remessa Expressa. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
7.4. A importação do produto de que trata esta Seção estará desobrigada de autorização de embarque no exterior. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
8. É vedada a comercialização das amostras de produtos de que trata esta Seção, bem como a alteração da finalidade a que se destina a importação, informada no procedimento de importação. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO IV
DOS COSMÉTICOS, PERFUMES E PRODUTOS DE HIGIENE PESSOAL (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
9. O disposto nesta Seção abrange a importação de amostras de produtos, nas formas de produto acabado ou a granel, pertencentes à classe de cosméticos, perfumes e produtos de higiene pessoal, não regularizados junto à ANVISA, e que não estejam expressamente proibidos no território nacional, destinadas a análise laboratorial de controle da qualidade e avaliação de embalagem e rotulagem; análise para fins de registro; desenvolvimento de novos produtos e pesquisa de mercado; ou ensaios de segurança e eficácia. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
9.1 A importação de que trata o item 9 desta Seção deverá submeter-se a fiscalização pela autoridade sanitária, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária, prevista no Capítulo II, subitem 1.2, a qual deverá estar instruída por Termo de Responsabilidade, constante do Capítulo XXII, desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
9.2. A importação dos produtos de que trata esta Seção dar-se-á por meio do SISCOMEX ou de Remessa Expressa. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
9.3. A importação dos produtos de que trata esta Seção estará desobrigada de autorização de embarque no exterior. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
10. A importação de que trata esta Seção será facultada a laboratório habilitado pela Rede Brasileira de Laboratórios Analíticos em Saúde (REBLAS), mediante a apresentação de declaração de autorização da pessoa jurídica interessada na realização dos ensaios e de Petição para Fiscalização e Liberação Sanitária, prevista no Capítulo II, subitem 1.2, a qual deverá estar instruída por Termo de Responsabilidade, constante do Capítulo XXII, desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
10.1. O importador de que trata o item 10 desta Seção ficará desobrigado da autorização de funcionamento para atividade de importar. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
11. É vedada a comercialização das amostras de produtos de que trata esta Seção, bem como a alteração da finalidade a que se destina a importação, informada no procedimento de importação. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO V
DOS ALIMENTOS
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
12. A importação de amostras de matéria-prima e produto acabado, pertencentes à classe de alimentos, destinada a análise para fins de registro, teste de controle da qualidade, avaliação de embalagem ou rotulagem, desenvolvimento de novos produtos ou de equipamentos participantes do processo fabril ou laboratorial, ou pesquisa de mercado, deverá submeter-se a fiscalização pela autoridade sanitária, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária, prevista no Capítulo II, subitem 1.2, a qual deverá estar instruída por Termo de Responsabilidade, constante do Capítulo XXII desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
12.1. A importação destinada a pesquisa de mercado dependerá de parecer favorável concedido pelo setor técnico competente da ANVISA em sua sede. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
12.2. A exigência de que trata o subitem 12.1 desta Seção independerá da obrigatoriedade de registro do produto. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
12.3. A importação de produto de que trata esta Seção dar-se-á por meio das modalidades de importação SISCOMEX ou Remessa Expressa. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
12.4. A importação de produto de que trata esta Seção estará desobrigada de autorização de embarque no exterior. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
12.5. Não será autorizada a importação de amostra de alimento com obrigatoriedade de registro na ANVISA, cuja finalidade seja pesquisa de mercado. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
13. É vedada a comercialização das amostras de produtos de que trata esta Seção, bem como a alteração da finalidade a que se destina a importação, informada no procedimento de importação. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO VI
DAS DISPOSIÇÕES FINAIS
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
14. A Petição para Fiscalização e Liberação Sanitária de que tratam as Seções I, II, III e IV deste Capítulo deverá ser instruída por documento subscrito pelo responsável técnico e responsável legal da Empresa importadora, no qual deverão constar as seguintes informações: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) finalidade da importação; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) quantidade total, justificada, para o número de amostras importadas; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) detalhamento da fórmula qualitativa e quantitativa da amostra importada, exceto quando se tratar de produtos médicos; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) especificações técnicas da amostra importada; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e) números dos lotes, ou partidas, e número de unidades produzidas por lote; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
f) descrição dos testes a serem realizados no território nacional, com o resumo do protocolo justificando a quantidade solicitada, quando couber; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) descrição da metodologia da pesquisa, se for o caso; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
h) ocorrência de resíduos resultantes da operacionalização da finalidade de importação proposta, metodologia de tratamento adequados inativação; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
i) nome do responsável técnico pelo produto importado e respectivas informações referentes ao Cadastro de Pessoa Física e Conselho profissional de seu registro, com identificação do número de inscrição. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
CAPÍTULO XXII
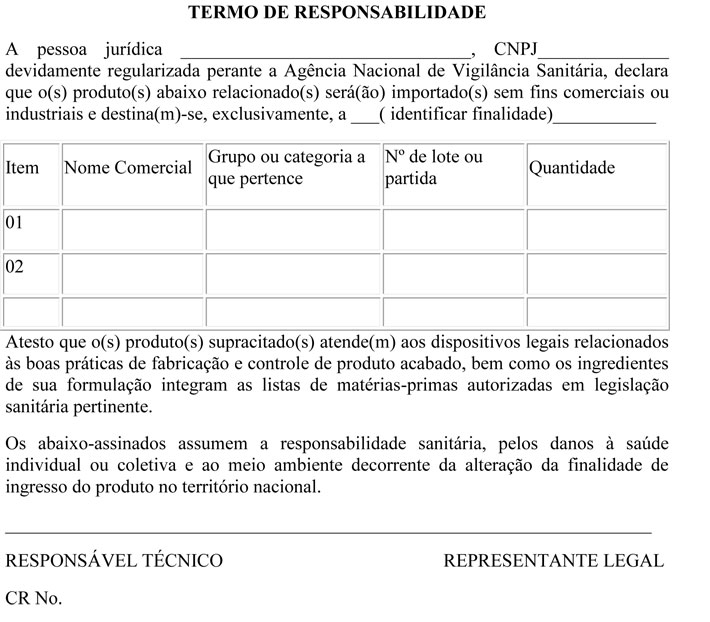
Obs. A pessoa jurídica "Laboratório" está dispensada de regularização na ANVISA. CAPÍTULO XXIII
IMPORTAÇÃO DE CÉLULAS E TECIDOS HUMANOS PARA FINS TERAPÊUTICOS
SEÇÃO I
DAS DISPOSIÇÕES GERAIS
1. O ingresso no território nacional de células e tecidos somente será autorizado mediante comprovação da sua finalidade terapêutica pelo importador, e critérios da legislação pertinente, inclusive de biossegurança, atendidas as exigências sanitárias deste Regulamento.
2. A importação de que trata este Capítulo, salvo disposição expressa, dar-se-á por meio das modalidades de importação no Sistema Integrado de Comércio Exterior - SISCOMEX - Módulo Importação, Remessa Expressa, ou Declaração Simplificada de Importação, não eletrônica, ou Bagagem Acompanhada.
2.1. Para fins de autorização da importação, o interessado deverá apresentar o pleito de importação, à Gerencia Geral de Sangue, Outros Tecidos, Células e Órgãos - GGSTO, acompanhado das informações exigidas neste Capítulo com antecedência mínima de 5 (cinco) dias úteis da data prevista da chegada do material no território nacional.
2.2. Para os fins de fiscalização e liberação sanitária, o importador deverá apresentar à ANVISA Petição para Fiscalização e Liberação Sanitária, de que trata o subitem 1.2. do Capítulo II.
3. O deferimento e liberação sanitária da importação do material de que trata este Capítulo, nas modalidades descritas, dar-se-ão pela manifestação expressa da autoridade sanitária em exercício no local de seu desembaraço após inspeção física satisfatória, assim como manifestação expressa e favorável de importação pela Coordenação Geral do Sistema Nacional de Transplante - CGSNT, e de parecer técnico favorável da Gerência-Geral de Sangue, outros Tecidos, Células e Órgãos - GGSTO - da ANVISA, em sua sede, no âmbito de suas competências, emitido após recebimento e avaliação das exigências constantes deste Capítulo em análise documental.
3.1. Excetuar-se-á do disposto neste item a importação de células e tecidos germinativos e pré-embriões humanos, que dependerá somente do parecer técnico favorável da Gerência-Geral de Sangue, outros Tecidos, Células e Órgãos - GGSTO.
3.2. Será autorizada a guarda e responsabilidade ao importador de células e tecidos integrantes das Seções III e IV deste Capítulo, em ambientes apropriados à manutenção de sua integridade.
4. Caberá ao importador a obrigação pelo cumprimento das normas regulamentares e legais, medidas, formalidades e exigências ao processo administrativo de importação.
4.1. Incluir-se-á no disposto neste item a obrigação de adotar medidas idôneas, próprias e junto a terceiros contratados para a importação do material de que trata esse Capítulo, que evitem ou impeçam prejuízo à saúde.
5. Os casos omissos referentes à importação de células e tecidos para fins terapêuticos serão examinados em conjunto pela Gerência-Geral de Portos, Aeroportos, Fronteiras e Recintos Alfandegados - GGPAF, e pela Gerência-Geral de Sangue, outros Tecidos, Células e Órgãos - GGSTO, e decididos pelo Diretor responsável pela supervisão desta Gerência-Geral da ANVISA.
6. O acondicionamento, embalagem e transporte do material biológico de que trata este Capítulo deverá ser efetivado de modo que sejam garantidas e mantidas a sua integridade, em recipiente apropriado e exclusivo para a finalidade da importação, na temperatura adequada, e devidamente identificado, de acordo com o disposto neste Regulamento e na legislação pertinente, e, subsidiariamente, pelas informações complementares indicadas pelo importador.
6.1. Serão consideradas exclusivamente para efeito deste Capítulo embalagens externas:
a) o recipiente térmico rígido ou embalagem resistente para revestimento de isolante térmico, quando o material biológico for transportado com gelo ou gelo seco ou outro material refrigerante utilizado.
b) embalagem rígida, utilizada nos transportes contendo "dry-shipper", quando o material biológico for transportado em nitrogênio líquido.
7. O material de que trata este Capítulo deverá apresentar-se, quando da sua chegada no território nacional, com embalagem externa identificada na língua pátria ou língua inglesa, com as seguintes informações:
a) nome, endereço completo, telefone e identificação do importador, com indicação do Cadastro Nacional de Pessoa Física ou Cadastro Nacional de Pessoa Jurídica;
b) nome, endereço completo e telefone da instituição de origem;
c) nome, endereço completo e telefone do estabelecimento de saúde de destino, com indicação do Cadastro Nacional da Pessoa Jurídica;
d) condições de conservação do material com data e horário de acondicionamento;
e) peso do contêiner quando da saída da instituição fornecedora para material armazenado em "dryshipper".
7.1. A identificação de que trata este item deverá ser de fácil visualização de modo a permitir sua imediata leitura, e deverá conter as exigências das normas de biossegurança.
7.2. A identificação de tecido músculo-esquelético, pele, valva cardíaca e córnea de que trata este item deverá conter os seguintes dizeres: "MATERIAL BIOLÓGICO PARA FINS TERAPÊUTICOS".
7.3. A identificação de células e tecidos germinativos, embriões e células progenitoras hematopoéticas de que trata este item deverá conter os seguintes dizeres: "MATERIAL BIOLÓGICO PARA FINS TERAPÊUTICOS. VEDADA SUBMISSÃO À IRRADIAÇÃO (RAIOS X)",
7.4. As embalagens que contenham gelo seco, nitrogênio líquido ou outro líquido criogênico deverão estar sinalizadas externamente, de acordo com as normas nacionais e internacionais para transporte de produtos perigosos.
7.5. No caso das córneas deverá também constar prazo de validade.
8. As Coordenações de Vigilância Sanitária de Portos, Aeroportos e Fronteiras nos Estados e Distrito Federal deverão informar à GGSTO as condições de armazenamento e acondicionamento do material biológico quando da sua chegada e observações complementares relacionadas à sua integridade.
SEÇÃO II
DA IMPORTAÇÃO DE PELE, TECIDO MÚSCULO-ESQUELÉTICO E VALVA CARDÍACA
9. Além do disposto na Seção I deste Capítulo, aplicar-se-á à importação de pele, tecido músculo-esquelético e valva cardíaca o previsto nesta Seção e legislação pertinente.
10. A importação do material de que trata esta Seção deverá sujeitar-se à manifestação expressa e favorável da CGSNT por meio de um comprovante de autorização da importação, previamente ao seu embarque no exterior.
11. Após manifestação expressa e favorável da CGSNT, caberá a ANVISA a fiscalização e liberação sanitária da importação do material de que trata esta Seção.
11.1. A solicitação de parecer técnico de que trata o item 3 deste Capítulo deverá ser instruído com as seguintes informações:
a) nome e Cadastro Nacional de Pessoa Física do receptor;
b) tipo de material biológico a ser importado e quantidade;
c) nome e endereço completo da instituição fornecedora que processou o material;
c) país de origem do material a ser importado;
d) país de procedência do material a ser importado;
e) data da retirada, validade, condições de armazenamento e acondicionamento, tipo de processamento e recomendações complementares relacionadas à sua qualidade e integridade;
f) identificação do transportador, local e data prevista para sua chegada;
g) nome e endereço completos do estabelecimento de saúde ou profissional transplantador a qual se destina o material.
11.2. Deverão ser encaminhados junto à solicitação de importação os seguintes documentos:
a) laudo com o diagnóstico emitido pelo profissional responsável pelo procedimento terapêutico, justificando o procedimento e a importação;
b) autorização do receptor para a realização do procedimento terapêutico, ou autorização dos pais/ responsável legal, quando o receptor for juridicamente incapaz, assinada e com firma reconhecida;
c) resultados de exames sorológicos do doador, para marcadores de infecções transmissíveis HIV-1 e 2, Sífilis, Hepatite B, Hepatite C, HTLV I / II, doença de Chagas, Toxoplasmose, Citomegalovírus, e outros que venham a ser exigidos pela legislação pertinente, bem como os demais controles sorológicos obrigatórios no país origem;
d) resultados de exames microbiológicos, quando couber.
e) possíveis resíduos de produtos químicos utilizados no processamento que possam desencadear reações adversas.
f) informação sobre tipo de esterilização complementar.
12. Quanto ao acondicionamento e transporte:
a) a embalagem deve assegurar a integridade e a esterilidade de seu conteúdo e não oferecer risco de liberação de substâncias citotóxicas ou pirogênicas para o produto.
b) o material deverá ser transportado em sistema validado para manutenção de temperatura adequada para cada tipo de tecido, conforme itens 12.1, 12.2 e 12.3.
c) O recipiente térmico deve assegurar o trânsito do material em temperatura adequada por um período de 24 (vinte e quatro) horas além do tempo estimado para a chegada do material até o local de destino.
12.1. Quando se tratar de peças ósseas o material deverá ser acondicionado e embalado em:
a) embalagens plásticas, triplas, estéreis, ou embalagem primária de vidro estéril e secundária de plástico estéril, ou única, de vidro estéril lacrado adequadas para o armazenamento dos tecidos até seu uso;
b) recipiente térmico que garanta a manutenção de temperatura inferior 6° C positivos.
12.1.1. excetua-se do disposto no subitem 12.1.b o transporte de osso liofilizado que é realizado em temperatura ambiente.
12.2. Quando se tratar de tecidos moles e pele devem ser acondicionados e embalados em:
a) embalagens plásticas, duplas, estéreis ou embalagem primária de vidro, estéril, com secundária de plástico estéril adequadas para o armazenamento dos tecidos até seu uso;
b) recipiente térmico que garanta a manutenção de temperatura entre 2 e 8° C positivos;
12.3. Quando se tratar de valvas cardíacas o material deverá ser acondicionado e embalado em:
a) embalagens plásticas, duplas, estéreis adequadas para o armazenamento dos tecidos até seu uso;
b) reservatório especial para transporte contendo nitrogênio líquido, "dryshipper", para manutenção de temperatura de 150º C negativos por 48 (quarenta e oito) horas além do tempo estimado para a chegada do material até o local de destino;
c) embalagem externa rígida para proteção do "dryshipper".
12.4. Entre as embalagens primária e secundária, ou secundária e terciária deve haver etiqueta contendo as seguintes informações:
a) nome, endereço completo e telefone de contato da instituição fornecedora; b) identificação do doador;
c) código alfa-numérico, único, de identificação da unidade de tecido; d) tipo de tecido;
e) quando se tratar de tecido músculo - esquelético e pele, especificar o processamento, a quantidade de tecido expressa em volume, peso, dimensão ou a combinação dessas unidades de medida quando aplicável;
f) data de validade;
g) condições para armazenamento;
h) informação de que o produto está liberado para uso em humanos;
i) possíveis resíduos de produtos químicos utilizados no processamento que possam desencadear reações adversas;
j) informação sobre tipo de esterilização complementar.
SEÇÃO III
DA IMPORTAÇÃO DE CÉLULAS PROGENITORAS HEMATOPOÉTICAS
13. Além do disposto na Seção I deste Capítulo, aplicar-se-á à importação de células progenitoras hematopoéticas obtidas de medula óssea, sangue periférico, ou de sangue de cordão umbilical e placentário, para fins de transplante alogênico, o previsto nesta Seção e na legislação pertinente.
14. A importação de que trata esta Seção dar-se-á pela CGSNT.
15. Caberá a ANVISA a fiscalização e liberação sanitária da importação do material de que trata esta Seção.
16. O parecer técnico de que trata o item 3 deste Capítulo deverá ser instruído por solicitação para importação com as seguintes informações:
16.1. Quanto aos dados relacionados ao receptor do material:
a) nome, número do Cartão Nacional de Saúde e número do Registro Brasileiro de Receptores de Medula Óssea (REREME);
b) relatório médico justificando a necessidade do procedimento;
c) autorização do receptor para a realização do procedimento terapêutico, ou autorização dos pais / responsável legal, quando o receptor for juridicamente incapaz, assinada e com firma reconhecida.
16.2. Quanto aos dados relacionados ao material importado:
a) nome e endereço completo da instituição fornecedora do material;
b) resultados de exames sorológicos do doador, para marcadores de infecções transmissíveis HIV-1 e 2, Sífilis, Hepatite B, Hepatite C, HTLV I / II, Citomegalovírus e outros que venham a ser exigidos pela legislação pertinente, bem como os demais controles sorológicos obrigatórios no país origem. Na hipótese de importação de células progenitoras hematopoéticas de sangue de cordão umbilical e placentário deverão ser informados os resultados dos exames sorológicos da genitora, e/ou os resultados dos exames realizados na unidade de sangue de cordão umbilical e placentário coletada, conforme previsto em legislação pertinente;
b.1) a Autoridade Sanitária competente do país receptor deve analisar o perfil epidemiológico das patologias transmissíveis pelo sangue existentes no país de origem do material, podendo exigir a informação ou realização de outros testes na unidade de células progenitoras hematopoéticas.
c) resultado dos exames de histocompatibilidade;
d) resultados dos testes de viabilidade celular, número total de células nucleadas, número de unidades formadoras de colônias granulocíticas-monocíticas (CFU-GM), contagem de CD34, resultados dos testes de contaminação bacteriana, aeróbica e anaeróbica, e fúngica, em conformidade com a legislação pertinente, quando couber;
e) data da coleta, condições de armazenamento e acondicionamento, e recomendações complementares relacionadas à sua qualidade e integridade;
f) país de origem do material a ser importado;
g) país de procedência do material a ser importado;
h) identificação do transportador, local e data prevista para sua chegada; i) nome e endereço da instituição transplantadora a qual se destina o material.
17. O acondicionamento, embalagem e transporte do material de que trata esta Seção deverá ser efetivado de modo que sejam observadas as disposições do item 6 deste Capítulo.
17.1. Quando se tratar de células progenitoras hematopoéticas não criopreservadas:
a) o material deverá ser acondicionado em bolsa plástica, apropriada para hemocomponentes;
b) o material deverá ser transportado em temperatura entre 4ºC e 24ºC, em recipiente térmico dotado de sistema de registro da temperatura interna que indique valores fora dos limites estabelecidos.
17.1.1. Os prazos entre o término da coleta e o início da infusão não deverão exceder 48 (quarenta e oito) horas.
17.1.2. O material utilizado para manutenção da temperatura do recipiente térmico não poderá estar em contato direto com a embalagem primária.
17.2. Quando se tratar de células progenitoras hematopoéticas criopreservadas a 135°C negativos:
a) o material deverá ser acondicionado em bolsa plástica, apropriada para hemocomponentes;
b) a bolsa plástica deverá ser acondicionada em temperatura igual ou inferior à 135ºC negativos;
c) o material deverá ser transportado em contêiner:
c.1) mantido em embalagem protetora específica;
c.2) apropriado para transporte a seco, ou "dry-shipper";
17.2.1 O volume de nitrogênio líquido deverá ser suficiente para manutenção da temperatura por um prazo mínimo de 48 (quarenta e oito) horas além do horário estimado para sua chegada ao estabelecimento que fará a infusão.
17.3. Quando se tratar de células progenitoras hematopoéticas criopreservadas a 80°C negativos:
a) o material deverá ser acondicionado em bolsa plástica, apropriada para hemocomponentes;
b) o material deverá ser transportado em sistema validado para manutenção de temperatura igual ou inferior à 65ºC negativos pelo prazo de 24 (vinte e quatro) horas.
SEÇÃO IV
DA IMPORTAÇÃO DE CÉLULAS E TECIDOS GERMINATIVOS E PRÉ EMBRIÕES HUMANOS
18. Além do disposto na Seção I deste Capítulo, aplicar-se-á à importação de células e tecidos germinativos e pré-embriões humanos o previsto nesta Seção e na legislação pertinente.
19. A solicitação para a importação deve ser enviada à Gerência Geral de Sangue, outros Tecidos, Células e Órgãos - GGSTO/ANVISA, de documento em papel timbrado do estabelecimento de saúde onde o procedimento será realizado, e assinado pelo responsável legal e pelo profissional responsável pelo procedimento.
19.1 Este documento deverá conter as seguintes informações:
a) identificação do estabelecimento de saúde de destino (nome e Cadastro Nacional de Pessoa Jurídica), com identificação de sua licença sanitária;
b) identificação do material biológico, descrevendo também a sua quantidade;
c) identificação da receptora, do casal receptor, ou do proprietário (a) do material, com nome, Registro Geral e Cadastro Nacional de Pessoa Física;
d) justificativa da importação;
e) condições de armazenamento e de acondicionamento, e recomendações complementares relacionadas à sua integridade e qualidade, até o momento da utilização;
f) país de origem do material a ser importado;
g) país de procedência do material a ser importado;
h) identificação do Banco de Células e Tecidos Germinativos - BCTG no qual o material será armazenado, em caso do estabelecimento de saúde importador, onde o procedimento terapêutico será realizado, não ser um BCTG.
i) identificação do transportador, local e data prevista para sua chegada.
19.1.1. Para a importação de sêmen, tecidos ovariano e testicular, além das informações do subitem 19.1, também informar identificação e endereço completo da instituição fornecedora que processou o material a ser importado;
19.1.2. Para a importação de embriões, além das informações do subitem 19.1, também informar:
a) identificação e endereço completo da instituição fornecedora que realizou a fertilização in vitro e que está armazenando os embriões;
b) data do procedimento de fertilização in vitro e da criopreservação.
19.2. A solicitação para importação deverá ser acompanhada dos seguintes documentos:
a) cópia da licença sanitária do estabelecimento de saúde onde será realizado o procedimento;
b) cópia legível de documentos de identidade e Cadastro Nacional de Pessoa Física da receptora, casal receptor ou do (a) proprietário (a) do material;
c) laudo com o diagnóstico emitido pelo profissional responsável pelo procedimento terapêutico, justificando o procedimento e a importação;
d) autorização por escrito da receptora, do casal receptor ou do (a) proprietário (a) do material, para a realização do procedimento de reprodução assistida e para o transporte do material, assinada e com firma reconhecida, constando os números do Registro Geral e do Cadastro Nacional de Pessoa Física;
e) cópia da licença sanitária do BCTG no qual o material será armazenado, em caso do estabelecimento de saúde importador, onde o procedimento terapêutico será realizado, não ser um BCTG;
19.2.1 Para importação de embriões, além dos documentos em 19.2, enviar documento da instituição de origem, que comprove que os embriões importados são do casal.
19.2.2. Para importação de sêmen, tecidos ovariano e testicular, além dos documentos em 19.2, enviar documento da instituição de origem contendo os resultados dos exames clínicos, sorológicos, microbiológicos e genéticos realizados, para avaliação de risco de transmissão de doenças.
19.2.3. Para importação de sêmen doado para uso terapêutico em terceiros, além dos documentos em 19.2 e 19.2.2., enviar:
a) documento da instituição fornecedora, contendo os dados fenotípicos do doador;
b) documento comprobatório da ausência de células ou tecidos germinativos disponíveis, emitido por pessoas jurídicas idôneas de no mínimo 3 (três) Bancos de Células e Tecidos Germinativos instalados no país.
20. Quanto ao acondicionamento e transporte:
20.1. Para o transporte a temperatura interior do recipiente contendo a embalagem deverá ser adequada para a manutenção da integridade e qualidade do material importado.
20.2. O acondicionamento, a embalagem e o transporte devem garantir a segurança do material, inclusive a quantidade de nitrogênio no contêiner, que deve ser suficiente para um período de pelo menos 48 (quarenta e oito) horas além do período previsto para o desembaraço.
20.3. O responsável pelo acondicionamento do material no exterior deverá emitir declaração, que acompanhará o contêiner com o material biológico, contendo as seguintes informações:
a) nome e endereço completos da instituição fornecedora do material importado; b) data e hora da embalagem;
c) peso do contêiner, quando da saída da instituição fornecedora;
d) nome, endereço completo e telefone do estabelecimento de saúde de destino, com indicação do Cadastro Nacional de Pessoa Jurídica.
SEÇÃO V
DA IMPORTAÇÃO DE CÓRNEAS HUMANAS
21. Além do disposto na Seção I deste Capítulo, aplicar-se-á à importação de córneas humanas para fins de transplante o previsto nesta Seção e na legislação pertinente.
22. A importação do material de que trata esta Seção deverá sujeitar-se à manifestação expressa e favorável do SNT.
23. A importação de que trata esta Seção dar-se-á pelo paciente inscrito na lista de espera do transplante.
23.1. O paciente inscrito na lista de espera do transplante poderá outorgar poderes à terceiro para proceder à importação de que trata esta Seção, desde que comprove essa condição do outorgado.
24. Caberá a ANVISA a fiscalização e liberação sanitária da importação do material de que trata esta Seção.
25. O parecer técnico de que trata o item 3 deste Capítulo deverá ser instruído pela apresentação de documento descrito no subitem 25.1 e solicitação para importação.
25.1. Documento referente ao paciente fornecido pela Central de Notificação, Captação e Distribuição de Órgãos - CNCDO, do respectivo Estado de residência do paciente contendo as seguintes informações:
a) nome e Cartão Nacional de Saúde;
b) enfermidade que indica o transplante;
c) data de sua inclusão e número do paciente na lista de espera;
d) identificação no Conselho Profissional do responsável técnico da equipe que realizará o transplante;
e) nome e endereço completo do estabelecimento de saúde onde será realizado o procedimento.
25.2. A solicitação para importação deverá conter as seguintes informações:
a) nome e endereço completo da instituição de origem responsável pela retirada do tecido, processamento e liberação;
b) data da retirada e da validade, meio de preservação utilizado com o lote, condições de armazenamento e acondicionamento, e recomendações complementares relacionadas a sua qualidade e integridade;
c) país de origem do material a ser importado;
d) país de procedência do material a ser importado;
e) identificação do transportador, local e data de chegada;
26. Deverão ser encaminhados junto à solicitação de importação os resultados de exames sorológicos do doador para marcadores de doenças transmissíveis: HIV-1 e 2, Hepatite B, Hepatite C e outros que venham a ser exigidos em legislação sanitária pertinente.
27. Os formulários da instituição de origem com as informações sobre a doação, o doador (causa mortis, idade) e avaliação da córnea devem ser enviados juntamente com o tecido.
28. O prazo de validade máximo tolerável para córneas humanas importadas será determinada pela solução de conservação, conforme especificação do fabricante a contar da data de sua preservação, observadas as condições ambientais exigidas para sua manutenção e conservação, devendo chegar ao país até no mínimo 7 (sete) dias antes de expirado o prazo de validade.
29. O acondicionamento, embalagem e transporte do material de que trata esta Seção deverá ser efetivado de modo que sejam observadas as disposições do item 6 deste Capítulo, devendo ainda:
a) ser acondicionado em embalagem primária identificada com etiqueta, que deverá estar protegida contra choque mecânico;
b) ser transportado em recipiente térmico com a temperatura entre 2ºC e 8ºC, o qual deverá dispor de sistema de monitoramento de registro de temperatura interna que acuse valores fora desses limites.
29.1. O material refrigerante utilizado para manutenção da temperatura do recipiente térmico não poderá estar em contato direto com a embalagem primária.
29.2. Deverá ser assegurada a manutenção da temperatura para realização de transporte interno, até a chegada ao destino final.
30. Deverá ser encaminhado a GGSTO, pelo profissional responsável pelo procedimento/transplante, resultados de avaliação da córnea pós-transplante seis meses após o procedimento.
CAPÍTULO XXIV
MATERIAL BIOLÓGICO HUMANO PARA FINS DE DIAGNÓSTICO LABORATORIAL
1. A importação de material de natureza biológica humana destinado a diagnóstico laboratorial e de material de referência originário de material biológico humano destinado à implantação de metodologia analítica em estabelecimento prestador de serviço de diagnóstico clínico humano deverá se sujeitar, previamente ao seu desembaraço no território nacional, à manifestação expressa e favorável da autoridade sanitária competente.
1.1. Incluir-se-á nas disposições deste item o material procedente do exterior destinado à:
a) exames clínicos, biológicos, microbiológicos e imunológicos vinculados à triagem para verificação de compatibilidade entre doadores internacionais e pacientes com indicação médica de transplante, no território nacional;
b) testes de proficiência em laboratórios da rede integrante de programas especiais de saúde pública.
c) testes de proficiência em laboratórios da rede privada vinculados ao desenvolvimento de programas internacionais de proficiência.
d) diagnóstico laboratorial vinculado a programas oficiais de Saúde Pública.
1.2. Deverão ser cumpridas as exigências da legislação sanitária pertinente relacionadas à embalagem, transporte e armazenagem de material biológico de natureza humana.
2. A importação de material de natureza biológica humana de que trata este Capítulo dar-se-á por meio das modalidades de SISCOMEX - Módulo Importação, Remessa Expressa ou Remessa Postal, devendo o importador requerer sua fiscalização por meio de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, e instruída pelo Termo de Responsabilidade integrante do Capítulo XXV deste Regulamento.
2.1. O Termo de Responsabilidade deverá ser apresentado com reconhecimento de firma em cartório. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.1.1. Ficarão desobrigados da exigência do reconhecimento de firma em cartório os signatários autorizados pelos responsáveis pela Gestão do Sistema Nacional de Laboratórios de Saúde Pública. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3. O de material de natureza biológica humana, importada por meio do SISCOMEX - LI eximir-se-á da obrigação de autorização de embarque no exterior.
4. Será autorizada a importação por pessoa física, responsável técnico de estabelecimento de saúde prestador de serviço de diagnóstico laboratorial clínico humano de padrão de referência ou de proficiência, originário de material biológico humano para fins de implantação e desenvolvimento de metodologia analítica.
4.1. A pessoa física de que trata este item, além de atender as demais disposições deste Capítulo, deverá anexar à Petição de que trata o item 2, documento comprobatório de seu vínculo e função profissional com o estabelecimento de saúde, onde será implantada ou desenvolvida a metodologia.
4.2. O documento de que trata o subitem anterior deverá ser apresentado na sua forma original, e:
a) ser subscrito pelo responsável legal do estabelecimento de saúde com reconhecimento de firma em cartório;
b) expressar o compromisso de observância e cumprimento das normas e procedimentos estabelecidos pela legislação sanitária, bem como de ciência das penalidades as quais ficará sujeito, nos termos da Lei nº 6.437, de 20 de agosto de 1977.
5. Em situações excepcionais, em áreas geográficas de fronteira, poderá ser autorizada a importação por meio de pessoa física de amostras biológicas humanas destinadas a diagnóstico laboratorial clínico, mediante a apresentação perante a autoridade sanitária competente em exercício, de receituário médico com indicação do tipo de exame a ser realizado.
6. As amostras biológicas humanas deverão apresentar-se devidamente acondicionadas e em embalagens apropriadas e previstas em legislação vigente.
CAPÍTULO XXV
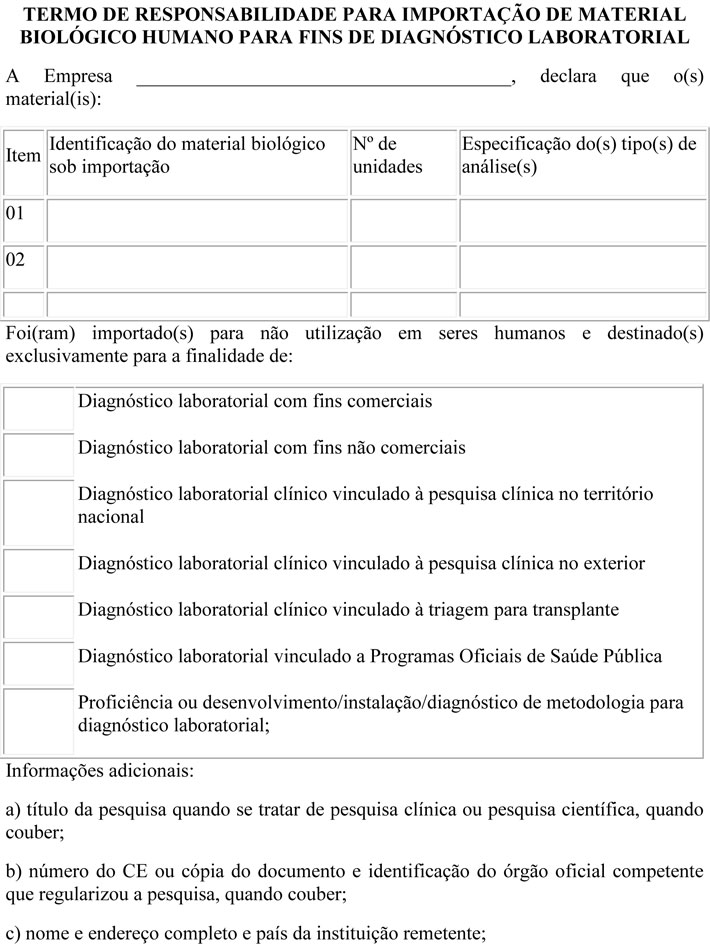

CAPÍTULO XXVI
PESQUISA CLÍNICA
SEÇÃO I
DO PRODUTO OBJETO DA PESQUISA CLÍNICA
1 - A importação para fins de pesquisa clínica de bens ou produtos pertencentes às classes de medicamentos (incluídos os produtos destinados às intervenções dietéticas que não integram a classe de alimentos passíveis de registro), produtos médicos ou produtos para diagnóstico in vitro deverá submeter-se à autorização de embarque no exterior no Licenciamento de Importação, junto ao SISCOMEX, mediante a apresentação de formulário apropriado disposto em legislação pertinente. (Revogado pela Resolução - RDC nº 09, de 20 de fevereiro de 2015) (Revogado pela Resolução - RDC nº 10, de 20 de fevereiro de 2015)
1.1. A solicitação inicial para autorização de embarque do Licenciamento de Importação (LI) deverá ser protocolizada na ANVISA, em sua sede, devendo cumprir as demais determinações sanitárias vigentes. Para as autorizações de embarque subseqüentes, a aprovação do LI ocorrerá no local do desembaraço dos produtos; Essas
avaliações serão baseadas e respaldadas pela autorização de embarque inicial concedida pela área técnica competente, conforme disposto em legislação pertinente. (Revogado pela Resolução - RDC nº 09, de 20 de fevereiro de 2015) (Revogado pela Resolução - RDC nº 10, de 20 de fevereiro de 2015)
1.2. O deferimento do Licenciamento de Importação e a liberação sanitária de bens ou produtos dar-se-ão pela autoridade sanitária competente em exercício no local de desembaraço do produto, mediante o cumprimento do disposto neste Regulamento, bem como o atendimento às indicações de rotulagem e embalagem, transporte e armazenagem, de acordo com a regulamentação do produto perante a ANVISA, ou, subsidiariamente, aquelas fornecidas pelo fabricante.
1.2.1 Para os medicamentos importados produzidos por outro fabricante que não o importador ou patrocinador do estudo clínico o certificado de análise do produto acabado poderá ser substituído por:
a) cópia da nota fiscal de compra do medicamento, especificando todos os lotes; e
b) declaração, contendo número dos lotes, nome do princípio ativo e nome comercial dos medicamentos conforme são comercializados no mercado estrangeiro, assinada pelo responsável técnico.
1.2.2. Além do disposto no subitem anterior, deverão ser apresentados, após a chegada do produto no território nacional, os seguintes documentos:
a) cópia do Comunicado Especial - CE, emitido pela área técnica competente da ANVISA em sua sede;
b) conhecimento de carga embarcada -AWB, BL ou CTR;
c) autorização de acesso para inspeção, de acordo com a regulamentação fiscal pertinente, quando couber;
d) fatura comercial.
SEÇÃO II
DOS PRODUTOS MÉDICOS E PRODUTOS PARA DIAGNÓSTICO IN VITRO IMPORTADOS PARA O ACOMPANHAMENTO OU AVALIAÇÃO DE PESQUISA CLÍNICA
2. A importação de bens e produtos sob vigilância sanitária pertencentes às classes de produtos médicos e produtos para diagnóstico in vitro vinculado ao acompanhamento e avaliação do desenvolvimento de pesquisa clínica aprovada deverá submeter-se à autorização de embarque em licenciamento de importação - LI pela área técnica competente da ANVISA em sua sede, mediante a apresentação de formulário apropriado disposto em legislação pertinente. (Revogado pela Resolução - RDC nº 10, de 20 de fevereiro de 2015)
2.1. A solicitação inicial para autorização de embarque do Licenciamento de Importação - LI, deverá ser protocolizada na ANVISA, em sua sede, devendo cumprir as demais determinações sanitárias vigentes. (Revogado pela Resolução - RDC nº 10, de 20 de fevereiro de 2015)
2.1.1. Para as autorizações de embarque subseqüentes, a aprovação do LI ocorrerá no local do desembaraço dos produtos, e serão baseadas e respaldadas pela autorização de embarque inicial concedida pela área técnica competente, conforme disposto em legislação pertinente. (Revogado pela Resolução - RDC nº 10, de 20 de fevereiro de 2015)
2.2. O deferimento do Licenciamento de Importação, junto ao SISCOMEX, dar se-á mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2 perante a autoridade sanitária em exercício no local de desembaraço e ao atendimento às indicações de rotulagem e embalagem, transporte e armazenagem, de acordo com a regulamentação do produto perante a ANVISA, ou, subsidiariamente, aquelas fornecidas pelo fabricante.
SEÇÃO III
DOS KITS PARA COLETA DE MATERIAL BIOLÓGICO VINCULADOS AO ACOMPANHAMENTO OU AVALIAÇÃO DE PESQUISA CLÍNICA
3. A importação de kits para coleta de material biológico, vinculada ao acompanhamento e a avaliação do desenvolvimento de pesquisa clinica aprovada deverá submeter-se à fiscalização pela autoridade sanitária competente em exercício no local de seu desembaraço, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, instruída por Termo de Responsabilidade constante do Capítulo XXVII, deste Regulamento, apresentado com reconhecimento de firma em cartório e acompanhados dos seguintes documentos:
a) conhecimento de carga embarcada - AWB, BL ou CTR;
b) autorização de acesso para inspeção, de acordo com a regulamentação fiscal pertinente, quando couber;
c) fatura comercial.
d) cópia do Comunicado Especial - CE, emitido pela área técnica competente da ANVISA em sua sede;
3.1. A importação de que trata esta Seção dar-se-á por meio do SISCOMEX , Remessa Expressa ou Remessa Postal e estará desobrigada de autorização de embarque no exterior.
4. Serão vedadas a comercialização e alteração da finalidade informada no procedimento a que se destina a importação de que trata esta Seção.
5. O deferimento do Licenciamento de Importação e a liberação sanitária de bens ou produtos dar-se-ão pela autoridade sanitária competente em exercício no local de desembaraço mediante o cumprimento do disposto neste Regulamento, bem como o atendimento às indicações de rotulagem e embalagem, transporte e armazenagem, de acordo com a regulamentação do produto perante a ANVISA, ou, subsidiariamente, aquelas fornecidas pelo fabricante.
6. Os bens ou produtos de que tratam esta Seção estarão desobrigadas de regularização perante a ANVISA.
SEÇÃO IV
DO MATERIAL BIOLÓGICO HUMANO VINCULADO À PESQUISA CLÍNICA EM DESENVOLVIMENTO NO EXTERIOR, DESTINADO A DIAGNÓSTICO LABORATORIAL CLÍNICO
7. A importação de material biológico humano vinculado ao acompanhamento e avaliação do desenvolvimento de pesquisa, destinada a diagnóstico laboratorial clínico deverá submeter-se à fiscalização pela autoridade sanitária competente em exercício no local de desembaraço do produto, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, instruída por Termo de Responsabilidade constante do Capítulo XXVII, deste Regulamento, apresentado com reconhecimento de firma em cartório e acompanhados dos seguintes documentos:
a) conhecimento de carga embarcada - AWB, BL ou CTR;
b) autorização de acesso para inspeção, de acordo com a regulamentação fiscal pertinente;
c) fatura comercial.
7.1. A importação de bens e produtos de que trata esta Seção dar-se-á por meio do SISCOMEX, Remessa Expressa ou Remessa Postal.
7.2. A importação do bem ou produto de que trata esta Seção estará desobrigada de autorização de embarque no exterior.
8. Serão vedadas a comercialização e alteração da finalidade informada no procedimento a que se destina a importação de que trata esta Seção.
9. O deferimento do Licenciamento de Importação e/ou liberação sanitária do material dar-se-ão pela autoridade sanitária competente em exercício no local de desembaraço mediante o cumprimento do disposto neste Regulamento, bem como o atendimento às indicações de rotulagem e embalagem, transporte e armazenagem, de acordo com as informações indicadas pelo exportador do material.
SEÇÃO V
DAS DISPOSIÇÕES FINAIS
10. As importações de que trata este Capítulo estarão sujeitas a inspeção física, a critério da autoridade sanitária.
11. Nas embalagens secundárias e externas utilizadas para a movimentação e transporte dos materiais de que trata este Capítulo deverão constar:
a) o número do protocolo clínico ao qual o bem ou produto está submetido à pesquisa clínica de que trata a Seção I;
b) quantidade de material importado;
c) as informações sobre cuidados especiais para armazenagem, como temperatura, umidade, luminosidade;
d) as informações sobre forma física ou forma farmacêutica referentes à apresentação do produto, de que trata a Seção I;
12. Será vedada a entrada no território nacional de materiais não regularizados perante a ANVISA, para fins de pesquisa clínica, sem a prévia aprovação da autoridade sanitária competente.
CAPÍTULO XXVI
PESQUISA CLÍNICA
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) SEÇÃO I
DO PRODUTO OBJETO DA PESQUISA CLÍNICA
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1. A importação de produtos pertencentes às classes de medicamentos, produtos médicos ou produtos para diagnóstico in vitro sob investigação, para uso exclusivo em pesquisa clínica, deverá submeter-se a análise e deferimento do Licenciamento de Importação pela autoridade sanitária, mediante apresentação de Petição para Fiscalização e Liberação Sanitária, junto ao SISCOMEX. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1.1 O importador deve informar na descrição do produto o número do Comunicado Especial (CE) ou Comunicado Especial Específico (CEE) ou Documento para Importação de Produto(s) sob investigação do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) ou Dossiê de Investigação Clínica de Dispositivo Médico (DICD), emitido pela área técnica competente da Anvisa em sua sede. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1.2. Constituem documentos obrigatórios para instrução do processo de importação de que trata esta Seção: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Conhecimento de carga embarcada; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Fatura comercial; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Nos casos de importações realizadas por outros que não o detentor do DDCM ou DICD, documento de delegação de responsabilidades de importação. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2. É vedada a entrada no território nacional de produtos sob investigação não previstos no CE, CEE ou Documento para Importação de Produto sob investigação do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) ou Dossiê de Investigação Clínica de Dispositivo Médico (DICD). (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3. É vedada a alteração de finalidade de importação dos bens e produtos de que trata esta Seção. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO II
DOS PRODUTOS MÉDICOS E PRODUTOS PARA DIAGNÓSTICO IN VITRO IMPORTADOS PARA O ACOMPANHAMENTO OU AVALIAÇÃO DE PESQUISA CLÍNICA
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
4. A importação de bens e produtos sob vigilância sanitária pertencentes às classes de produtos médicos e produtos para diagnóstico in vitro, vinculada ao acompanhamento e à avaliação do desenvolvimento de pesquisa clínica aprovada, dar se-á mediante a apresentação de Petição para Fiscalização e Liberação Sanitária, prevista no Capítulo II, subitem 1.2 e o atendimento às indicações de rotulagem, embalagem, transporte e armazenagem. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO III
DOS KITS PARA COLETA DE MATERIAL BIOLÓGICO VINCULADOS AO ACOMPANHAMENTO OU AVALIAÇÃO DE PESQUISA CLÍNICA
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5. A importação de kits para coleta de material biológico, vinculada ao acompanhamento e à avaliação do desenvolvimento de pesquisa clínica aprovada, deverá submeter-se à fiscalização pela autoridade sanitária, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária, prevista no Capítulo II, subitem 1.2, a qual deverá ser instruída por Termo de Responsabilidade, constante do Capítulo XXVII desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5.1 O importador deve informar, na descrição do produto, o número do Comunicado Especial (CE) ou Comunicado Especial Específico (CEE) ou Documento para Importação de Produto(s) sob investigação do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) ou Dossiê de Investigação Clínica de Dispositivo Médico (DICD), emitido pela área técnica competente da Anvisa em sua sede. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5.2. São documentos obrigatórios para instrução do processo de importação de que trata esta Seção: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Conhecimento de carga embarcada; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Fatura comercial; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Nos casos de importações realizadas por outros que não o detentor do DDCM ou DICD, documento de delegação de responsabilidades de importação. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5.3. A importação de que trata esta Seção dar-se-á por meio do SISCOMEX, Remessa Expressa ou Remessa Postal e estará desobrigada de autorização de embarque no exterior. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
6. É vedada a comercialização dos produtos de que trata esta Seção, bem como a alteração da finalidade a que se destina a importação, informada no procedimento de importação. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
7. Os bens ou produtos de que trata esta Seção estão desobrigados de regularização perante a ANVISA. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO IV
DO MATERIAL BIOLÓGICO HUMANO VINCULADO A PESQUISA CLÍNICA EM DESENVOLVIMENTO NO EXTERIOR, DESTINADO A DIAGNÓSTICO LABORATORIAL CLÍNICO
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
8. A importação de material biológico humano, vinculada ao acompanhamento e avaliação do desenvolvimento de pesquisa, destinada a diagnóstico laboratorial clínico, deverá submeter-se à fiscalização pela autoridade sanitária, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária, prevista no Capítulo II, subitem 1.2, a qual deverá ser instruída por Termo de Responsabilidade, constante do Capítulo XXVII desta Resolução, acompanhados dos seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Declaração do Importador com a informação do número do Comunicado Especial (CE) ou Comunicado Especial Específico (CEE); (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Conhecimento de carga embarcada; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Fatura comercial. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
8.1. A importação de bens e produtos de que trata esta Seção dar-se-á por meio do SISCOMEX, Remessa Expressa ou Remessa Postal. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
8.2. A importação de bem ou produto de que trata esta Seção está desobrigada de autorização de embarque no exterior. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
9. É vedada a comercialização dos produtos de que trata esta Seção, bem como a alteração da finalidade a que se destina a importação, informada no procedimento de importação. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
10. O deferimento do Licenciamento de Importação ou a liberação sanitária do material se dará mediante o cumprimento do disposto nesta Resolução, bem como o atendimento às indicações de rotulagem e embalagem, transporte e armazenagem, de acordo com as informações indicadas pelo exportador do material e regulamentadas por normas nacionais e internacionais de transporte. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO V
DAS DISPOSIÇÕES FINAIS
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
11. As importações de que trata este Capítulo estarão sujeitas a inspeção física, a critério da autoridade sanitária. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
12. Nas embalagens secundárias e externas utilizadas para a movimentação e transporte dos materiais de que trata este Capítulo deverão constar: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Número do protocolo clínico da pesquisa à qual o produto está submetido; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) informações sobre cuidados para armazenamento, como temperatura, umidade e luminosidade; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) número de lote ou código de identificação ou número de série que permitam a rastreabilidade do produto importado. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
12.1 Medicamentos importados apenas em embalagem primária e contendo QR Code ou outro identificador devem contemplar os requisitos mínimos descritos nas alíneas a e b, em suas embalagens externas ou de transporte. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
12.2 As informações vinculadas ao QR Code ou a outro identificador devem permitir a completa rastreabilidade do produto junto ao centro de pesquisa. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
CAPÍTULO XXVII

CAPÍTULO XXVIII
SITUAÇÕES ADUANEIRAS ESPECIAIS
SEÇÃO I
DO TRÂNSITO ADUANEIRO
1. A importação de bens e produtos sob licenciamento não automático junto ao SISCOMEX, sujeitas a regime de trânsito aduaneiro por meio do Manifesto Internacional de Carga e Despacho de Trânsito Aduaneiro - MIC/DTA -, Despacho de Trânsito Aduaneiro - DTA - e Despacho de Trânsito Aduaneiro Simplificado - DTA-S, estão dispensadas de anuência ou autorização perante a ANVISA.
1.1. Excetuar-se-á do disposto neste item a importação de bens e produtos perecíveis ou que necessitem de armazenagem especial, que deverão ter a autorização para o trânsito aduaneiro concedida pela autoridade sanitária, no local de entrada no território nacional. (Exigência suspensa pela Resolução - RDC nº 48, de 31 de agosto de 2012)
1.2. Excetuar-se-á do disposto neste item à importação destinada a Regime de Entreposto Aduaneiro, Loja Franca e ao consumo de bordo de veículos terrestres que operarem transporte coletivo internacional de passageiros, aeronaves e embarcações de bandeira estrangeira em trânsito ou sob afretamento de empresa brasileira.
1.3. O deferimento em Licenciamento de Importação ou em documento aduaneiro apropriado, e a liberação sanitária de produtos sujeitos ao regime de trânsito aduaneiro dar-se-ão pela autoridade sanitária competente em exercício no local onde ocorrerá o desembaraço aduaneiro.
2. Será vedada a aplicação de regime de trânsito aduaneiro à importação de bens e produtos pertencentes às seguintes classes e categorias:
a) substâncias e medicamentos sujeitos a controle especial, constantes dos Procedimentos 1 e 1-A, do Capítulo XXXIX, deste Regulamento;
b) células e tecidos humanos para fins terapêuticos;
c) medicamentos a granel, semi-elaborados ou acabados pertencentes às categorias de hemoderivados e biológicos, e as matérias-primas que os integram, constantes dos Procedimentos 2, 2-A, 2-B, 2-C e 5.3, do Capítulo XXXIX, deste Regulamento;
d) produtos acabados pertencentes às classes de medicamentos, alimentos e produtos médicos, quando destinados à pesquisa clínica;
e) Talidomida e medicamentos à base desse princípio ativo.
2.1. Excetuar-se-ão do disposto as alíneas "b" e "c" deste item às importações destinadas a programas públicos de saúde, vinculadas ao Ministério da Saúde, e Secretarias Estaduais e Municipais.
2.2. Excluir-se-á do disposto na alínea "d" a importação de bens e produtos pertencentes à classe de produtos médicos vinculadas ao acompanhamento e avaliação de desenvolvimento de pesquisa clínica.
3. Será vedado o trânsito aduaneiro de bens ou produtos sob suspeita de comprometimento do padrão de identidade e qualidade, ou em situações emergenciais e provisórias por medidas relacionadas ao contexto sanitário e epidemiológico internacional.
3.1. Para os fins deste item, a critério da autoridade sanitária ou no cumprimento de medida emergencial e provisória, o bem ou material será submetido à fiscalização no local de entrada no país.
SEÇÃO II
DA ADMISSÃO TEMPORÁRIA
4. A importação de bens ou produtos sob vigilância sanitária e sujeito a licenciamento não automático no SISCOMEX, em Regime Aduaneiro Especial de Admissão Temporária, deverá atender as formalidades de requerimento e tramitação, de acordo com o disposto no Capítulo XXXIX deste Regulamento.
5. O importador deverá requerer autorização de embarque à autoridade sanitária por meio de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, instruída pelas seguintes informações complementares às demais integrantes deste Regulamento:
a) nome do responsável técnico pelo bem ou produto durante o período de sua permanência no território nacional;
b) quantidade do bem ou produto;
c) prazo de validade ou data de vencimento do bem ou produto, no que couber; d) finalidade da importação;
e) prazo de permanência do produto no território nacional, com indicação da data de seu retorno ao exterior;
f) local de armazenagem ou exposição do produto no prazo sujeito à Admissão Temporária.
5.1. O importador deverá apresentar o respectivo comprovante de exportação à autoridade sanitária em exercício no local de desembaraço aduaneiro, no prazo máximo de 10 (dez) dias úteis a contar da remessa da mercadoria para o exterior.
5.2. A permanência do bem ou produto sob Regime Aduaneiro de Admissão Temporária em prazo superior ao indicado na alínea "e" do subitem anterior sujeitará o importador às sanções sanitárias cabíveis.
6. O deferimento da Licença de Importação e a Liberação Sanitária dar-se-ão pela autoridade sanitária da ANVISA, no local de desembaraço aduaneiro.
7. Fica autorizada, na forma deste Regulamento, para fins de Regime Aduaneiro Especial de Admissão Temporária, a importação de bens ou produtos relacionadas nos Procedimentos 4 e 5 do Capítulo XXXIX.
7.1. Excetuam-se deste item os alimentos.
8. Será vedado a nacionalização do bem ou produto admitido sob o Regime Aduaneiro Especial de Admissão Temporária que não atenda a legislação sanitária.
SEÇÃO III
DO ENTREPOSTO ADUANEIRO
9. A importação de bens ou produtos sob vigilância sanitária em Regime Especial de Entreposto Aduaneiro deverá ser comunicada pelo importador ou consignatário à autoridade sanitária em exercício no local de desembaraço aduaneiro, em prazo não superior a 5 (cinco) dias úteis a contar da permissão para esse regime, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2. e regularizada quanto a Autorização de Funcionamento para esta atividade.
9.1. O comunicado deverá ser instruído com o documento que autoriza o Regime Especial de Entreposto Aduaneiro, em sua forma original e cópia para autenticação, a qual ficará retida, devendo conter as seguintes informações:
a) nome comum ou nome técnico, químico ou biológico do bem ou produto, quando se tratar de matéria-prima;
b) nome da matéria-prima alimentícia, quando se tratar de alimentos;
c) nome comercial, quando se tratar de produto acabado ou a granel e produto pertencente à classe de medicamentos, também deverá ser informado o nome do princípio ativo base da formulação; para a classe de alimentos, a designação do produto e marca;
d) número ou código dos lotes ou partidas de produção dos bens ou produtos entrepostados;
e) prazo de validade por lote ou partida;
f) informação sobre a regularização do produto junto a ANVISA, se houver;
g) identificação da empresa a qual foi concedido o regime, com indicação do Cadastro Nacional de Pessoa Jurídica e endereço completo;
h) nome do fabricante;
i) informação sobre a regularização da empresa importadora na ANVISA se houver;
j) identificação do recinto alfandegado ou entreposto;
l) localização do bem ou produto no recinto alfandegado;
m) cuidados especiais para armazenagem e manutenção da identidade e qualidade do bem ou produto entrepostado, como temperatura, umidade, luminosidade, entre outros.
10. Em caso de retorno dos bens e produtos referentes a esta seção, o importador deverá comprovar a remessa ao exterior à autoridade sanitária em exercício no recinto alfandegado de armazenagem do produto, no prazo máximo de 5 (cinco) dias úteis a contar da emissão do documento aduaneiro.
10.1. A comprovação de que trata este item deverá ser efetivada pela apresentação do documento aduaneiro supracitado com cópia, a qual ficará retida.
11. Será vedada a aplicação de Regime Especial de Entreposto Aduaneiro à importação de bens e produtos pertencentes às seguintes classes e categorias:
a) substâncias e medicamentos sujeitos a controle especial, constantes dos Procedimentos 1 e 1-A, do Capítulo XXXIX, deste Regulamento;
b) células e tecidos humanos para fins terapêuticos;
c) medicamentos a granel, semi-elaborados ou acabados pertencentes às categorias de hemoderivados e biológicos, e as matérias-primas que os integram, constantes dos Procedimentos 2, 2-A, 2-B, 2-C e 5.3, do Capítulo XXXIX, deste Regulamento;
d) produtos acabados pertencentes às classes de medicamentos, alimentos e produtos médicos, quando destinados à pesquisa clínica;
e) talidomida e medicamentos à base desse princípio ativo, matérias-primas e produtos integrantes do Procedimento 6 do Capítulo XXXIX, deste Regulamento.
11.1. Excetuar-se-ão do disposto a alínea "c" deste item, as importações destinadas a programas públicos de saúde, vinculadas ao Ministério da Saúde e Secretarias Estaduais e Municipais.
11.2. Excluir-se-á do disposto na alínea "d" a importação dos bens ou produtos pertencentes às classes de produtos médicos vinculadas ao acompanhamento e avaliação de desenvolvimento de pesquisa clínica.
12. A nacionalização do bem ou produto importado sob permissão de Regime Especial de Entreposto Aduaneiro deverá submeter-se à fiscalização sanitária pela autoridade sanitária competente em exercício, no local onde ocorrerá o seu desembaraço, de acordo com os critérios do Capítulo XXXIX deste Regulamento.
SEÇÃO IV
DA ENTREGA FRACIONADA
13. A importação de bens ou produtos sob vigilância sanitária com entrega fracionada, satisfeitas as condições sanitárias, sujeitar-se-á a deferimento de Licenciamento de Importação com ressalva junto ao SISCOMEX pela autoridade sanitária em exercício no local de desembaraço aduaneiro, quando da chegada da primeira fração importada.
13.1. As importações fracionadas de que trata este item deverão ser comunicadas à autoridade sanitária em exercício no local de desembaraço aduaneiro de bens ou produtos, com antecedência mínima de 12 (doze) horas a contar da data e horário estimados para sua chegada.
13.2. A comunicação em prazo inferior ao indicado no subitem anterior sujeitará o importador às sanções sanitárias cabíveis.
13.3. A ressalva de que trata este item deverá ser registrada no campo referente à situação do Licenciamento de Importação no SISCOMEX com o seguinte texto: "PRODUTO SOB ENTREGA FRACIONADA. A LIBERAÇÃO À EXPOSIÇÃO OU ENTREGA AO CONSUMO DAS REMESSAS FRACIONADAS INTEGRANTES DESTE LICENCIAMENTO DE IMPORTAÇÃO DAR-SE-Á MEDIANTE FISCALIZAÇÃO SATISFATÓRIA DA AUTORIDADE SANITÁRIA EM EXERCÍCIO NO LOCAL DE DESEMBARAÇO".
14. A importação de que trata esta Seção deverá ser instruída com declaração do importador se responsabilizando por comunicar a entrada de cada fração de bens ou produtos do total indicado no Licenciamento de Importação, subscrita pelo representante legal da empresa, com reconhecimento de firma em cartório.
15. A liberação somente ocorrerá após fiscalização sanitária pela autoridade em exercício no local de desembaraço aduaneiro, na forma deste Regulamento.
SEÇÃO V
DO DEFERIMENTO ANTECIPADO DE LICENCIAMENTO DE IMPORTAÇÃO
16. O deferimento antecipado de Licenciamento de Importação junto ao SISCOMEX poderá ocorrer na importação de bens ou produtos perecíveis:
a) em caso de não oferta de ambiente armazenador em condições operacionais compatíveis às especificações do fabricante para fins de manutenção da segurança e integridade sanitária;
b) em caso de capacidade de armazenagem insuficiente.
c) na importação por órgãos e entidades da Administração Pública, direta e indireta, federal, estadual e municipal, inclusive empresas públicas e sociedades de economia mista.
16.1. O Licenciamento de Importação de que trata este item será deferido com ressalva pela autoridade sanitária em exercício no local de desembaraço aduaneiro.
16.2. A importação de que trata este item deverá ser comunicada à autoridade sanitária em exercício no local de desembaraço aduaneiro dos produtos, com antecedência mínima de 24 (vinte e quatro) horas a contar do horário estimado para sua chegada.
16.3. A comunicação em prazo inferior ao indicado no subitem anterior sujeitará o importador às sanções sanitárias cabíveis.
16.4. A ressalva de que trata o subitem 16.1. deverá ser registrada no campo referente à situação do Licenciamento de Importação no SISCOMEX com o seguinte texto: "DEFERIMENTO ANTECIPADO. A LIBERAÇÃO, A EXPOSIÇÃO OU ENTREGA PARA CONSUMO DOS BENS OU PRODUTOS INTEGRANTES DESTE LICENCIAMENTO DE IMPORTAÇÃO ESTARÁ SUJEITA À FISCALIZAÇÃO DA AUTORIDADE SANITÁRIA EM EXERCÍCIO NO LOCAL DE DESEMBARAÇO."
17. A liberação sanitária somente ocorrerá após inspeção física da importação, a critério da autoridade sanitária, em exercício no local de desembaraço aduaneiro, na forma deste Regulamento.
17.1. No caso de exposição ao consumo sem a liberação pela autoridade sanitária, dos produtos sob deferimento antecipado, será o importador responsabilizado e sujeito às penalidades da legislação vigente.
18. O importador poderá solicitar prorrogação do prazo de vigência do Licenciamento de Importação pelo prazo de 90 (noventa) dias a contar da expiração do seu prazo de validade.
CAPÍTULO XXVIII
SITUAÇÕES ADUANEIRAS ESPECIAIS
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) SEÇÃO I
DO TRÂNSITO ADUANEIRO
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1. O regime de trânsito aduaneiro por meio do Manifesto Internacional de Carga e Despacho de Trânsito Aduaneiro (MIC/DTA), Despacho de Trânsito Aduaneiro (DTA), Conhecimento-Carta de Porte Internacional - Declaração de Trânsito Aduaneiro (TIF-DTA), Declaração de Trânsito de Transferência (DTT) ou Declaração de Trânsito de Contêiner (DTC) está dispensado de anuência ou autorização perante a ANVISA.
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2. É vedada a aplicação de regime de trânsito aduaneiro na importação de bens e produtos pertencentes às seguintes classes e categorias: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) substâncias e medicamentos sujeitos a controle especial, constantes dos Procedimentos 1 e 1A do Capítulo XXXIX desta Resolução; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Talidomida e medicamentos à base desse princípio ativo; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) células e tecidos humanos para fins terapêuticos; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) bens ou produtos sob suspeita de comprometimento do padrão de identidade e qualidade, ou em situações emergenciais e provisórias, por medidas relacionadas ao contexto sanitário e epidemiológico internacional. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.1. Para a situação descrita na alínea “d” do item 2 desta Seção, a critério da autoridade sanitária, o bem ou material poderá, a qualquer tempo, ser submetido a fiscalização. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO II
DA ADMISSÃO TEMPORÁRIA
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3. A importação de bens ou produtos sob vigilância sanitária e sujeitos a licenciamento não automático no SISCOMEX, em Regime Aduaneiro Especial de Admissão Temporária, deverá atender as formalidades de requerimento e tramitação, de acordo com o disposto no Capítulo XXXIX desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
4. O importador deverá apresentar as seguintes informações complementares às demais integrantes desta Resolução: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) nome do responsável técnico pelo bem ou produto durante o período de sua permanência no território nacional; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) quantidade do bem ou produto; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) prazo de validade ou data de vencimento do bem ou produto; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) finalidade da importação; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e) prazo de permanência do produto no território nacional, com indicação da data de seu retorno ao exterior; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
f) local de armazenagem ou exposição do produto no prazo sujeito à Admissão Temporária. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
4.1. O importador deverá apresentar o respectivo comprovante de exportação no prazo máximo de 10 (dez) dias úteis a contar da remessa da mercadoria para o exterior. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5. É vedada a nacionalização do bem ou produto admitido sob o Regime Aduaneiro Especial de Admissão Temporária que não atenda à legislação sanitária vigente. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO III
ENTREPOSTO ADUANEIRO
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
6. É vedada a aplicação de Regime Especial de Entreposto Aduaneiro à importação de bens e produtos pertencentes às seguintes classes e categorias: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) substâncias e medicamentos sujeitos a controle especial, constantes dos Procedimentos 1 e 1-A, do Capítulo XXXIX, desta Resolução; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) células e tecidos humanos para fins terapêuticos; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) medicamentos a granel, semielaborados ou acabados pertencentes às categorias de hemoderivados e biológicos, e as matérias-primas que os integram, constantes dos Procedimentos 2, 2-A, 2-B e 2-C, do Capítulo XXXIX desta Resolução; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) talidomida e medicamentos à base desse princípio ativo. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
6.1. Excetuar-se-ão do disposto a alínea “c” do item 7 desta Seção, as importações destinadas a programas públicos de saúde, vinculadas ao Ministério da Saúde e Secretarias Estaduais e Municipais. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
7. A nacionalização do bem ou produto importado sob permissão de Regime Especial de Entreposto Aduaneiro deverá submeter-se a fiscalização sanitária, de acordo com os critérios do Capítulo XXXIX desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO IV
DA ENTREGA FRACIONADA
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
8. A importação de bens ou produtos sob vigilância sanitária com entrega fracionada, satisfeitas as condições sanitárias, sujeitar-se-á a deferimento de Licenciamento de Importação com ressalva junto ao SISCOMEX, pela autoridade sanitária, quando da chegada da primeira fração importada. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
8.1. As importações fracionadas de que trata o item 9 desta Seção deverão ser comunicadas à autoridade sanitária com antecedência mínima de 12 (doze) horas a contar da data e horário estimados para sua chegada. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
8.2. A comunicação em prazo inferior ao indicado no subitem 9.1 desta Seção sujeitará o importador às sanções sanitárias cabíveis. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
8.3. A ressalva de que trata o item 9 desta Seção deverá ser registrada no campo referente à situação do Licenciamento de Importação no SISCOMEX, com o seguinte texto: “PRODUTO SOB ENTREGA FRACIONADA. A LIBERAÇÃO À EXPOSIÇÃO OU ENTREGA AO CONSUMO DAS REMESSAS FRACIONADAS INTEGRANTES DESTE LICENCIAMENTO DE IMPORTAÇÃO DAR-SE-Á MEDIANTE FISCALIZAÇÃO SATISFATÓRIA DA AUTORIDADE SANITÁRIA”.
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
9. A importação de que trata esta Seção deverá ser instruída com declaração do importador responsabilizando-se por comunicar a entrada de cada fração do total de bens ou produtos indicados no Licenciamento de Importação, subscrita pelo representante legal da empresa. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO V
CARNÊ ATA
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
10. O regime aduaneiro de admissão temporária de bens transportados ao amparo de Carnê ATA, previsto no Decreto nº. 7.545, de 02 de agosto de 2011, que promulga a Convenção de Istambul, será aplicado conforme disposto nesta Seção. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
11.Poderão ser submetidos ao regime de que trata esta Seção, nos termos estabelecidos nos Anexos B.1, B.5 e B.6 do Decreto nº. 7.545, de 02 de agosto de 2011, os seguintes bens e produtos sob regime de vigilância sanitária: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Bens e produtos sujeitos ao regime de vigilância sanitária destinados à exposição, feira, congresso ou evento similar; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Produtos para saúde e produtos para diagnóstico in vitro destinados a fins educacionais, científicos ou culturais; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Bens e produtos sujeitos ao regime de vigilância sanitária para fins desportivos, desde que a quantidade seja compatível com o uso pessoal. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
12. A fiscalização e liberação pela autoridade sanitária de bens transportados ao amparo do Decreto nº. 7.545, de 02 de agosto de 2011 serão efetuadas com base exclusivamente no que constitui o Carnê ATA. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) O Carnê ATA deverá ser apresentado pelo importador ou seu representante à autoridade sanitária no local de desembaraço; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) A verificação física da mercadoria somente será realizada quando a autoridade sanitária entender que esse procedimento é necessário; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) verificado o cumprimento das condições sanitárias para a concessão do regime, a autoridade sanitária efetuará a aposição de carimbo e assinatura se existente campo apropriado no voucher de entrada que compõe o Carnê ATA, considerando o bem pronto para ser entregue ao seu beneficiário. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
13. Poderá submeter-se também ao regime do Carnê ATA o ingresso no território nacional de equipamentos médicos não regularizados na ANVISA, destinados à exposição em feiras, congressos ou evento similar. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
13.1 O equipamento médico de que trata este item, durante a sua permanência no território nacional, deverá estar sob a assistência de profissional responsável técnico, e a formação profissional do responsável técnico deve atender as exigências constantes na legislação sanitária vigente pertinente. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
14. Considera-se beneficiário do regime a pessoa física ou jurídica que conste no Carnê ATA como titular. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
15. O beneficiário poderá trazer ao país apenas parte dos bens descritos na Lista Geral constante no Carnê ATA. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
16. A manifestação da autoridade sanitária produzirá efeitos sobre a totalidade dos bens de interesse sanitário descritos na Lista Geral do Carnê ATA. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
17. Não poderão ser admitidos ou mantidos no regime de que trata esta Seção bens que, durante sua permanência no país: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) estejam sujeitos a sofrer ou sofram qualquer alteração, com exceção da depreciação normal resultante de sua utilização; ou (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) estejam sujeitos a ser consumidos. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
18. É vedada a importação de materiais profissionais, com finalidade sujeita à vigilância sanitária, sob o regime desta Seção. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO VI
LOJA FRANCA
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
19. A importação para exposição à venda ou entrega ao consumo de bens ou produtos sob vigilância sanitária em Lojas Francas, deve obedecer às exigências sanitárias pertinentes, incluindo: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Condições de uso e consumo descritas pelo fabricante; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Prazo de validade, se existente na embalagem; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Armazenagem em ambiente adequado, de modo a garantir e manter seu padrão de identidade e qualidade. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
20.Os produtos em exposição em Lojas Francas não possuem obrigatoriedade de regularização formal junto ao SNVS. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
21. O bem ou produto exposto à venda ou entregue ao consumo em Loja Franca poderá sujeitar-se a análise fiscal ou de controle, na forma desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
22. Será obrigatório em Lojas Francas a manutenção das informações dos bens ou produtos sob vigilância sanitária, por classe, nome comercial, quantidade, número do lote ou partida, nome do fabricante e identificação do comprador, pelo prazo de 5 (cinco) anos a contar da data de sua entrega à venda ou sua exposição ao consumo.
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018) CAPÍTULO XXIX
LOJA FRANCA
(Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1. A exposição à venda ou entrega ao consumo de bens ou produtos importados em Lojas Francas, bem como aquelas oferecidas em vôos internacionais por empresas aéreas nacionais, sujeitar-se-ão, no que couber, às exigências sanitárias pertinentes. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1.1. Incluir-se-á no disposto neste item, em especial: (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) prazo de validade e condições de uso e consumo dos bens ou produtos que não ofereçam risco ou dano à saúde; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) exposição dos bens ou produtos em ambiente adequado de modo a garantir e manter seu padrão de identidade e qualidade; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) obrigatoriedade da empresa que comercializar produtos nas áreas de portos, aeroportos e fronteiras de Autorização de Funcionamento para a atividade de importar; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) obrigatoriedade da empresa que armazenar bens ou produtos para suprir Lojas Francas em áreas de portos, aeroportos e fronteiras de Autorização de Funcionamento para a atividade de armazenar, bem como de cumprir a legislação sanitária pertinente quanto às Boas Práticas de Armazenagem. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1.2. Excluir-se-á do disposto neste item o registro ou regularização formal do produto no Sistema Nacional de Vigilância Sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2. O bem ou produto exposto à venda ou entregue ao consumo em Loja Franca poderá sujeitar-se à análise fiscal ou de controle, na forma deste Regulamento. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3. Será obrigatório em Lojas Francas manter informações dos bens ou produtos sob vigilância sanitária por classe, nome comercial, quantidade, número do lote ou partida, nome do fabricante e identificação do comprador, pelo prazo de 5 (cinco) anos a contar da data de sua entrega à venda ou sua exposição ao consumo. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
CAPÍTULO XXX
PRODUTOS DESTINADOS A ABASTECIMENTO INICIAL E REPOSIÇÃO DE ENFERMARIA, FARMÁCIA OU CONJUNTO MÉDICO DE BORDO OU A PRESTAÇÃO DE SERVIÇOS INTERNOS DE VEÍCULOS TERRESTRES QUE OPEREM TRANSPORTE COLETIVO INTERNACIONAL DE PASSAGEIROS, OU DE EMBARCAÇÕES E AERONAVES
SEÇÃO I
DOS MEDICAMENTOS, PRODUTOS MÉDICOS E PRODUTOS PARA DIAGNÓSTICO IN VITRO
1. A importação de produtos pertencentes às classes de medicamentos, produtos médicos e produtos para diagnóstico in vitro destinada a abastecimento inicial e reposição de enfermaria, farmácia ou conjunto médico de bordo de veículos terrestres que operem transporte coletivo internacional de passageiros, ou de embarcações e aeronaves, deverá sujeitar-se à manifestação expressa e favorável da autoridade sanitária competente.
1.2. Somente poderão ser importadas para os fins do disposto nesta seção bens ou produtos na forma de produto acabado.
2. A liberação sanitária somente ocorrerá após fiscalização dos bens ou produtos importadas pela autoridade sanitária em exercício no local de desembaraço aduaneiro, na forma deste Regulamento. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3. A importação de produtos pertencentes às classes de medicamentos que contenham substância entorpecente ou psicotrópica, integrantes da Portaria SVS/MS nº 344, de 1998, somente poderá ter seu desembaraço aduaneiro nos pontos de entrada e desembaraço no território nacional autorizados para essa finalidade, de acordo com a legislação sanitária pertinente.
4. Os produtos de que tratam esta Seção ficarão isentos de registro ou regularização formal no Sistema Nacional de Vigilância Sanitária, não se eximindo do cumprimento de outras exigências sanitárias cabíveis.
4.1. A critério da autoridade sanitária, os produtos de que tratam este Capítulo sujeitar-se-ão a análise fiscal e de controle, na forma deste Regulamento.
5. Serão vedadas a comercialização e alteração de finalidade informada no procedimento a que se destina a importação de que trata esta Seção.
SEÇÃO II
DOS ALIMENTOS, SANEANTES, PRODUTOS DE HIGIENE PESSOAL, PERFUMES E COSMÉTICOS DESTINADOS AO CONSUMO INTERNO OU A PRESTAÇÃO DE SERVIÇOS
6. A importação de produtos pertencentes às classes de produtos de higiene pessoal, saneantes ou alimentos, destinados ao consumo ou a prestação de serviços de bordo em embarcações, aeronaves e veículos terrestres que operem transporte coletivo internacional de passageiros, deverá submeter-se à fiscalização da ANVISA pela autoridade competente no local de desembaraço, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no subitem 1.2. do Capítulo II.
6. A importação de produtos pertencentes às classes de produtos de higiene pessoal, saneantes ou alimentos, destinados ao consumo ou a prestação de serviços de bordo em embarcações, aeronaves e veículos terrestres que operem transporte coletivo internacional de passageiros, deverá submeter-se à fiscalização da ANVISA, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no subitem 1.2 do Capítulo II desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
6.1. A petição de que trata este item deverá ser instruída pelo competente documento de registro de ingresso no território nacional e por documento assinado pelo representante legal do importador, contendo as seguintes informações:
a) nome da empresa de transporte;
b) país de bandeira da embarcação ou país ao qual esteja vinculada a empresa aérea ou terrestre;
c) nome do porto ou do aeroporto instalado no território nacional onde ocorrerá o abastecimento;
d) identificação do meio de transporte destinatário do produto, nome ou prefixo;
e) declaração de não utilização dos bens ou produtos para finalidade diversa da indicada para a importação.
6.2. O documento declaratório com as informações enumeradas no subitem anterior deverá apresentar-se com reconhecimento de firma em cartório. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
7. A importação de que trata esta Seção estará desobrigada de autorização de embarque no exterior.
SEÇÃO III
DA EMBARCAÇÃO DE BANDEIRA BRASILEIRA, EMBARCAÇÃO DE BANDEIRA ESTRANGEIRA SOB AFRETAMENTO OU ARRENDAMENTO DE EMPRESA BRASILEIRA E AERONAVE INTEGRANTE DA FROTA AÉREA DE EMPRESA BRASILEIRA
8. A importação de produtos pertencentes à classe de medicamentos, produtos médico e produtos pra diagnostico in vitro, não regularizados junto ao Sistema Nacional de Vigilância Sanitária-SNVS, na forma esta Seção, para abastecimento e reposição de embarcação de bandeira brasileira, embarcação de bandeira estrangeira sob afretamento ou arrendamento de empresa brasileira e de aeronave integrante da frota aérea de empresa brasileira, deverá submeter-se a parecer prévio, conclusivo e satisfatório, da área técnica competente da ANVISA, em sua sede, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no subitem 1.2. do Capítulo II.
8.1. A importação de que trata esta Seção dar-se-á exclusivamente por meio do Siscomex.
9. A importação de que trata esta Seção estará desobrigada da autorização de embarque no exterior.
9.1. Excluir-se-ão do disposto no item anterior a importação de produtos pertencentes às classes de medicamentos integrantes dos Procedimentos nº 1, nº 1-A, nº 2, nº 2-A, 2-B, 2-C e nº 3, do Capítulo XXXIX deste Regulamento.
SEÇÃO IV
DA EMBARCAÇÃO E AERONAVE DE BANDEIRA ESTRANGEIRA OU VEÍCULO TERRESTRE INTEGRANTE DA FROTA DE EMPRESA ESTRANGEIRA, QUE OPEREM TRANSPORTE COLETIVO INTERNACIONAL DE PASSAGEIROS, EM TRÂNSITO PELO TERRITÓRIO NACIONAL
10. A importação de produtos pertencentes à classe de medicamentos, produtos médicos e produtos pra diagnostico in vitro, para abastecimento e reposição de veículo terrestre integrante de frota de empresa estrangeira, que opere transporte coletivo internacional de passageiros, ou de embarcação ou aeronave de bandeira estrangeira, deverá submeter-se à fiscalização da ANVISA pela autoridade competente no local de desembaraço mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no subitem 1.2. do Capítulo II.
10. A importação de produtos pertencentes às classes de medicamentos, produtos médicos e produtos para diagnostico in vitro, para abastecimento e reposição de veículo terrestre integrante de frota de empresa estrangeira que opere transporte coletivo internacional de passageiros, ou de embarcação ou aeronave de bandeira estrangeira, deverá submeter-se à fiscalização da ANVISA, mediante a apresentação de Petição para Fiscalização e Liberação Sanitária prevista no subitem 1.2. do Capítulo II desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
10.1. A petição de que trata este item deverá ser instruída pelo competente documento de registro de ingresso no território nacional e por documento assinado pelo representante legal do importador, contendo as seguintes informações:
a) nome da empresa de transporte;
b) país de bandeira da embarcação ou país ao qual esteja vinculada a empresa aérea ou terrestre;
c) nome do porto ou do aeroporto instalado no território nacional onde ocorrerá o abastecimento;
d) identificação do meio de transporte destinatário do produto, nome ou prefixo;
e) declaração de não utilização dos produtos para finalidade diversa da indicada para a importação.
10.2. O documento declaratório com as informações enumeradas no subitem anterior deverá apresentar-se com reconhecimento de firma em cartório. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
11. Excluir-se-ão do disposto no item anterior a importação de medicamentos que integrem os Procedimentos 1, 1-A e 3, do Capítulo XXXIX deste Regulamento que deverá submeter-se a parecer prévio, conclusivo e satisfatório da área técnica competente da ANVISA, em sua sede.
11.1. A importação dos medicamentos entorpecentes, psicotrópicos e aqueles que contenham substâncias precursoras em sua composição, de que trata a Portaria SVS/MS nº 344, de 1998 e suas alterações, dar-se-á conforme legislação vigente.
CAPÍTULO XXXI
TRANSPORTE, MOVIMENTAÇÃO E ARMAZENAGEM DE BENS E PRODUTOS IMPORTADOS
SEÇÃO I
DAS DISPOSIÇÕES GERAIS
1. O transporte, movimentação e armazenagem dos bens ou produtos importados sob vigilância sanitária dar-se-á mediante o cumprimento das Boas Práticas, visando à manutenção de sua natureza, integridade, identidade e qualidade, de modo que:
a) impeçam ou evitem quaisquer acidentes ou danos;
b) atendam as especificações de temperatura de acondicionamento e de armazenagem, níveis de umidade tolerados, sensibilidade à luminosidade, entre outros, definidas pelo fabricante, ou em conformidade com a legislação sanitária;
c) as disponham em ambientes satisfatórios de higiene e desinfecção, de forma a segregar cargas incompatíveis.
2. Não será autorizada a liberação de bens ou produtos sob vigilância sanitária transportado, movimentado ou armazenado em condições ambientais que estiverem em desacordo com as especificações técnicas, indicadas pelo fabricante ou fornecidas em face da regularização perante o Sistema Nacional de Vigilância Sanitária - SNVS.
3. As condições identificadas no item anterior implicarão:
a) quando da importação pelo SISCOMEX, no indeferimento do Licenciamento de Importação;
b) quando da importação por outras modalidades a não autorização da importação ocorrerá em documento próprio;
4. A não autorização de importação deverá ser comunicada à Secretaria da Receita Federal do Brasil - Ministério da Fazenda, por intermédio de seu órgão local, para procedimento posterior de consulta à autoridade sanitária referente à movimentação ou destino daquele produto.
SEÇÃO II
DO TRANSPORTE
5. O transporte do bem ou produto dar-se-á por empresas regularizadas no Sistema Nacional de Vigilância Sanitária, quanto a Autorização de Funcionamento, Autorização Especial de Funcionamento e licença sanitária, para a respectiva atividade e classe de produto.
6. Deverão ser informadas no Conhecimento de Carga expedido, para cargas aéreas, aquáticas ou terrestres, as condições ambientais para transporte e armazenagem, como temperatura, umidade e luminosidade e outras previstas na legislação sanitária, quando couber.
7. A empresa de transporte aéreo ou aquático internacional dos bens ou produtos deverá apresentar cópia do Manifesto de Carga transportada, com previsão de desembarque, quando solicitado pela autoridade sanitária.
8. A empresa de transporte terrestre internacional de bens ou produtos deverá apresentar, por ocasião de trânsito por estação aduaneira de fronteira, o Manifesto Internacional de Cargas ou Despacho de Trânsito Aduaneiro, quando solicitado pela autoridade sanitária em exercício no local.
SEÇÃO III
DA ARMAZENAGEM
9. A armazenagem do bem ou produto dar-se-á por empresas regularizadas no Sistema Nacional de Vigilância Sanitária, quanto a Autorização de Funcionamento, Autorização Especial de Funcionamento e licença sanitária, para a respectiva atividade e classe de produto.
9.1. Considera-se armazenagem para os fins deste item a guarda dos bens ou produtos sob vigilância sanitária, independentemente do prazo de sua duração e da sua disposição temporária, da natureza e finalidade comercial da pessoa jurídica que exerça essa atividade, nas condições e exigências sanitárias previstas neste Regulamento, nas demais normas sanitárias, e, subsidiariamente, pelos dados fornecidos pelo importador e fabricante, para sua garantia e manutenção.
CAPÍTULO XXXII
BENS OU PRODUTOS EXPORTADOS PRODUZIDOS NO TERRITÓRIO NACIONAL E RETORNADOS
1. O bem ou produto sob vigilância sanitária exportado que, por quaisquer motivos seja retornado ao território nacional, deverá obedecer ao disposto neste Regulamento.
1.1. Inclui-se neste item a importação de amostras representativas do bem ou produto exportado sob rechaço para fins de controle de qualidade no território nacional.
2. O bem ou produto deverá ter o registro de Licenciamento de Importação junto ao SISCOMEX - Módulo Importação, ficando desobrigada de requerer autorização de embarque no exterior perante a autoridade sanitária em exercício no local de seu desembaraço aduaneiro.
3. O importador deverá apresentar à autoridade sanitária em exercício no local de desembaraço aduaneiro as informações referentes ao retorno e a destinação do bem ou produto, bem como o Laudo Analítico de Controle da qualidade realizado no exterior, se couber.
4. A autoridade sanitária pronunciar-se-á quanto ao deferimento de Licenciamento de Importação com ressalva e emissão dos competentes termos legais de apreensão ou de apreensão e interdição, conforme o caso, para fins de análise fiscal ou de controle, e de guarda e responsabilidade, se couber.
4.1. O termo legal de que trata este item será lavrado concomitantemente à colheita da amostra do produto.
4.2. A ressalva de que trata este item deverá ser registrada com o seguinte texto: "PRODUTO EXPORTADO COM RETORNO AO TERRITÓRIO NACIONAL SOB GUARDA E RESPONSABILIDADE DO IMPORTADOR. A LIBERAÇÃO À EXPOSIÇÃO OU ENTREGA AO CONSUMO DAR-SE-Á MEDIANTE APRESENTAÇÃO DE ANÁLISE PRÉVIA, CONCLUSIVA E SATISFATÓRIA DO LAUDO LABORATORIAL DO PRODUTO PELA AUTORIDADE SANITÁRIA EM EXERCÍCIO NO LOCAL DE DESEMBARAÇO ADUANEIRO".
4.3 A empresa importadora será notificada a realizar as análises de controle de qualidade das amostras descrito no subitem 1.1 e apresentar à autoridade sanitária o laudo de análise laboratorial.
4.4 Em caso de laudo de análise insatisfatório deverão ser apresentados o mapa de distribuição nacional e internacional do lote analisado e comprovação de retorno da totalidade exportada.
5. A liberação sanitária somente ocorrerá após análise satisfatória do laudo laboratorial do produto pela autoridade sanitária, em exercício no local de desembaraço aduaneiro.
5.1. Poderá ser realizada inspeção física dos bens ou produtos, no local de armazenagem.
6. Quando da impossibilidade de realização da análise fiscal ou de controle em laboratórios oficiais, será facultada a realização de ensaios analíticos de controle da qualidade em laboratório próprio do fabricante ou por ele terceirizado, na forma deste Regulamento e de acordo com legislação sanitária pertinente desde que justificada e autorizada pelo setor técnico da ANVISA em sua sede.
7. Os casos omissos referentes à importação de que trata este Capítulo serão examinados em conjunto pela Gerência-Geral de Portos, Aeroportos e Fronteiras - GGPAF, e pelo setor técnico competente da ANVISA, em sua sede.
CAPÍTULO XXXII
BENS OU PRODUTOS EXPORTADOS PRODUZIDOS NO
TERRITÓRIO NACIONAL E RETORNADOS
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1. O bem ou produto sob vigilância sanitária exportado que, por quaisquer motivos, seja retornado ao território nacional deverá ter o registro de Licenciamento de Importação junto ao SISCOMEX – Módulo Importação, ficando desobrigado de autorização de embarque no exterior. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1.1. Inclui-se no item 1 deste Capítulo a importação de amostras representativas do bem ou produto exportado, sob rechaço, para fins de controle de qualidade no território nacional. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2. O importador deverá apresentar à autoridade sanitária as informações referentes ao retorno e à destinação do bem ou produto, bem como o Laudo Analítico de Controle da Qualidade realizado no exterior, se couber. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3. A autoridade sanitária pronunciar-se-á quanto ao deferimento do Licenciamento de Importação, deferimento com Termo de Guarda e Responsabilidade ou emissão dos termos legais de apreensão ou interdição, conforme o caso, para fins de análise fiscal ou de controle. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3.1 A autoridade sanitária poderá realizar coleta de amostra e enviá-la para laboratórios oficiais ou credenciados. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3.1.1. Na impossibilidade de realização da análise fiscal ou de controle em laboratórios oficiais, será facultada a realização de ensaios analíticos de controle da qualidade em laboratório próprio do fabricante ou por estes terceirizado, observada a legislação sanitária pertinente, desde que justificado e autorizado pelo setor técnico competente da ANVISA em sua sede. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3.2. O deferimento com Termo de Guarda e Responsabilidade deverá ser registrado no Siscomex com o seguinte texto: “PRODUTO EXPORTADO COM RETORNO AO TERRITÓRIO NACIONAL, SOB GUARDA E RESPONSABILIDADE DO IMPORTADOR. A LIBERAÇÃO À EXPOSIÇÃO OU ENTREGA AO CONSUMO DAR-SE-Á MEDIANTE APRESENTAÇÃO DE
LAUDO LABORATORIAL DO PRODUTO CONCLUSIVO E SATISFATÓRIO ”. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
4. Quando determinada análise laboratorial pela autoridade sanitária, em caso de laudo insatisfatório, deverão ser apresentados o mapa de distribuição nacional e internacional do lote analisado e comprovação de retorno da totalidade exportada. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5. Os casos omissos referentes à importação de que trata este Capítulo serão examinados em conjunto pela Gerência-Geral de Portos, Aeroportos e Fronteiras (GGPAF), e pelo setor técnico competente da ANVISA, em sua sede. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
CAPÍTULO XXXIII
DEVOLUÇÃO/RECHAÇO DE BEM OU PRODUTO IMPORTADO INTERDITADO
1. O requerimento de devolução parcial ou total ao exterior, de bens ou produtos sob vigilância sanitária importados, sob apreensão ou interdição, em função do não cumprimento das exigências sanitárias dispostas neste Regulamento ou em outros diplomas legais sanitários em vigência, deverá ser submetido à autoridade sanitária em exercício no local de seu desembaraço aduaneiro.
1.1. À Coordenação de Portos, Aeroportos e Fronteiras da ANVISA, caberá a análise técnica conclusiva do requerimento de que trata este item;
1.2. Em casos de suspeita ou comprometimento do produto quanto à sua integridade e qualidade a Gerência Geral de Portos, Aeroportos, Fronteiras e Recintos Alfandegados deverá ser imediatamente comunicada.
2. Quando não ocorrer à efetivação do desembaraço aduaneiro das substâncias constantes das listas da Portaria SVS/MS nº 344/98 e de suas atualizações, bem como os medicamentos que as contenham, serão devolvidos ou retornados ao país de origem e a empresa deverá solicitar o cancelamento da documentação relativa à importação.
3. O importador deverá apresentar o respectivo comprovante de devolução da mercadoria ao exterior à autoridade sanitária em exercício no local de desembaraço aduaneiro, no prazo máximo de 10 (dez) dias úteis a contar da remessa do bem ou produto.
4. Todas as obrigações e ônus relacionados à devolução, parcial ou total, do bem ou produto ao exterior ficarão sob encargo do importador.
CAPÍTULO XXXIV
RETORNO DE BEM OU PRODUTO EXPORTADO PARA FINS DE PRESTAÇÃO DE SERVIÇO NO EXTERIOR OU CONSERTO, REPARO OU RESTAURAÇÃO
1. O exportador de bens ou produtos sob vigilância sanitária, para fins de prestação de serviço no exterior ou conserto com posterior retorno ao território nacional, deverá previamente ao seu embarque para o exterior, apresentar à autoridade sanitária, em exercício no local de desembaraço aduaneiro, Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2., instruída com os seguintes documentos:
a) Declaração em conformidade com o Capítulo XXXV;
b) fatura comercial em duas vias, original e cópia para autenticação, a qual ficará retida, ou declaração de propriedade do bem ou produto em que estejam descritas suas especificações técnicas, como nome comercial, marca, modelo e fabricante, assinada pelo responsável, pessoa física ou jurídica, sendo que nesse caso, por seu representante legal;
c) Documento oficial da comprovação de saída do bem ou produto.
2. A solicitação de liberação de importação referente ao retorno dos bens e produtos de que trata este Capítulo dar-se-á através da apresentação à autoridade sanitária, em exercício no local de desembaraço aduaneiro, da Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, instruída pela Declaração de Saída do Bem ou Produto para o Exterior.
3. A importação de que trata este Capítulo estará desobrigada de autorização de embarque no exterior.
CAPÍTULO XXXIV
RETORNO DE BEM OU PRODUTO EXPORTADO PARA FINS DE PRESTAÇÃO DE SERVIÇO OU CONSERTO OU REPARO OU RESTAURAÇÃO NO EXTERIOR
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1. A solicitação de liberação de importação referente ao retorno dos bens e produtos de que trata este Capítulo dar-se-á através da apresentação da Petição para Fiscalização e Liberação Sanitária prevista no Capítulo II, subitem 1.2, instruída com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) nota fiscal de compra ou declaração de propriedade do bem ou produto, em que estejam descritas suas especificações técnicas, como nome comercial, marca, modelo e fabricante, assinada pelo responsável, pessoa física ou jurídica, sendo nesse último caso, por seu representante legal; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Declaração de exportação ou documento aduaneiro equivalente que comprove a saída do bem ou produto. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2. A importação de que trata este Capítulo estará desobrigada de autorização de embarque no exterior. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
CAPÍTULO XXXV
DECLARAÇÃO DE SAÍDA DE BEM OU PRODUTO PARA EXTERIOR (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)Este texto não substitui o(s) publicado(s)
CAPÍTULO XXXVI
DAS PENALIDADES E RESTRIÇÕES
SEÇÃO I
DAS DISPOSIÇÕES GERAIS
1. O não cumprimento ou inobservância do disposto neste Regulamento sujeitará o importador e o responsável pela regularização do produto às penalidades e restrições previstas na legislação sanitária, sem prejuízo do exercício das atribuições de outros órgãos públicos.
1.1. Conforme a necessidade e adequação das penalidades e restrições para a prevenção e promoção da saúde pública, na hipótese de aplicação conjunta de medidas com a autoridade aduaneira, esta poderá promover a guarda de produto.
1.2. O disposto no item anterior não exime a autoridade sanitária de aplicar as penalidades e restrições pertinentes por intermédio da lavratura de termos legais.
SEÇÃO II
DA APREENSÃO, INTERDIÇÃO CAUTELAR E INUTILIZAÇÃO
2. A apreensão de amostras para efeito de análise, fiscal ou de controle, será acompanhada de Termo de Apreensão.
3. Os bens ou produtos sujeitar-se-ão à análise de controle ou fiscal mediante colheita de amostras sempre que a autoridade sanitária entender necessário, quando for obrigatória ou por suspeita de contrariedade à legislação sanitária.
3.1. Excetua-se do disposto no item anterior o bem ou produto importado por pessoa física cuja quantidade inviabilize este procedimento.
4. Nas hipóteses em que forem flagrantes os indícios de alteração, adulteração ou contrariedade à legislação sanitária, os produtos sujeitar-se-ão à interdição de caráter preventivo, mediante lavratura de Termo de Apreensão e Interdição para o lote ou partida importada.
4.1. Incluir-se-ão no disposto neste item os bens ou produtos:
a) em que forem constatadas avaria em suas embalagens, com suspeita de comprometimento de sua integridade;
4.2. A interdição cautelar durará o prazo necessário para realização de testes, provas, análises ou outras providências requeridas, limitando-se ao prazo assinalado para sua execução.
5. Os bens ou produtos sujeitar-se-ão à interdição nas hipóteses de resultado laboratorial condenatório ou constatação de contrariedade à legislação sanitária, mediante Termo de Interdição, inclusive interdição do estabelecimento, quando necessário.
6. O bem ou produto não previsto em documento de importação sujeitar-se-á à apreensão e interdição, ou interdição, conforme o caso.
7. Na hipótese de alteração, adulteração ou falsificação dos bens ou produtos que impliquem na impropriedade do uso ou consumo, ficarão sujeitas a inutilização, mediante lavratura de Termo de Inutilização, sob encargo do importador.
7.1. Incluir-se-ão no disposto neste item os bens ou produtos objeto de fiscalização sanitária de doações internacionais.
7.2. Os procedimentos técnicos, intermediários e finais, relacionados a inutilização deverão obrigatoriamente ocorrer sob anuência e na presença da autoridade sanitária.
7.3. Os métodos de tratamento e destinação final relacionados a inutilização de todas e quaisquer bens ou produtos de interesse da vigilância sanitária, ainda que não sujeitas a controle expresso de modalidades de importação, deverão atender às disposições de controle ambiental da unidade federada de sua execução.
SEÇÃO III
DA GUARDA E RESPONSABILIDADE
8. Os bens ou produtos sob vigilância sanitária submetidos à análise, fiscal ou de controle, quando de seu ingresso no país poderão ter sua saída da área alfandegada autorizada, com ressalva, mediante a sujeição do importador ao Termo de Guarda e Responsabilidade.
8.1. A ressalva de que trata este item deverá ser registrada no campo referente à situação da Licença de Importação no SISCOMEX, ou em documento de importação próprio, com o seguinte texto: "PRODUTO SOB EXIGÊNCIA SANITÁRIA. A LIBERAÇÃO À INDUSTRIALIZAÇÃO, EXPOSIÇÃO À VENDA OU ENTREGA AO CONSUMO DAR-SE-Á MEDIANTE MANIFESTAÇÃO EXPRESSA DA AUTORIDADE SANITÁRIA".
9. Constituirá pressuposto obrigatório para guarda e responsabilidade do bem ou produto na forma desta Seção, sua armazenagem em estabelecimento detentor de Licença Sanitária ou autorização equivalente, emitida pela autoridade sanitária do Estado, Município ou o Distrito Federal, e, quando couber, autorizada junto a ANVISA no tocante à Autorização de Funcionamento ou Autorização de Funcionamento Especial, para a respectiva atividade e classe de produto.
10. A liberação do bem ou produto e das obrigações decorrentes do Termo de Guarda e Responsabilidade dar-se-á após inspeção física, ou adoção de outras medidas que julgar necessárias, pela Coordenação de Vigilância Sanitária de Portos, Aeroportos e Fronteiras do estado federado do local de guarda.
10.1. A manifestação de que trata este item deverá ser inscrita no próprio termo.
10.2. Considerar-se-ão outras medidas necessárias para os fins deste item, a fiscalização subsidiária do bem ou produto, instalações físicas e documentos de registros técnicos da empresa para resolubilidade da exigência sanitária determinada pela autoridade sanitária, inclusive em outras unidades federadas.
CAPÍTULO XXXVII
DISPOSIÇÕES FINAIS
1. Será vedada a importação de bens ou produtos sob vigilância sanitária por meio de mala diplomática ou consular, em função do conceito desse instituto, de acordo com a legislação pertinente.
1.1. O não cumprimento ou inobservância do disposto neste item sujeitará o importador às disposições deste Regulamento.
2. A importação com finalidade declarada pelo importador, não sujeita a intervenção sanitária da ANVISA, cuja classificação tarifária - NCM/SH - integre a listagem e os procedimentos previstos no Capítulo XXXIX deste Regulamento, deverá ter o deferimento do Licenciamento de Importação exercido em consonância com a autoridade da ANVISA, no local de desembaraço aduaneiro.
2.1. A importação de que trata o item anterior, deverá ter registrado no campo "informações complementares" do Licenciamento de Importação a finalidade e uso do produto.
2.2. A consonância no exercício fiscal de que trata este item limitar-se-á à análise documental apresentada pelo importador por meio da Petição para Fiscalização Sanitária prevista no Capítulo II, subitem 1.2., instruída por Termo de Responsabilidade conforme Capítulo XXXVIII.
2.2.1. O Termo de Responsabilidade de que trata este subitem deverá ser subscrita pelo responsável legal e/ou responsável técnico, com reconhecimento de firma em cartório e acompanhada por manifestação satisfatória e conclusiva do órgão público anuente, quando couber.
2.2.2. Os bens ou produtos não sujeitos a intervenção sanitária da ANVISA de que tratam este item, não serão consideradas como hipótese de incidência para recolhimento na importação da Taxa de Fiscalização de Vigilância Sanitária junto a ANVISA, de acordo com a enumeração legal dos bens e produtos sob seu exclusivo controle e fiscalização sanitária.
2.3. Não estão sujeitas a intervenção sanitária da ANVISA, na importação, as substâncias "TRICLOROETILENO, DISSULFIRAM ou LITIO (METALICOS E SEUS SAIS)" previstas nas Portarias SVS/MS nº. 344/98, quando de sua utilização para outros fins, que não os terapêuticos ou medicamentosos, desde que comprovado a importação para pessoa jurídica responsável pela produção em parque industrial nacional de produtos sem fins terapêuticos ou medicamentosos;
2.3.1. O importador de que trata o disposto no subitem anterior, deverá apresentar a autoridade sanitária no local de desembaraço, petição para fiscalização sanitária prevista no Capítulo II, subitem 1.2. instruída por Termo de Responsabilidade de trata o Capítulo XXXVIII;
2.3.2. O exercício de que trata este subitem limitar-se-á a análise da documentação apresentada pelo importador.
2.4. O deferimento do Licenciamento de Importação dar-se-á com ressalva, mediante análise satisfatória das informações exigidas pela autoridade sanitária.
2.5. A ressalva de que trata o item anterior deverá ser registrada no campo referente à situação do licenciamento de importação no SISCOMEX com o seguinte texto: "BEM OU PRODUTO IMPORTADO COM FINALIDADE NÃO SUJEITA A INTERVENÇÃO SANITÁRIA DA ANVISA, CONFORME TERMO DE RESPONSABILIDADE APRESENTADO PELO IMPORTADOR".
2. A importação com finalidade declarada pelo importador, não sujeita a intervenção sanitária da ANVISA, cuja classificação tarifária - NCM/SH - integre a listagem e os procedimentos previstos no Capítulo XXXIX desta Resolução, deverá submeter-se à fiscalização da ANVISA, mediante apresentação de Petição para Fiscalização e Liberação Sanitária, prevista no subitem 1.2 do Capítulo II, instruída pelo Termo de Responsabilidade descrito no Capítulo XXXVIII desta Resolução. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.1. O Termo de Responsabilidade de que trata o item 2 deste Capítulo será subscrito pelo responsável legal e/ou responsável técnico do Importador e deverá obrigatoriamente descrever qual a finalidade e o uso do produto importado. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.2. Os bens ou produtos não sujeitos a intervenção sanitária da ANVISA de que trata o item 2 deste Capítulo, não serão consideradas como hipótese de incidência para recolhimento, na importação, da Taxa de Fiscalização de Vigilância Sanitária junto à ANVISA. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.3. Substâncias constantes nas Listas da Portarias SVS/MS nº 344, de 12 de maio de 1998, e suas atualizações, com isenção de controle prevista nessa mesma Portaria, quando utilizadas exclusivamente para fins industriais legítimos, que não os terapêuticos ou medicamentosos, não estão sujeitas a intervenção sanitária da ANVISA.
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
2.4. O deferimento do Licenciamento de Importação se dará após análise satisfatória das informações exigidas nesta Resolução, com registro, no campo referente à situação do licenciamento de importação no SISCOMEX, do seguinte texto: “BEM OU PRODUTO IMPORTADO COM FINALIDADE NÃO SUJEITA A INTERVENÇÃO SANITÁRIA DA ANVISA, CONFORME TERMO DE RESPONSABILIDADE APRESENTADO PELO IMPORTADOR”. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
3. Além dos procedimentos previstos neste Regulamento, deverão ser observadas e cumpridas às medidas e formalidades previstas em outros dispositivos legais e regulamentares, ou outras determinadas a qualquer tempo pela autoridade sanitária, inclusive quanto à suspensão temporária ou definitiva da importação, à vista de razões fundamentadas de prevenção e precaução da nocividade do bem ou produto à saúde humana individual e coletiva.
4. As informações relativas à importação de bens ou produtos, na forma deste Regulamento, deverão corresponder fidedignamente às constatadas quando da sua inspeção e fiscalização sanitária.
5. As medidas para o exercício da fiscalização de bens ou produtos sob exigência sanitária, na forma deste Regulamento, em áreas externas não compreendidas para o processo de importação ou fora dos recintos alfandegados, poderão ser realizadas pela respectiva instância do Sistema Único de Saúde em que se encontre o produto, de acordo com a integração em nível executivo das ações de saúde, conforme adotado e acordado pela ANVISA, em sua sede.
6. O bem ou produto sob vigilância sanitária apreendido ou interditado por outras autoridades públicas, de saúde ou não, no exercício fiscal do processo de importação, na forma deste Regulamento, deverá submeter-se a parecer técnico prévio da respectiva Coordenação de Vigilância Sanitária de Portos, Aeroportos e Fronteiras em que a mesma se encontre apreendida e interditada, com vistas à manifestação sobre seu padrão de identidade e qualidade, e sua liberação sanitária, se for o caso.
6.1. Incluir-se-ão no disposto deste item os bens ou produtos sob vigilância sanitária destinados à doação, leilão ou qualquer outro evento que viabilize seu contato, exposição ou consumo, potencial ou efetivo, de forma direta ou indireta, por seres humanos.
7. Todas as medidas, formalidades e exigências sanitárias para o cumprimento e observância deste Regulamento serão efetivadas conforme orientação técnico-normativa dos setores hierárquicos responsáveis, tanto da Gerência-Geral de Portos, Aeroportos e Fronteiras, e das Gerências-Gerais, setores técnicos competentes, quanto da Diretoria Colegiada da ANVISA, na pessoa do seu Diretor-Presidente.
8. A importação de bens ou produtos não regularizados na ANVISA, vinculada à obrigatoriedade de cumprimento de ações judiciais deferidas no interesse de tratamento clínico de pacientes, na qual a pessoa jurídica importadora seja o Ministério da Saúde, Secretarias de Estado e Distrito Federal ou Municipais de Saúde, deverá ter análise e o deferimento do Licenciamento de Importação concedidos pela autoridade sanitária em exercício no local de desembaraço aduaneiro.
8. A importação de bens ou produtos não regularizados na ANVISA, vinculada à obrigatoriedade de cumprimento de ações judiciais deferidas no interesse de tratamento clínico de pacientes, na qual a pessoa jurídica importadora seja instituição pública integrante da estrutura organizacional do Sistema Único de Saúde (SUS), terá deferimento automático do licenciamento de importação no SISCOMEX, independentemente da realização de qualquer outra análise técnica ou procedimental, sendo de responsabilidade do importador garantir a qualidade e segurança dos produtos adquiridos. (Redação dada pela Resolução – RDC nº 262, de 1º de fevereiro de 2019)
9. A importação de medicamentos de que tratam os procedimentos 2, 2-A, 2-B e 2-C do Capítulo XXXIX, não regularizados na ANVISA, destinados a programas de saúde publica estará sob autorização exclusiva Diretoria Colegiada da ANVISA, na pessoa do Diretor Presidente.
10. O pleito de nacionalização de produto sob vigilância sanitária motivado pela constatação de irregularidades sanitárias, em análise documental ou em inspeção física, quando fundamentado por documentação técnica, deverá ser requerido à Coordenação de Portos, Aeroportos, Fronteiras e Recintos Alfandegados da unidade federada onde ocorreu a intervenção fiscal e analisado posteriormente, quando couber, pela Gerência Geral de Portos, Aeroportos, Fronteiras e Recintos Alfandegados e/ou pelas áreas técnicas competentes da ANVISA, em sua sede.
10.1. Em virtude do disposto no item acima deverá ser elaborado parecer conclusivo para aprovação das Gerências Gerais envolvidas ou da Diretoria Colegiada da ANVISA, quando couber.
11. A importação de cabelo humano desprovido de bulbo capilar, destinado à confecção de perucas e apliques, dar-se-á por meio de registro de Licenciamento de Importação junto ao SISCOMEX, de acordo com o Capítulo XXXIX deste Regulamento ou Remessa Expressa. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
11.1. O produto de que trata este item deverá apresentar-se em embalagem íntegra, e identificada em seu rótulo com as informações técnicas pertinentes, como esterilização, desinfecção e desinfestação. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
11.2. A empresa importadora do produto de que trata este item estará desobrigada de Autorização de Funcionamento junto a ANVISA. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
12. A critério da autoridade sanitária poderá ser exigida a tradução, por signatário devidamente identificado pelo nome, endereço e número do Cadastro de Pessoa Física-CPF, dos documentos apresentados em língua estrangeira, para os fins deste Regulamento.
13. A Regulamentação da alteração da titularidade da empresa em razão de fusão, cisão, incorporação ou sucessão deverá atender ao disposto na legislação sanitária pertinente.
14. Os órgãos e entidades participantes da anuência para importação de bens ou produtos de interesse sanitário poderão mediante acordo entre as partes implantar e promover medidas pactuadas para a consecução do disposto neste Regulamento.
14.1. Para os fins do disposto neste item, os órgãos e entidades poderão adotar:
a) conduta de fiscalização sanitária harmônica, por categoria de risco dos produtos;
b) metodologia de coleta, transporte e análise laboratorial, por categoria do produto importado importada;
c) definição de laboratório responsável por tipo de análise, para os fins do disposto na alínea anterior;
d) plano de capacitação de recursos humanos;
e) plano de trabalho de implantação do sistema harmonizado de fiscalização sanitária e fitossanitária dos bens ou produtos importados, e cronograma de execução.
15. Os casos não previstos neste Regulamento serão analisados pela área técnica competente da ANVISA, em sua sede.
CAPÍTULO XXXVIII


CAPÍTULO XXXIX
PROCEDIMENTOS ADMINISTRATIVOS PARA ENQUADRAMENTO DOS PRODUTOS JUNTO AO SISTEMA INTEGRADO DE COMÉRCIO EXTERIOR
SEÇÃO I
PROCEDIMENTO 1 - BENS E PRODUTOS SUJEITOS AO CONTROLE ESPECIAL DE QUE TRATA A PORTARIA SVS/MS Nº 344, DE 1998 E SUAS ATUALIZAÇÕES, EM SUAS LISTAS "A1", "A2", "A3", "B1", "B2" E "D1"
SEÇÃO I
PROCEDIMENTO 1 - BENS E PRODUTOS SUJEITOS AO CONTROLE ESPECIAL DE QUE TRATA A PORTARIA SVS/MS Nº 344, DE 1998 E SUAS ATUALIZAÇÕES, EM SUAS LISTAS "A1", "A2", "A3", "B1", "B2", "C3" E "D1"
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
1. A importação de bens e produtos sujeitos ao controle especial de que trata a Portaria SVS/MS nº 344, de 1998 e suas atualizações, na forma de matéria-prima, produto semi-elaborado ou produto acabado, conforme enquadramento dos bens e produtos disponível no sítio eletrônico da ANVISA estará sujeita ao registro de Licenciamento de Importação no SISCOMEX e autorização prévia favorável de embarque, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
2. A autorização prévia favorável de embarque dar-se-á mediante manifestação da área técnica competente da ANVISA, em sua sede, em Brasília, DF.
2.1. Caberá a empresa interessada encaminhar à ANVISA requerimento para autorização de embarque no exterior, mediante preenchimento de Petição de Autorização de Embarque no Exterior.
3. Os bens e produtos sujeitos ao controle especial de que trata a Portaria SVS/MS nº 344, de 1998 e suas atualizações, somente poderão entrar em território nacional pelos seguintes portos e aeroportos: (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Porto do Rio de Janeiro, Rio de Janeiro, RJ; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Aeroporto Internacional do Rio de Janeiro - Aeroporto Maestro Antônio Carlos Jobim, Rio de Janeiro, RJ; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Porto de Santos, Santos, SP; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Aeroporto Internacional de São Paulo - Aeroporto Governador André Franco Montoro, Guarulhos, SP. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
4. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçada a matéria-prima, o insumo ou o medicamento:
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II ;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Autorização de Importação ou Certificado de Não Objeção emitido pela área competente na ANVISA (2ª via original ou cópia para autenticação);
e) Autorização de Exportação ou Certificado de Não Objeção (2ª via original ou cópia para autenticação) emitida pela autoridade competente no exterior;
f) Fatura Comercial - "Invoice" (original e cópia para autenticação); g) Conhecimento de Carga Embarcada (original e cópia para autenticação);
h) Declaração quanto aos lotes ou partidas, identificados alfa-numericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
i) Laudo Analítico de Controle de Qualidade, por lote ou partida, emitido pelo fabricante, exceto quando se tratar de importações de padrões de referência primários;
j) Guia de Retirada de Substâncias, Medicamentos Entorpecentes, ou que determinem dependência física ou psíquica, na forma do Capítulo V da Portaria SVS/MS nº 344, de 1998 e suas atualizações, emitida em 6 (seis) vias; (Revogada pela Resolução – RDC nº 62, de 11 de fevereiro de 2016)
l) Instrumento de procuração da pessoa jurídica detentora da regularização do produto junto a ANVISA ao representante legal, responsável pelo desembaraço; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
m) Documento de averbação referente à comprovação da atracação do bem e produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenada.
4.1. Os documentos de que tratam as alíneas "d", "e", "h" e "i" deverão ser atestados pelo responsável técnico. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
4.2. Estará isento da apresentação do documento da alínea "l", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
5. O enquadramento dos produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO II
PROCEDIMENTO 1-A - BENS E PRODUTOS SUJEITOS AO CONTROLE ESPECIAL DE QUE TRATA A PORTARIA SVS/MS Nº 344, DE 1998 E SUAS ATUALIZAÇÕES, EM SUA LISTA "F"
6. É vedada a importação de produtos sujeitas ao controle especial de que trata a Portaria SVS/MS nº 344, de 1998 e suas atualizações, constantes da Lista "F", na forma de matéria-prima, produto semi-elaborado ou produto acabado, conforme enquadramento dos bens e produtos disponível no sítio eletrônico da ANVISA, salvo se destinada a ensino e pesquisa.
7. A importação dos bens e produtos de que trata esta Seção estará sujeita ao registro de Licenciamento de Importação no SISCOMEX e autorização prévia favorável de embarque, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
8. A autorização prévia favorável de embarque dar-se-á mediante manifestação da área técnica competente da ANVISA, em sua sede, em Brasília, DF.
8.1.Caberá a empresa interessada encaminhar à ANVISA requerimento de autorização de embarque no exterior, mediante preenchimento de Petição de Autorização de Embarque no Exterior.
9. Os bens e produtos s sujeitos ao controle especial de que trata a Portaria SVS/MS nº 344, de 1998 e suas atualizações, constantes da Lista "F", somente poderão entrar em território nacional pelos seguintes portos e aeroportos:
a) Porto do Rio de Janeiro, Rio de Janeiro, RJ;
b) Aeroporto Internacional do Rio de Janeiro - Aeroporto Maestro Antônio Carlos Jobim, Rio de Janeiro, RJ;
c) Porto de Santos, Santos, SP;
d) Aeroporto Internacional de São Paulo - Aeroporto Governador André Franco Montoro, Guarulhos, SP.
10. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçada a matéria-prima, o insumo ou o medicamento:
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Autorização de Importação ou Certificado de Não Objeção emitido pela área competente na ANVISA (2ª via original ou cópia para autenticação);
e) Autorização de Exportação ou Certificado de Não Objeção (2ª via original ou cópia para autenticação) emitida pela autoridade competente no exterior;
f) Fatura Comercial - "Invoice" (original e cópia para autenticação); g) Conhecimento de Carga Embarcada (original e cópia para autenticação);
h) Declaração quanto aos lotes ou partidas, identificados alfa-numericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
i) Laudo Analítico de Controle de Qualidade, por lote ou partida, emitido pelo fabricante, exceto quando se tratar de importações de padrões de referência primários;
j) Guia de Retirada de Substâncias, Medicamentos Entorpecentes, ou que determinem dependência física ou psíquica, na forma do Capítulo V da Portaria SVS/MS nº 344 de 1998 e suas atualizações, emitida em 6 (seis) vias; (Revogada pela Resolução – RDC nº 62, de 11 de fevereiro de 2016) (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
l) Instrumento de procuração da pessoa jurídica detentora da regularização do produto junto a ANVISA ao representante legal, responsável pelo desembaraço; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
m) Documento de averbação referente à comprovação da atracação do bem ou produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenado.
10.1. Os documentos de que tratam as alíneas "d", "e", "h" e "i" deverão ser atestados pelo responsável técnico. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
10.2. Estará isento da apresentação do documento da alínea "l", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
11. O enquadramento dos produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO III
PROCEDIMENTO 2 - HEMODERIVADOS
12. A importação de hemoderivados na forma de matéria-prima, produto semi elaborado, produto a granel ou produto acabado, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
13. Os bens e produtos de que tratam esta Seção somente poderão entrar em território nacional pelos seguintes portos e aeroportos: (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Porto do Rio de Janeiro, Rio de Janeiro, RJ; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Aeroporto Internacional do Rio de Janeiro - Aeroporto Maestro Antônio Carlos Jobim, Rio de Janeiro, RJ; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Porto de Santos, Santos, SP; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Aeroporto Internacional de São Paulo - Aeroporto Governador André Franco Montoro, Guarulhos, SP; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e) Aeroporto Internacional Tancredo Neves, MG; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
f) Aeroporto Internacional de Porto Alegre - Aeroporto Internacional Salgado Filho, RS; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Aeroporto Internacional de Brasília - Aeroporto Internacional Presidente Juscelino Kubitschek, DF; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
h) Aeroporto Internacional de Guararapes - Aeroporto Internacional Gilberto Freire, PE; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
i) Aeroporto Internacional de Manaus - Aeroporto Internacional Eduardo Gomes, AM. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
16. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o bem ou produto:
16. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Declaração quanto aos lotes ou partidas, identificados alfanumericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Laudo Analítico de Controle de Qualidade do ingrediente farmacêutico ativo e produto terminado, por lote ou partida, emitido pelo fabricante, exceto quando se tratar de importações de padrões de referência primários;
h) Certificado de liberação do lote do produto acabado (terminado), emitido pela autoridade sanitária do país de fabricação, para hemoderivados, exceto quando se tratar de importações de padrões de referência primários;
i) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente, para colheita e transporte de produtos para análise de controle, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
j) Instrumento de procuração da pessoa jurídica detentora da regularização do produto junto a ANVISA ao representante legal, responsável pelo desembaraço; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
l) Documento de averbação referente à comprovação da atracação do bem ou produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o bem ou produto encontra-se armazenada.
13.1.Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
13.2. Os documentos de que tratas as alíneas "f" e "g" deverão ser atestados pelo responsável técnico (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
13.3. Estará isento da apresentação do documento da alínea "j", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
14. O enquadramento dos bens ou produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
15. A importação de amostras de medicamentos não regularizados, sem comprovação de segurança e eficácia, destinada à análise para fins de registro, testes de controle da qualidade, estudos de estabilidade, bioequivalência e equivalência farmacêutica ou ainda testes de equipamentos participantes do processo fabril ou laboratorial, cuja composição integra substâncias ativas com comprovação de segurança e eficácia deverá atender as exigências sanitárias previstas neste procedimento, excetuada a referente à apresentação do registro ANVISA.
SEÇÃO IV
PROCEDIMENTO 2A - SOROS E VACINAS
16. A importação de soros hiperimunes e vacinas na forma de matéria-prima, produto semi-elaborado, produto a granel ou produto acabado, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
17. Os bens e produtos de que tratam esta Seção somente poderão entrar em território nacional pelos seguintes portos e aeroportos: (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Porto do Rio de Janeiro, Rio de Janeiro, RJ; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Aeroporto Internacional do Rio de Janeiro - Aeroporto Maestro Antônio Carlos Jobim, Rio de Janeiro, RJ; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Porto de Santos, Santos, SP; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Aeroporto Internacional de São Paulo - Aeroporto Governador André Franco Montoro, Guarulhos, SP; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e) Aeroporto Internacional Tancredo Neves, MG; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
f) Aeroporto Internacional de Porto Alegre - Aeroporto Internacional Salgado Filho, RS; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Aeroporto Internacional de Brasília - Aeroporto Internacional Presidente Juscelino Kubitschek, DF; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
h) Aeroporto Internacional de Guararapes - Aeroporto Internacional Gilberto Freire, PE; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
i) Aeroporto Internacional de Manaus - Aeroporto Internacional Eduardo Gomes, AM. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
18. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o bem ou produto:
18. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Declaração quanto aos lotes ou partidas, identificados alfanumericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Laudo Analítico de Controle de Qualidade do ingrediente farmacêutico ativo e produto terminado, por lote ou partida, emitido pelo fabricante, exceto quando se tratar de importações de padrões de referência primários;
h) Certificado de liberação do lote do produto acabado (terminado), emitido pela autoridade sanitária do país de fabricação, para vacinas e soros, exceto quando se tratar de importações de padrões de referência primários;
i) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente, para colheita e transporte de produtos para análise de controle, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
j) Instrumento de procuração da pessoa jurídica detentora da regularização do produto junto a ANVISA ao representante legal, responsável pelo desembaraço; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
l) Documento de averbação referente à comprovação da atracação do bem ou produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o bem ou produto encontra-se armazenada. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
18.1.Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
18.2. Os documentos de que tratas as alíneas "f" e "g" deverão ser atestados pelo responsável técnico. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
18.3. Estará isento da apresentação do documento da alínea "j", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
19. O enquadramento dos bens ou produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
20. A importação de amostras de medicamentos não regularizados, sem comprovação de segurança e eficácia, destinada à análise para fins de registro, testes de controle da qualidade, estudos de estabilidade, bioequivalência e equivalência farmacêutica ou ainda testes de equipamentos participantes do processo fabril ou laboratorial, cuja composição integra substâncias ativas com comprovação de segurança e eficácia deverá atender as exigências sanitárias previstas neste procedimento, excetuada a referente à apresentação do registro ANVISA.
SEÇÃO V
PROCEDIMENTO 2B- PRODUTOS BIOLÓGICOS DERIVADOS DE FLUIDOS OU TECIDOS DE ORIGEM ANIMAL E ALÉRGENOS
21. A importação de produtos biológicos derivados de fluidos ou tecidos de origem animal e alérgenos na forma de matéria-prima, produto semi-elaborado, produto a granel ou produto acabado, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
22. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o insumo ou o produto:
22. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Declaração quanto aos lotes ou partidas, identificados alfanumericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Laudo Analítico de Controle de Qualidade ingrediente farmacêutico ativo e produto terminado, por lote ou partida, emitido pelo fabricante, exceto quando se tratar de importações de padrões de referencia primários;
h) Instrumento de procuração da pessoa jurídica detentora da regularização do produto junto a ANVISA ao representante legal, responsável pelo desembaraço; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
i) Documento de averbação referente à comprovação da atracação do bem ou produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenada. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
22.1. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
22.2. Os documentos de que tratas as alíneas "f" e "g" deverão ser atestados pelo responsável técnico. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
22.3. Estará isento da apresentação do documento da alínea "h", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
23. O enquadramento dos bens ou produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
24. A importação de amostras de medicamentos não regularizados, sem comprovação de segurança e eficácia, destinada à análise para fins de registro, testes de controle da qualidade, estudos de estabilidade, bioequivalência e equivalência farmacêutica ou ainda testes de equipamentos participantes do processo fabril ou laboratorial, cuja composição integra substâncias ativas com comprovação de segurança e eficácia deverá atender as exigências sanitárias previstas neste procedimento, excetuada a referente à apresentação do registro ANVISA.
SEÇÃO VI
PROCEDIMENTO 2C - PRODUTOS BIOLÓGICOS OBTIDOS POR PROCEDIMENTOS BIOTECNOLÓGICOS, ANTICORPOS MONOCLONAIS, MEDICAMENTOS CONTENDO MICROORGANISMOS VIVOS, ATENUADOS OU MORTOS E PROBIÓTICOS.
25. A importação de produtos biológicos obtidos por procedimentos biotecnológicos, anticorpos monoclonais, medicamentos contendo microorganismos vivos, atenuados ou mortos e probióticos na forma de matéria-prima, produto semi elaborado, produto a granel ou produto acabado, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA estará sujeita ao registro de Licenciamento de Importação no SISCOMEX e autorização prévia favorável de embarque, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
25. A importação de produtos biológicos obtidos por procedimentos biotecnológicos, anticorpos monoclonais, medicamentos contendo microorganismos vivos, atenuados ou mortos e probióticos na forma de matéria-prima, produto semielaborado, produto a granel ou produto acabado, estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se a fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
25.1. A autorização prévia de embarque dar-se-á mediante manifestação do setor técnico da ANVISA em sua sede, em Brasília, DF. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
25.2. Caberá a empresa interessada, encaminhar à autoridade competente requerimento de autorização de embarque no exterior, mediante preenchimento de Petição de Autorização de Embarque no Exterior. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
25.3. Constituir-se-á documentação obrigatória para apresentação à área responsável pela autorização prévia de embarque do insumo ou o produto: (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) protocolo resumido de produção do produto (de acordo com o protocolo padrão da OMS, caso o produto esteja incluído no mesmo); (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) certificado de análise do controle de qualidade da matéria-prima (princípio ativo), emitido pelo fabricante; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) certificado de análise do controle de qualidade do produto acabado, emitido pelo fabricante; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) certificado de liberação do lote do produto emitido pela autoridade sanitária do país de origem; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e) documentos técnicos do hemoderivado utilizado como estabilizante, quando for o caso: (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e.1) declaração de origem do plasma utilizado; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e.2) certificado de análise do controle de qualidade do plasma utilizado; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e.3) certificado de liberação da sorologia do plasma utilizado. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
26. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o insumo ou o produto:
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente;
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber;
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Declaração quanto aos lotes ou partidas, identificados alfanumericamente, no que couber;
g) Laudo Analítico de Controle de Qualidade do produto terminado, por lote ou partida, emitido pelo fabricante, exceto quando se tratar de importações de padrões de referencia primários;
h) Instrumento de procuração da pessoa jurídica detentora da regularização do produto junto a ANVISA ao representante legal, responsável pelo desembaraço;
i) Documento de averbação referente à comprovação da atracação do bem ou produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenada.
26. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II desta Resolução; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Fatura Comercial - “Invoice”; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Conhecimento de Carga Embarcada; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) protocolo resumido de produção do produto (de acordo com o protocolo padrão da OMS, caso o produto esteja nele incluído); (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e) certificado de análise do controle de qualidade da matéria-prima (princípio ativo), emitido pelo fabricante; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
f) certificado de análise do controle de qualidade do produto acabado, emitido pelo fabricante; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) certificado de liberação do lote do produto, emitido pela autoridade sanitária do país de origem, quando couber; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
h) os seguintes documentos técnicos do hemoderivado utilizado como estabilizante, quando for o caso: declaração de origem do plasma utilizado; certificado de análise do controle de qualidade do plasma utilizado; e certificado de liberação da sorologia do plasma utilizado. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
26.1. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata este Capítulo deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
26.2. Os documentos de que tratas as alíneas "f" e "g" deverão ser atestados pelo responsável técnico. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
26.3. Estará isento da apresentação do documento da alínea "h", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
27. O enquadramento dos bens ou produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
28. A importação de amostras de medicamentos não regularizados, sem comprovação de segurança e eficácia, destinada à análise para fins de registro, testes de controle da qualidade, estudos de estabilidade, bioequivalência e equivalência farmacêutica ou ainda testes de equipamentos participantes do processo fabril ou laboratorial, cuja composição integra substâncias ativas com comprovação de segurança e eficácia deverá atender as exigências sanitárias previstas neste procedimento, excetuada a referente à apresentação do registro ANVISA.
SEÇÃO VII
PROCEDIMENTO 3 - PRODUTOS SUJEITO A CONTROLE ESPECIAL DE QUE TRATA A PORTARIA SVS/MS Nº 344 DE 1998 E SUAS ATUALIZAÇÕES, EM SUAS LISTAS "C1", "C2", "C3", "C4" E "C5"
SEÇÃO VII
PROCEDIMENTO 3 - PRODUTOS SUJEITO A CONTROLE ESPECIAL DE QUE TRATA A PORTARIA SVS/MS Nº 344 DE 1998 E SUAS
ATUALIZAÇÕES, EM SUAS LISTAS "C1", "C2" E "C5"
(Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
(Revogadas as disposições aplicáveis à Lista "C4", às substâncias e aos medicamentos antirretrovirais pela Resolução – RDC nº 103, de 31 de agosto de 2016)
29. A importação de produto sujeitos ao controle especial de que trata a Portaria SVS/MS nº 344, de 1998 e suas atualizações, na forma de matéria-prima, produto semi elaborado ou produto acabado, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA estará sujeita ao registro de Licenciamento de Importação no SISCOMEX e autorização prévia favorável de embarque, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
29. A importação de produtos sujeitos ao controle especial de que trata a Portaria SVS/MS nº 344, de 12 de maio de 1998, e suas atualizações, na forma de matéria prima, produto semielaborado ou produto acabado, estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
30. A autorização prévia favorável de embarque dar-se-á mediante manifestação da área técnica competente, da ANVISA em sua sede, em Brasília, DF. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
30.1. Caberá a empresa interessada encaminhar à ANVISA apresentar requerimento de autorização de embarque no exterior, mediante preenchimento de Petição de Autorização de Embarque no Exterior. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
31. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o produto:
31. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Certificado de Não Objeção, ou Declaração de que no país de origem não há expedição desse documento; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e) Fatura Comercial - "Invoice";
f) Conhecimento de Carga Embarcada;
g) Declaração quanto aos lotes ou partidas, identificados alfa-numericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
h) Laudo Analítico de Controle de Qualidade, por lote ou partida, emitido pelo fabricante, exceto quando se tratar de importações de padrões de referencia primários;
i) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
j) Instrumento de procuração da pessoa jurídica detentora da regularização do produto junto a ANVISA ao representante legal, responsável pelo desembaraço; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
l) Documento de averbação referente à comprovação da atracação do produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenado. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
31.1. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
31.2. Os documentos de que tratam as alíneas "g" e "h" deverão ser atestados pelo responsável técnico, e, naquele caso, também pelo responsável ou representante legal. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
31.3. Estará isento da apresentação do documento da alínea "j", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
32. O enquadramento dos produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO VIII
PROCEDIMENTO 4 - PRODUTOS PARA SAÚDE
(Exigência suspensa quanto à autorização de embarque pela Resolução - RDC nº 48, de 31 de agosto de 2012)
33. A importação de produtos para saúde na forma de matéria-prima, produto semi-elaborado, produto a granel ou produto acabado, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA, estará sujeita ao registro de Licenciamento de Importação no SISCOMEX e autorização prévia favorável de embarque, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
33. A importação de produtos para saúde, na forma de matéria-prima, produto semielaborado, produto a granel ou produto acabado, estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
34. A autorização prévia de embarque dar-se-á mediante manifestação da autoridade sanitária de desembaraço aduaneiro no tocante ao status no Licenciamento de Importação. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
34.1. Nos casos previstos neste Regulamento, a autorização prévia de embarque dar-se-á mediante manifestação da área técnica competente, da ANVISA em sua sede, em Brasília, DF. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
35. Caberá a empresa interessada encaminhar à autoridade competente, na forma dos itens 25 e 25.1 desta Seção, requerimento de autorização de embarque no exterior, mediante preenchimento de Petição de Autorização de Embarque no Exterior. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
35.1. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária quando da autorização de embarque no exterior: (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Declaração do detentor do registro autorizando a importação por terceiro; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Instrumento de representação da pessoa jurídica detentora da regularização do produto junto a ANVISA a favor do responsável legal ou representante legal; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) informações sobre o produto e pessoa jurídica importadora, como regularização do produto e da empresa e número de Licenciamento de Importação ou Licenciamento Simplificado de Importação. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
35.2. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
35.3. Estará isento da apresentação do documento da alínea "c", o mandatário devidamente cadastrado junto à respectiva CVSPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
35.4. Estará dispensada da apresentação de informação de regularização da empresa a importação de matérias-primas da classe de produtos desta Seção.
36. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o produto:
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber;
c) Fatura Comercial - "Invoice";
d) Conhecimento de Carga Embarcada;
e) Declaração quanto aos lotes ou partidas, identificados alfa-numericamente, no que couber;
f) Informações, por lote ou partida, emitido pelo fabricante de cada produto;
g) Comprovante de esterilidade do produto ou Laudo de Controle de Qualidade do lote, emitido pelo fabricante, quando couber;
h) Instrumento de procuração da pessoa jurídica detentora da regularização do produto junto a ANVISA ao representante legal, responsável pelo desembaraço;
i) Documento de averbação referente à comprovação da atracação do produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenada. (Exigência suspensa pela Resolução - RDC nº 48, de 31 de agosto de 2012)
36. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II desta Resolução; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) Fatura Comercial - “Invoice”; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Conhecimento de Carga Embarcada; (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Comprovante de esterilidade do produto, para produtos estéreis; e (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
e) Declaração do detentor da regularização autorizando a importação por terceiro. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
36.1. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
36.2. Os documentos de que tratam a alíneas "e", "f" e "g" deverão ser atestados pelo responsável técnico. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
36.3. Estará isento da apresentação do documento da alínea "h", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
37. O enquadramento do produto de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO IX
PROCEDIMENTO 5 - OUTROS PRODUTOS
Subseção I
Procedimento 5.1. – Alimentos
38. A importação de alimentos na forma de matéria-prima, produto semi elaborado, produto a granel ou produto acabado, conforme enquadramento dos produtos no sítio eletrônico da ANVISA, estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
39. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde ocorrerá o desembaraço do produto:
39. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Declaração quanto aos lotes ou partidas, identificados alfanumericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Laudo Analítico de Controle de Qualidade, por lote ou partida, emitido pelo fabricante ou produtor de produtos na forma da regulamentação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
h) Certificado da "Administración Nacional de Medicamentos, Alimentos y Tecnología", para produto oriundo da Argentina, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
i) Declaração do detentor do registro autorizando a importação por terceiro;
j) Licença de Funcionamento, Alvará ou documento correspondente pertinente para a atividade realizada (importar, armazenar, etc) no produto no território nacional, emitido pela autoridade sanitária competente do Estado, Município ou do Distrito Federal;
l) Instrumento de representação da pessoa jurídica detentora da regularização do produto junto a ANVISA a favor do responsável legal ou representante legal; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
m) Documento de averbação referente à comprovação da atracação da o produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra se armazenada. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
39.1. Os documentos de que tratam as alíneas "f" e "g" deverão ser atestados pelo responsável ou representante legal; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
39.2. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
39.3. Estará isento da apresentação do documento da alínea "l", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
40. O enquadramento dos produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
Subseção II
Procedimento 5.2. - Cosméticos, Produtos de Higiene e Perfumes
41. A importação de cosméticos, produtos de higiene e perfumes na forma de matéria-prima, produto semi-elaborado, produto a granel ou produto acabado, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
42. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o produto:
42. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Informações sobre o produto e pessoa jurídica importadora, como regularização do produto e da empresa e número de Licenciamento de Importação ou Licenciamento Simplificado de Importação. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Declaração quanto aos lotes ou partidas, identificada alfanumericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
h) Declaração do detentor do registro autorizando a importação por terceiro;
i) Instrumento de representação da pessoa jurídica detentora da regularização do produto junto a ANVISA a favor do responsável legal ou representante legal; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
j) Documento de averbação referente à comprovação da atracação do produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenado. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
42.1. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
42.2. O documento de que trata a alínea "g" deverá ser atestado pelo responsável técnico. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
42.3. Estará isento da apresentação do documento da alínea "i", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
43. O enquadramento dos produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
Subseção III
Procedimento 5.3. – Medicamentos
44. A importação de medicamentos em geral, não enquadrados nas disposições anteriores, na forma de matéria-prima, produto semi-elaborado, produto a granel ou produto acabado, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
45. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o produto:
45. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Declaração quanto aos lotes ou partidas, identificados alfanumericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Laudo Analítico de Controle de Qualidade, por lote ou partida, emitido pelo fabricante, exceto quando se tratar de importações de padrões de referencia primários;
h) Informações sobre o produto e pessoa jurídica importadora, como regularização do produto e da empresa e número de Licenciamento de Importação ou Licenciamento Simplificado de Importação. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
i) Declaração do detentor do registro autorizando a importação por terceiro;
j) Instrumento de representação da pessoa jurídica detentora da regularização do produto junto a ANVISA a favor do responsável legal ou representante legal; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
l) Documento de averbação referente à comprovação da atracação do produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenada. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
45.1. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
45.2. Os documentos de que tratam as alíneas "f" e "g" deverão ser atestados pelo responsável técnico. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
45.3. Estará isento da apresentação do documento da alínea "j", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
46. O enquadramento dos produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
47. A importação de amostras de medicamentos não regularizados, sem comprovação de segurança e eficácia, destinada à análise para fins de registro, testes de controle da qualidade, estudos de estabilidade, bioequivalência e equivalência farmacêutica ou ainda testes de equipamentos participantes do processo fabril ou laboratorial, cuja composição integra substâncias ativas com comprovação de segurança e eficácia deverá atender as exigências sanitárias previstas neste procedimento, excetuada a referente à apresentação do registro ANVISA.
Subseção IV
Procedimento 5.4. – Saneantes
48. A importação de saneantes na forma de matéria-prima, produto semi elaborado, produto a granel ou produto acabado, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
49. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o produto:
49. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Declaração quanto aos lotes ou partidas, identificada alfanumericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Informações sobre o produto, seu respectivo lote e partida, e pessoa jurídica importadora, como regularização do produto e da empresa e número de Licenciamento de Importação ou Licenciamento Simplificado de Importação; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
h) Declaração do detentor do registro autorizando a importação por terceiro;
i) Instrumento de representação da pessoa jurídica detentora da regularização do produto junto a ANVISA a favor do responsável legal ou representante legal; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
j) Documento de averbação referente à comprovação da atracação do produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenado. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
49.1. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
49.2. O documento de que trata a alínea "f" deverá ser atestado pelo responsável técnico. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
49.3. Estará isento da apresentação do documento da alínea "i", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
49.4. Estará dispensada da apresentação de informação de regularização da empresa a importação de matérias-primas da classe de saneantes desta Seção, não eximindo a apresentação da Licença de Funcionamento, Alvará ou documento correspondente pertinente para a armazenagem do produto no território nacional, emitido pela autoridade sanitária competente do Estado, Município ou do Distrito Federal, na forma da regulamentação local para concessão e renovação.
50. O enquadramento dos produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
Subseção V
Procedimento 5.5. - Produtos para Diagnóstico In Vitro
51. A importação de produtos para diagnóstico, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA, estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
52. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o produto:
52. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Declaração quanto aos lotes ou partidas, identificados alfanumericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Informações sobre o produto, seu respectivo lote e partida; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
h) Comprovante de esterilidade do produto, emitido pelo fabricante, quando couber;
i) Declaração do detentor do registro autorizando a importação por terceiro;
j) Instrumento de representação da pessoa jurídica detentora da regularização do produto junto a ANVISA a favor do responsável legal ou representante legal; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
l) Documento de averbação referente à comprovação da atracação do produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenado. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
52.1. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
52.2. O documento de que trata a alínea "f" deverá ser atestado pelo responsável técnico. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
52.3. Estará isento da apresentação do documento da alínea "j", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
53. O enquadramento dos produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
Subseção VI
Procedimento 5.6. - Produtos Diversos
54. A importação dos produtos, na forma desta Seção, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA, estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
54.1. São produtos enquadrados nesta Seção:
a) cabelos em suas diversas formas de apresentação para uso humano; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
b) perucas, barbas, sobrancelhas, pestanas, madeixas e artefatos semelhantes para uso humano; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) lã, pelos e outras matérias têxteis, preparados para a fabricação de perucas ou de artefatos semelhantes para uso humano; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) mamadeira, bico de mamadeira, chupeta, mordedor;
e) vestuários e acessórios para uso médico, odontológico ou hospitalar, incluindo artefatos confeccionados e moldes para vestuário; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
f) artefatos de matérias têxteis, calçados, chapéus e artefatos de uso semelhante, usados, nos casos de doação. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
55. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o produto
55. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Informações sobre o produto, seu respectivo lote e partida, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Declaração do detentor do registro autorizando a importação por terceiro, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
h) Instrumento de representação da pessoa jurídica detentora da regularização do produto junto a ANVISA a favor do responsável legal ou representante legal; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
i) Documento de averbação referente à comprovação da atracação do produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenado. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
55.1. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
55.2. Estará isento da apresentação do documento da alínea "h", o mandatário devidamente cadastrado junto à respectiva CVPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
56. O enquadramento dos produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO X
PROCEDIMENTO 6 - BENS E PRODUTOS QUE CONTÊM TECIDOS OU FLUIDOS DE ANIMAIS RUMINANTES
57. A importação de matéria-prima, produto semi-elaborado, produto a granel ou produto acabado, de quaisquer classes de produtos, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA estará sujeita ao registro de Licenciamento de Importação no SISCOMEX e autorização prévia favorável de embarque, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
57. A importação de matéria-prima, produto semi-elaborado, produto a granel ou produto acabado, de quaisquer classes de produtos, conforme enquadramento dos produtos disponível no Portal da ANVISA, estará sujeita ao registro de Licenciamento de Importação no SISCOMEX, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro. (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
58. A autorização prévia de embarque dar-se-á mediante manifestação da autoridade sanitária de desembaraço aduaneiro. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
58.1. Nos casos previstos neste Regulamento, a autorização prévia de embarque dar-se-á mediante manifestação do setor técnico da ANVISA em sua sede, em Brasília, DF. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
58.2. Caberá a empresa interessada encaminhar à autoridade competente, na forma dos itens 58 e subitem 58.1 desta Seção, requerimento de autorização de embarque no exterior, mediante preenchimento de Petição de Autorização de Embarque no Exterior. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
59. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o produto:
59. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Informações sobre o produto, sua data de fabricação, seu respectivo lote e partida, emitidas pelo fabricante, pessoa jurídica importadora, regularização do produto e da empresa e número de Licenciamento de Importação ou Licenciamento Simplificado de Importação; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Declaração quanto aos lotes ou partidas, identificados alfa-numericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
h) Comprovante de esterilidade do produto, emitido pelo fabricante, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
i) Declaração do detentor do registro autorizando a importação por terceiro;
j) Instrumento de procuração da pessoa jurídica detentora da regularização do produto junto a ANVISA ao representante legal, responsável pelo desembaraço; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
l) Documento de averbação referente à comprovação da atracação do produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenado. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
59.1. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata esta Seção deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
59.2. Os documentos de que tratam a alíneas "f", "g" e "h" deverão ser atestados pelo responsável técnico. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
59.3. Estará isento da apresentação do documento da alínea "j", o mandatário devidamente cadastrado junto à respectiva CVSPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
60. O enquadramento dos produtos de que trata esta Seção está disponível no sítio eletrônico da ANVISA, e produz seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
SEÇÃO XI
PROCEDIMENTO 7 - BENS E PRODUTOS SOB INTERVENÇÃO DECORRENTE DE CONTEXTO EPIDEMIOLÓGICO INTERNACIONAL, EMERGENCIAIS E TEMPORÁRIAS
62. A importação de produtos na forma de matéria-prima, produto semi elaborado, produto a granel ou produto acabado, assim definidas por ato do Diretor responsável pela ANVISA em situações de contexto epidemiológico internacional emergencial ou temporário, conforme enquadramento dos produtos disponível no sítio eletrônico da ANVISA, estará sujeita ao registro de Licenciamento de Importação no SISCOMEX e autorização prévia favorável de embarque, submetendo-se à fiscalização pela autoridade sanitária antes de seu desembaraço aduaneiro.
63. A autorização prévia de embarque dar-se-á mediante manifestação da autoridade sanitária de desembaraço aduaneiro.
63.1. Nos casos previstos neste Regulamento ou definido por ato do Diretor responsável pela ANVISA, a autorização prévia de embarque dar-se-á mediante manifestação do setor técnico da ANVISA em sua sede, em Brasília, DF.
64. Caberá a empresa interessada encaminhar à autoridade competente, na forma dos itens 63 e 63.1 desta Seção, requerimento de autorização de embarque no exterior, mediante preenchimento de Petição de Autorização de Embarque no Exterior.
65. Constituir-se-á documentação obrigatória para apresentação à autoridade sanitária onde será desembaraçado o produto:
65. O processo de importação deverá ser instruído com os seguintes documentos: (Redação dada pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
a) Petição para Fiscalização e Liberação Sanitária de que trata o subitem 1.2. do Capítulo II;
b) Guia de Recolhimento da União - GRU, da Secretaria do Tesouro Nacional, conforme disposto na legislação sanitária pertinente; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
c) Autorização de acesso para inspeção física, na forma da legislação fazendária, quando couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
d) Fatura Comercial - "Invoice";
e) Conhecimento de Carga Embarcada;
f) Declaração quanto aos lotes ou partidas, identificados alfanumericamente, no que couber; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
g) Informações sobre o produto, sua data de fabricação, seu respectivo lote e partida, emitidas pelo fabricante, pessoa jurídica importadora, regularização do produto e da empresa e número de Licenciamento de Importação ou Licenciamento Simplificado de Importação;
h) Comprovante de esterilidade do produto ou Laudo de Controle de Qualidade do lote, emitido pelo fabricante, quando couber;
i) Declaração do detentor do registro autorizando a importação por terceiro;
j) Instrumento de procuração da pessoa jurídica detentora da regularização do produto junto a ANVISA ao representante legal, responsável pelo desembaraço; (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
l) Documento de averbação referente à comprovação da atracação do produto no ambiente armazenador e sua respectiva localização, expedido pelo representante legal da pessoa jurídica administradora do recinto alfandegado onde o produto encontra-se armazenado. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
65.1. Quando não especificado a obrigatoriedade da apresentação exclusiva em sua forma original, os documentos de que trata este Capítulo deverão ser apresentados na sua forma original e cópia, para sua autenticação, ou previamente autenticados. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
65.2. Os documentos de que tratam a alíneas "f", "g" e "h" deverão ser atestados pelo responsável técnico e/ ou responsável legal. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
65.3. Estará isento da apresentação do documento da alínea "j", o mandatário devidamente cadastrado junto à respectiva CVSPAF de desembaraço. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
66. O enquadramento dos produtos de que trata esta Seção, definidas os produtos por ato do Diretor responsável pela ANVISA, estará disponível no sítio eletrônico da ANVISA, e produzirá seus efeitos legais para sua classificação na importação sob anuência sanitária. (Revogado pela Resolução – RDC nº 208, de 5 de janeiro de 2018)
CAPÍTULO XL
QUADRO I
FINALIDADES DE IMPORTAÇÃO
Feiras e Eventos:
EXPOSIÇÃO EM FEIRAS E EVENTOS.
EXPOSIÇÃO COM DEMONSTRAÇÃO EM FEIRAS E EVENTOS.
EXPOSIÇÃO, DEMONTRAÇÃO E DISTRIBUIÇÃO EM FEIRAS E EVENTOS.
Pesquisa Clínica:
PESQUISA CLÍNICA:
PESQUISA CLÍNICA / ACOMPANHAMENTO E/OU AVALIAÇÃO (Produtos médicos e produtos para diagnóstico in vitro).
PESQUISA CLÍNICA / COLETA (KIT) DE MATERIAL BIOLÓGICO VINCULADO AO ACOMPANHAMENTO E/OU AVALIAÇÃO.
Doação Internacional:
DOAÇÃO INTERNACIONAL EXCLUSIVA DE PEÇAS DE VESTUÁRIO USADOS E DE ARTEFATOS TÊXTEIS E SINTÉTICOS USADOS.
DOAÇÃO INTERNACIONAL DE PRODUTOS SOB VIGILÂNCIA SANITÁRIA - DIVERSAS.
Loja Franca
LOJA FRANCA, COMÉRCIO E ARMAZENAGEM;
Controle da qualidade:
TESTE DE CONTROLE DA QUALIDADE;
Aprovação de Registro de Produto:
APROVAÇÃO DE REGISTRO OU REGULARIZAÇÃO DO PRODUTO PERANTE O SNVS.
Testes de Equipamentos:
TESTE OPERACIONAL EM EQUIPAMENTOS INDUSTRIAL OU LABORATORIAL.
Teste de biodisponibilidade, bioequivalência ou equivalência farmacêutica:
TESTE DE BIODISPONIBILIDADE, BIOEQUIVALÊNCIA OU EQUIVALÊNCIA FARMACÊUTICA.
Pesquisa de Mercado:
PESQUISA DE MERCADO.
Avaliação de rotulagem ou embalagem:
AVALIAÇÃO DE EMBALAGEM OU ROTULAGEM.
Segurança e Eficácia:
TESTE PARA VERIFICAÇÃO DE SEGURANÇA E EFICÁCIA EM COSMÉTICOS, PERFUMES E PRODUTOS DE HIGIENE PESSOAL.
Diagnóstico laboratorial clínico:
DIAGNÓSTICO LABORATORIAL CLÍNICO DE MATERIAL BIOLÓGICO HUMANO.
DIAGNÓSTICO LABORATORIAL CLÍNICO DE MATERIAL BIOLÓGICO HUMANO VINCULADO À PESQUISA CLÍNICA EM DESENVOLVIMENTO NO EXTERIOR.
MATERIAL DE REFERÊNCIA ORIGINÁRIO DE MATERIAL BIOLÓGICO HUMANO DESTINADO Á DIAGNÓSTICO LABORATORIAL CLÍNICO.
DESENVOLVIMENTO OU VALIDAÇÃO DE METODOLOGIA ANALITICA EM LABORATÓRIO DE DIAGNÓSTICO DE CLÍNICO DE MATERIAL BIOLÓGICO HUMANO.
Pessoa física, consumo pessoal:
PESSOA FÍSICA, USO INDIVIDUAL, NÃO CARACTERIZADO COMO COMÉRCIO E REVENDA, OU USO EM TERCEIROS.
Pessoa física, prestação de serviços a terceiros:
PESSOA FÍSICA PARA PRESTAÇÃO DE SERVIÇOS A TERCEIROS. Células e Tecidos humanos:
PELE, TECIDO MÚSCULO-ESQUELÉTICO E VALVAS CARDÍACAS PARA FINS TERAPÊUTICOS;
CÉLULAS PROGENITORAS HEMATOPOÉTICAS PARA FINS TERAPÊUTICOS;
CÉLULAS E TECIDOS GERMINATIVOS E PRÉ-EMBRIÕES HUMANOS PARA FINS TERAPÊUTICOS.
CÓRNEAS HUMANAS PARA FINS TERAPÊUTICOS;
Enfermarias, farmácias ou conjunto médico de bordo:
REPOSIÇÃO OU ABASTECIMENTO INICIAL DE ENFERMARIA, FARMÁCIA OU CONJUNTO MÉDICO DE BORDO DE MEIOS DE TRANSPORTES; BRASILEIROS OU ESTRANGEIROS SOB AFRETAMENTO OU ARRENDAMENTO.
REPOSIÇÃO OU ABASTECIMENTO INICIAL DE ENFERMARIA, FARMÁCIA OU CONJUNTO MÉDICO DE BORDO DE MEIOS DE TRANSPORTES ESTRANGEIROS.
Licenciamento de importação de outra instituição:
DEFERIMENTO EM LICENCIAMENTO DE IMPORTAÇÃO DE PRODUTO COM FINALIDADE DE USO CUJO CONTROLE ESTÁ PREVISTO PARA OUTRA INSTITUIÇÃO ANUENTE.
Retorno de Produto Exportado:
RETORNO DE BEM OU PRODUTO SOB VIGILÂNCIA SANITÁRIA EXPORTADO.
RETORNO AO PAÍS, DE BEM OU PRODUTO SOB VIGILÂNCIA SANITÁRIA EXPORTADO PARA REPAROS, CONSERTOS OU RESTAURAÇÃO NO EXTERIOR.
Retorno para o Exterior de Produto Importado:
RECHAÇO OU RETORNO PARA O EXTERIOR DE BEM OU PRODUTO COM SUSPEITA DE IRREGULARIDADE SANITÁRIA OU COM IRREGULARIDADE CONFIRMADA LABORATORIALMENTE.
Indústria ou comércio:
FISCALIZAÇÃO E LIBERAÇÃO SANITÁRIA DE BEM OU PRODUTO IMPORTADO PARA FINS DE INDÚSTRIA OU COMÉRCIO.
Desinterdição de produtos:
DESINTERDIÇÃO SANIT£RIA DE BENS OU PRODUTOS.
Liberação de Termo de Guarda:
LIBERAÇÃO DE TERMO DE GUARDA E RESPONSABILIADE. Termo de InutilizaÁ„o:
EMISSÃO DE TERMO DE INUTILIZA«ÃO DE PRODUTOS SOB VIGIL¬NCIA SANITÁRIA.
Padrão ou Material de ReferÍncia:
PADRÃO OU MATERIAL DE REFER NCIA PARA CONTROLE QUALITATIVO DE MATÉRIAS-PRIMAS OU PRODUTOS SOB VIGILÃNCIA SANITÁRIA.
Programas de saúde pùblica:
USO EXCLUSIVO EM PROGRAMAS DE SA⁄DE P⁄BLICA - AQUISIÇÃO POR ORGANISMO MULTILATERAL INTERNACIONAL.
USO EXCLUSIVO EM PROGRAMAS DE SAÚDE PÙBLICA - AQUISIÇÃO PELO MINISTÉRIO DA SAÚDE OU SUAS ENTIDADES VINCULADAS.
QUADRO 2
NATUREZA DO BEM OU PRODUTO
PRODUTO ACABADO.
PRODUTO A GRANEL DESPROVIDO DE EMBALAGEM PRIMÁRIA. PRODUTO A GRANEL COM EMBALAGEM PRIMÁRIA.
PRODUTO SEMI-ELABORADO.
MATÉRIA-PRIMA OU INSUMO.
PADRÃO DE REFERENCIA
(*) Republicada por ter saÌdo no DOU nº 216, de 6-11-2008, SeÁ„o 1, P·g. 36, com incorreção no original.


Deixar comentário
Para comentar é preciso fazer login no sistema.