Inativação e Captura de Radicais Livres
publicado em 01/10/1991
P. H. Haller
Pentapharm Ltd., Basiléia, Suiça
 Neste artigo é descrita a ação de um inibidor de radicais livres composto de uma metaloenzima, peptídeos e glicogênio. Seu efeito preventivo contra a ação oxidativa dos raios UV foi determinado em dois experimentos utilizando homogenato de pele de rato. É descrito também outro produto de ação antioxidante em sistemas biológicos, trata-se de um extrato de coração bovino rico em ubiquinona (coenzima Q). A coenzima Q pode prevenir o envelhecimento dos tecidos agindo na respiração celular e na peroxidação de membranas. Sua associação com vitamina E combate a peroxidação lipídica e a formação do aldeído malônico. O teste experimental com lipossomas demonstrou que a ubiquinona penetra na, pele agindo em profundidade, podendo ser utilizada no tratamento capilar e no combate a caspa.
Neste artigo é descrita a ação de um inibidor de radicais livres composto de uma metaloenzima, peptídeos e glicogênio. Seu efeito preventivo contra a ação oxidativa dos raios UV foi determinado em dois experimentos utilizando homogenato de pele de rato. É descrito também outro produto de ação antioxidante em sistemas biológicos, trata-se de um extrato de coração bovino rico em ubiquinona (coenzima Q). A coenzima Q pode prevenir o envelhecimento dos tecidos agindo na respiração celular e na peroxidação de membranas. Sua associação com vitamina E combate a peroxidação lipídica e a formação do aldeído malônico. O teste experimental com lipossomas demonstrou que a ubiquinona penetra na, pele agindo em profundidade, podendo ser utilizada no tratamento capilar e no combate a caspa.
Radicais Livres
A Concentração de Radicais Livres sobre o Organismo
Glycoliv
Efeito Preventivo
Segundo Componente do Glycoliv
Lipoliv
Associação: Ubiquinona e Vitamina E
O envelhecimento é o resultado das alterações progressivas do nosso corpo que induzem a doenças e, finalmente, à morte das células do homem. Ainda hoje não se conhece exatamente onde se inicia o envelhecimento e quais são os mecanismos por ele responsáveis. Imagina-se que estes possam ser de natureza genética, hormonal, imunológica, provavelmente devido à presença dos radicais livros. Durante o envelhecimento pode-se constatar uma diminuição da velocidade da catálise, inibidora real das trocas enzimáticas. Atualmente existem duas teorias para explicar a causa: a primeira diz que a duração da vida está programada geneticamente, enquanto que a segunda postula que o envelhecimento é resultado da influência dos radicais liberados de forma endógena e exógena. Nós acreditamos que a realidade encontra-se na combinação destas duas teorias.
Radicais Livres
Os radicais livres são átomos de moléculas que apresentam um ou mais elétrons não emparelhados. Devido a isto, estes são extremamente reativos e têm vida muito breve. Os radicais livres, e de modo particular aqueles do oxigênio, são responsáveis por vasta gama de alterações metabólicas no interior do organismo. O oxigênio pode ligar-se, direta ou indiretamente, com a maior parte dos elementos. Graças à sua configuração eletrônica, a reação do oxigênio com os compostos orgânicos é sempre do tipo exotérmica. As explosões e o fogo não representam outra coisa que uma oxidação rápida.
É graças a tal reatividade que o oxigênio representa um papel fisiológico essencial. Quero lembrar que existem formas mais reativas deste elemento, como, por exemplo, o ozônio. Sabemos que o oxigênio é vital para todos os organismos aeróbicos, mas nenhuma forma deste elemento é muito tóxica e este é mesmo o caso dos radicais livres.
Os radicais livres de oxigênio formam-se graças à redução do oxigênio molecular. Devido à influência externa, o oxigênio molecular se liberta. Este acolhe um elétron e se torna radical superóxido O2-. Na segunda fase, dois radicais superóxidos reagem com dois de hidrogênio e formam o peróxido de hidrogênio. Na terceira fase, este último perde um elétron e o transfere ao hidrogênio que forma o radical oxidrila OH separado da água. Na quarta fase, este último é restituído a água após a absorção do quarto elétron.
Com exceção de alguns agentes químicos como os fármacos, são principalmente os fatores físicos, como o calor, o frio, a luz, os raios UV, as ondas supersônicas, os raios ionizantes ou combinações destes elementos, que levam a formação dos radicais livres. Os radicais não possuem todos a mesma reatividade. Os mais ativos (e mais nocivos) são os radicais oxidrila que levam a oxigenação de todo o material biológico local onde este se forma.
Não se conhece ainda uma proteção natural contra estes, todavia, em certas condições fisiológicas os radicais de oxidrila reagem com seus captores, como, por exemplo, açúcar, aminoácidos ou seus nucleosídeos, que reduzem a sua agressividade. Os radicais livres de oxigênio atacam as macromoléculas mais variadas: destroem numerosas membranas celulares e atacam os seus lipídeos com a consequente formação de peróxidos que tornam tais membranas permeáveis e, finalmente, as destroem. Ao mesmo tempo, os radicais livres de oxigênio podem inativar algumas enzimas e ácidos nucléicos. Todos nós conhecemos o processo de formação destes peróxidos quando as gorduras e os óleos se tornam rançosos.
A agressividade dos radicais livres não se limita somente à membrana celular e à matriz intracelular, mas além disto, aos compostos do espaço intercelular onde estes despolarizam o ácido hialurônico, os proteoglicanos e o colágeno. Hoje não conhecidas mais de 50 doenças sobre as quais os radicais livres de oxigênio têm influência. Por exemplo, todas as formas de artrite, de tumores, arteriosclerose, o mal de Alzheimer etc., mesmo as inflamações são devido a excesso de radicais livres de oxigênio.
A Concentração de Radicais Livres sobre o Organismo
É sabido que o nosso organismo combate a formação e os efeitos destes radicais. O organismo desenvolveu diferentes mecanismos de defesa e de controle com o objetivo de combater o efeito negativo dos radicais livres.
Levemos em consideração a SOD. Tratam-se de enzimas presentes em todos os tecidos aeróbicos em condições de metabolizar os radicais de peróxido catalisando a transformação destes radicais. Esta metaloenzima catalisa a transformação dos radicais de superóxido.
Como resultado desta reação de redução e de oxigenação, formam-se peróxido de oxigênio e água.
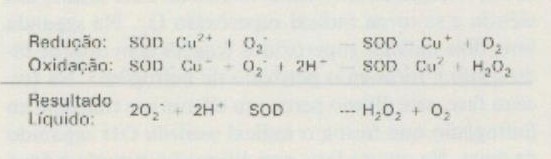
Como se nota, a SOD não age somente sobre os radicais superóxidos, mas também sobre os radicais oxidrila (OH) podendo ser obtida através da reação de Haber-Weiss, diminuindo a concentração de O2-. As SOD são metaloenzimas que contêm Cu, Zn, Mn ou Fe e são as enzimas mais estáveis que se conhece.
Glycoliv
Trata-se de uma fração altamente purificada de fígado bovino com atividade específica antioxidante. O produto se compõe de una metaloenzima, a Cu,Zn SOD, de peptídeos e de um polissacarídeo: o glicogênio. As proporções destes ingredientes são rigorosamente controladas. O conteúdo da metaloenzima é medido em unidades Markland (UIP), que representa a quantidade de enzima necessária para inibir a auto-oxidação do pirogalol em ambiente levemente alcalino. Portanto, 1 UIP inibe em 50% o pirogalol. A atividade do Glycoliv encontra-se entre 4.500 e 5.500 UIP/ml.
Em uma primeira série de experimentos medimos o poder de Glycoliv sobre a inibição da despolimerização do ácido hialurônico, induzida pela hipoxantina/ xantinoxidase. A xantinoxidase é uma flavoproteína que catalisa a oxidação da hipoxantina em xantina e esta última em ácido úrico. Devido a esta reação formam-se os radicais livres de oxigênio.
A xantinoxidase é uma enzima presente em todos os tecidos e parece ser a causa principal da formação dos radicais superóxidos em tecidos pós-isquêmicos. O resultado da reação do contato entre a hipoxantina/xantinoxidase e o acido hialurônico é a diminuição da viscosidade deste último.
A solução levada a teste continha 0,5% de ácido hialurônico, 2,5 M de hipoxantina e 0,1 U/ml de xantinoxidase. O Glycoliv foi adicionado em diversas concentrações como inibidor dos radicais livres.
Resultados: pode-se simular a despolimerização do ácido hialurônico deixado sob a influência dos radicais superóxido, de modo que esta pode ser medida diretamente. Sem Glycoliv a viscosidade do ácido hialurônico diminuiria, de modo drástico, já nos primeiros minutos. Cinco minutos após a adição de xantinoxidase a sua perda seria de 8,7%, após 15 minutos de 21,9%, após 3 horas de 46,9%. Dois dias após, a taxa poderia ser ainda de 12% do seu valor inicial. A adição de Glycoliv em concentrações de 1 a 100 UIP (0,02-2%) provocou, contrariamente, considerável inibição da perda de viscosidade.
Efeito Preventivo
Nos dois experimentos que seguiram, utilizamos homogenatos de pele de rato. Determinou-se através da adição de Glycoliv a inibição da oxidação provocada pelos raios UV. Uma característica das alterações da pele devido à oxidação é a formação de complexos lipídicos pigmentados fluorescentes, como, por exemplo, a lipofucsina, reconhecível em tecidos envelhecidos. Estes lipopigmentos são o resultado dos processos de degradação dos lipídeos. Este tipo de pigmento é reproduzido através da ação do aldeído malônico sobre a feniltilamina. Este aldeído nasce do processo e peroxidação dos ácidos graxos e é muito reativo. A formação de aldeído malônico é normalmente utilizada na química de alimentos para o controle dos óleos e gorduras rançosas. Há alguns anos os bioquímicos utilizaram-no para medir os efeitos e a inibição da peroxidação lipídica. Determinamos o poder do Glycoliv de inibir a oxidação induzida pela luz UV através da análise espectral do aldeído malônico gerado.
Quando um homogenato dos tecidos vem aquecido com o ácido tiobarbitúrico, forma-se uma reação colorida com variação que vai do rosa ao vermelho. A análise espectral mostrou que esta coloração é devida ao aldeído malônico proveniente dos ácidos graxos.
Os homogenatos de pele de rato mencionados acima foram filtrados, e em seguida adicionou-se água ou Glycoliv.
Estes homogenatos foram irradiados sucessivamente com uma lâmpada de raios UVA (sistema Wolff, tipo 9BWW6 de 20 watt).
Duas partes dos homogenatos foram tratadas com ácido tricloroacético: adicionou-se 0,5% de ácido tiobarbitúrico. Após a incubação de 1 hora em água em ebulição foram separados os precipitados e mediu-se o desaparecimento da substância sobrenadante sob o comprimento de onda de 531 nm.
Resultados: a forte irradiação provocou a oxidação muito rápida que alcançou o seu ponto culminante após 30 minutos. Quinze minutos após a irradiação, as modificações provocadas pelo Glycoliv à concentração de 2.500 UIP/ml inibiram em 36.5%; após 30 minutos, em 24,0% e, após 3 horas, ainda em 13% a atividade oxidativa.
Em outra série de experimentos, mediu-se a inibição da oxidação de Fe3 Fe2 em um homogenato de pele de rato. Esta oxidação, devido a uma transferência de elétrons, seguramente provoca a formação do RLO (radicais livres de oxigênio). O método utilizado foi análogo aos experimentos precedentes. Foram utilizados homogenatos de pele de rato, ao invés de provocar a oxidação através dos raios UV, adicionou-se a este homogenato 0,2 M de Fe3 m EDTA. A medida para a determinação do aldeído malônico forneceu os seguintes resultados: durante os primeiros 15 minutos a inibição com Glycoliv foi fraca, mas aos términos deste período esta alcançou o seu máximo, enquanto que a oxidação da solução aumentava. A inibição provocada por 2.500 UIP de Glycoliv após 15 minutos foi de 12,5%, após 1 hora foi de 48.8% e após 3 horas de 56.1%.
As medidas com as diversas concentrações de Glycoliv foram comprovatórias uma vez que os mesmos 25 UIP/ml (-0,5%) inibiram ainda 29.8% da oxidação.
Estas experiências confirmaram que o preparado é um principio potente contra os efeitos tóxicos do oxigênio.
Segundo Componente do Glycoliv
O segundo elemento componente do preparado de Glycoliv é uma fração de fígado contendo peptídeos e um polissacarídeo: o glicogênio.
O glicogênio é um polissacarídeo ramificado com peso molecular elevado, cuja síntese tem lugar principalmente no fígado e nas células musculares. É a partir da glicose que o glicogênio se forma no organismo animal. O seu papel é de formar a reserva de energia que, quando requisitada, torna-se imediatamente disponível. É diferente do acúmulo de gorduras, já que estas liberam muito lentamente a energia acumulada. A glicose em si não pode ser avaliada como em grande quantidade e, por esse motivo, se transforma por via enzimática em glicogênio. Logo que o organismo necessita de açúcar, glicogênio surge reconstituído na unidade da glicose. Esta glicose verifica-se, principalmente, através do intermediário do ciclo do ácido cítrico. Durante sua degradação em CO2 e água, é liberada muita bioenergia. Foi descoberto que o glicogênio aplicado em cosmético é um agente hidratante muito eficaz.
Conhecemos os danos causados pelo envelhecimento da pele que podem surgir mesmo prematuramente, devido a doença ou influência externa. Sabe-se que é necessária muita energia disponível biologicamente, devido a multiplicidade de reações químicas que ocorrem em cada célula.
Foi verificado também que o glicogênio reduz significativamente a rugosidade da pele.
Mediu-se a hidratação e a hipoproteção de uma emulsão contendo 5% de Glycoliv. Este preparado foi aplicado durante 14 dias sobre o antebraço de voluntários. No 15o dia mediu-se o grau de hidratação, com o uso de um instrumento, 15, 30, 60 e 180 minutos após a última aplicação. Os resultados mostram que graças ao Glycoliv o teor de água aumentou consideravelmente.
Durante outra série de experimentos, preparou-se marcas cutâneas com uma massa de silicone que foi aplicada sobre o antebraço e retirada após três minutos para poder analisar a estrutura dos relevos da pele. Os antebraços dos voluntários foram tratados ora com placebo, ora com emulsão contendo o princípio ativo e, ambos os casos, expostos por 5 minutos aos raios UV.
Foi observada a formação de eritemas e medida a rugosidade através das marcas da pele. A parte tratada com a emulsão não contendo Glycoliv apresentava maior rugosidade e eritema, enquanto que a zona tratada com a solução contendo Glycoliv não mostrava qualquer sinal de inflamação, a pele se apresentava lisa e não desidratada.
Concluindo, podemos afirmar que o Glycoliv é um preparado interessante para a adição a produtos cosméticos preventivos e de antienvelhecimento da pele, produtos solares e após o sol. Adicionado a uma emulsão detergente ou a um tônico, pode contribuir para atenuar o processo fisiológico normal de envelhecimento da pele, deixando-a mais lisa e protegendo-a dos raios UV e dos outros agentes agressivos.
É recomendada a adição deste principio ativo a produtos para cura da pele irritada (bebê, acne etc), pois como foi comentado, os processos inflamatórios avançam devido à presença dos radicais livres.
Lipoliv
O segundo preparado que obtivemos, é um extrato de coração bovino, rico em ubiquinona (coenzima Q), misturado com acetato de alfa-tocoferol e dissolvido em esqualeno de origem vegetal. As ubiquinonas constituem um grupo de benzoquinonas lipossolúveis. A sua estrutura é análoga àquela da vitamina K2. Trata-se de 2,3-dimetaxi-5-etil-6-poliprenil-1-4-bentoquinona.
A cadeia poliprênica é variável compreendendo de 1 a 12 unidades transisoprenóides. Este composto é descrito como coenzima Q10. Na natureza encontram-se as coenzimas de 6 a 10. No homem o fígado e o coração Não particularmente ricos em coenzimas Q10, mas também está presente no coração de boi e de porco.
A coenzima é o transportador dos elétrons na cadeia respiratória: recebe os elétrons da NADH-hidrogenase e os transporta para o citocromo b.
A ação antioxidante de Lipoliv nos sistemas biológicos é conhecida. Captura os radicais de oxigênio e impede até mesmo a peroxidação das cadeias alifáticas dos ácidos graxos insaturadas. O efeito “polidor” é semelhante aquele da vitamina E, pois esta quinona neutraliza, por um lado, o íon de superóxido e, por outro, interrompe a reação em cadeia da formação dos lipoperóxidos. A coenzima Q10 pode prevenir o envelhecimento dos tecidos, uma vez que age tanto sobre a respiração como sobre a peroxidação da membrana celular. O seu papel bioenergético e a sua ação protetora contra os efeitos negativos dos radicais livres apresentam certamente um grande interesse para a cosmetologia. Consequentemente, a coenzima Q10 é um aditivo útil na preparação dos produtos para a cura do envelhecimento da pele. O acetato de alfa-tocoferol é um agente muito bem conhecido dos cosmetólogos. A sua ação antioxidante é considerável. Por um lado, a molécula da vitamina E age como captura dos radicais livres, de outro, como nós já havíamos mencionado, inibe a ação em cadeia dos transportes dos elétrons e reduz até mesmo os radicais finais a quantidades inofensivas.
Associação: Ubiquinona e Vitamina E
Sabe-se que a carência de vitamina E nos coelhos leva a perda de coenzima Q, o que provoca grave distrofia, e isto pode ser tratado através da aplicação desta coenzima. Numerosas outras publicações mostram a relação entre estes dois compostos. Os casos de deficiência podem ser combatidos por destes elementos. Estudamos a eficácia do Lipoliv sobre a inibição da peroxidação lipídica,
Como já havíamos mencionado, uma das consequências da peroxidação lipídica e a formação do aldeído malônico. Em nossos experimentos foram utilizados os lipossomas provenientes de fração lipídica isolada de cérebro bovino como modelo de membranas lipídicas.
Escolhemos como modelo estes lipossomas, pois estes contêm grande quantidade e lipídeos similares àqueles presentes nas células da pele, particularmente aquelas nos espaços intercelulares do extrato córneo. A p-fenilenodiamina, na presença o ácido tiobarbitúrico, influencia a formação dos produtos oxigenados na peroxidação lipídica. Os aldeídos resultantes formam com o ácido tiobarbitúrico uma coloração rosa como já havíamos visto nos testes com Glycoliv.
Lipossomas preenchidos com 2 mg/ml de Lipoliv foram preparados por dispersão por ultrassom. Para os preparados de referência, substituiu-se o principio ativo pela mesma quantidade de água. O conteúdo em lipídeos foi sempre de 10 mg/ml e 0,2 ml da solução de fenilenodiamina foi adicionado a 5 ml de dispersão de lipossomas já carregados com Lipoliv e com água. As amostras foram incubadas durante 15 horas à temperatura ambiente e em seguida tratadas com ácido tricloroacético. Após terem sido filtradas, as amostras receberam o ácido tiobarbitúrico. A leitura da taxa de formação do aldeído malônico foi efetuada após 10 minutos de incubação em água em ebulição, com espectrômetro entre 500 e 550 nm.
Enquanto as amostras sem Lipoliv apresentaram a coloração rosa, aquelas contendo o princípio ativo não formaram quase aldeídos. Isto significa que no Lipoliv não surgiram produtos de decomposição devido à peroxidação lipídica.
Foi provado que a ubiquinona penetra na pele de rato tratada com este produto e, em seguida, o preparado age em profundidade. A ubiquinona é utilizada até mesmo no tratamento capilar e, em particular, no combate à caspa. Uma das causas da formação da caspa é a oxidação dos ácidos do couro cabeludo. A ação lipídica de certas lipases por parte dos microrganismos sobre o couro cabeludo podem dar lugar a formação de lipoperóxidos misturadas ao processo de queratose. Vimos que a coenzima Q10, graças ao seu poder antioxidante, é eficaz na luta contra a caspa.
Uma vez que a ubiquinona age em profundidade, acredita-se que seja ativa mesmo contra os comedões, já que estes são devido a uma hiperqueratose dos folículos da pele devido a aumento da secreção de gordura.
Podemos dizer que o Lipoliv pode ser utilizado em todos os preparados cosméticos destinados a proteção da pele contra os radicais livres, isto é, não só nos produtos antissolares e antienvelhecimento, mas também nos de tratamento da caspa.
Adaptado de artigo publicado em italiano na revista Prodotto Chimico, novembro de 1990,
Este artigo foi publicado na revista Cosmetics & Toiletries (Edição em Português), 3(5): 53-56, 1991.


Deixar comentário
Para comentar é preciso fazer login no sistema.