Uso de Hera na Cosmetologia
publicado em 01/10/1997
Carlos E. Lisboa e Rosana Gonçalves Rodrigues
Escola de Farmácia da Universidade Federal de Ouro Preto, Ouro Preto MG, Brasil
 Esta atualização técnica reúne dados sobre a eficácia/eficiência do extrato de hora (Hedera helix L.) e suas ações farmacológicas no combate à celulite.
Esta atualização técnica reúne dados sobre a eficácia/eficiência do extrato de hora (Hedera helix L.) e suas ações farmacológicas no combate à celulite.
Aspectos Botânicos
Constituintes Químicos
Ações Farmacológicas
Conclusão
A hera é uma planta histórica, cultivada desde os tempos antigos, ligada e presente em representações de crenças religiosas das civilizações primitivas. Na Grécia1,a simbolizava o amor, a amizade, a sobriedade e a glória imorredoura, na Índia coroava o Monte Meru2,b Sagrado; no Egito era consagrada a Osíris.3,c A mitologia nos apresenta a figura de muitos deuses com uma coroa de hera, entre os quais Baco,4,d deus do vinho. Por isso, na antiguidade, a hera era conhecida pelo nome de "planta de Baco", o que aumenta a crença de que em certos países da Europa, até o século passado, acreditava-se que a coroa de hera era capaz de cessar a dor de cabeça produzida pelos excessos alcoólicos.
Na época atual, a hera é tida como símbolo de ternura e de fidelidade. O povo considera sinal de felicidade quando a planta se desenvolve bem, sendo muito usada em jardinagem, devido a sua aderência a rochas, muros, paredes e árvores.
Aspectos Botânicos
A hera europeia cientificamente possui as seguintes denominações e características botânicas:
• Família: Araliaceae
- Espécie: Hedera helix L.
- Sinonímia: Hedera arborea Gars; H. communis Gray; H. lobata Gilib; H. poetarum; H. poetica Salis.
- Sinonímia vulgar estrangeira: Aradeira, Heradeira, Hereira, Hélera e Hedra, em Portugal; Edera e Ellera, dos italianos; English ivy e ivy, nos Estados Unidos; Epheu, na Alemanha; Hiedra e yedra, nos países de língua espanhola; Ivy, na Inglaterra; Lierre. L. d'Europeu, L. en Arre, L. Grimpant, na Franca; Yedra Trepadora, Espanha; Tch Ang Tch'Ocn T'Eng, na China.
- Sinonímia vulgar: Hera europeia, Hera trepadora. Hera de folha larga, Hera verdadeira.
- Origem: originária da Europa, norte da África, Ásia e Ilhas Canarias.
- Variedades: segundo Pio Correa,5 conta com numerosas variedades naturais, em sua maioria, oriundas das culturas em jardinação e três outras de origem climática ou geográfica: chrysocarpa Tenore, da Turquia, Grécia e Ásia Menor; hibernica Kirchn da Irlanda e taurica Rehd, da Criméia; podendo citar mais de cinquenta variedades hortícolas, destacando-se as conhecidas pelo nome de acuta, algeriensis, angularis, arborea, aurantica (de frutos alaranjados), azorica, bacciferu, cambwodiana, canariensis, caucasica, chrysophyla, conglomerata. contracta, cordata, cordifolia, dentata, digitata aurea, elegantissima, glimii, madeirense, marmorata, pennsylvanica, purpurea, rhoegreriana, submarginatas, viridis e willsiana.
• Família: Convolvulaceae
- Espécie: Evolvulus sericeus SW
- Sinonímia: C. erectus Browne, C. minimus Vitm, Evolvulus angustissimus H.B.K, E. commersonii Roem et Schelet, E. cuspidants H.B.K.
- Origem: Diversos países da América do Sul, inclusive o Brasil.
- Variedades: latior, de folhas mais largas, presente no sul do Brasil.
- Descrição macroscópica: Hedera helix L., trepadeira com raízes adventícias e fixadoras, folhas alternas, glabras, longopecioladas, palmadas, levemente trilobadas, base codiforme, verde escura, às vezes, com manchas brancacentas, limbo até 10 cm de comprimento. Há, ainda, presença de folhas brevipecioladas, inteiras, ovais, ou oblongas, muito coriáceas e mais grossas, nascendo nos ramos mais velhos.
Nos ramos floríferos, as flores apresentam-se lanceo-ovaladas ou rombeas, sem lóbulos, mais ou menos acuminado e base obtusa, flores verdes-amareladas em umbelas terminais ou umbelas longo-penduculadas tomentosas. Os frutos são pretos ou, às vezes, amarelos.5-8
Caule filiforme, com presença de raízes adventícias, podendo alcançar a altura de 30 m, sendo que as hastes superiores tornam-se firmes, rígidas, muito espalhadas e sem raízes adventícias.
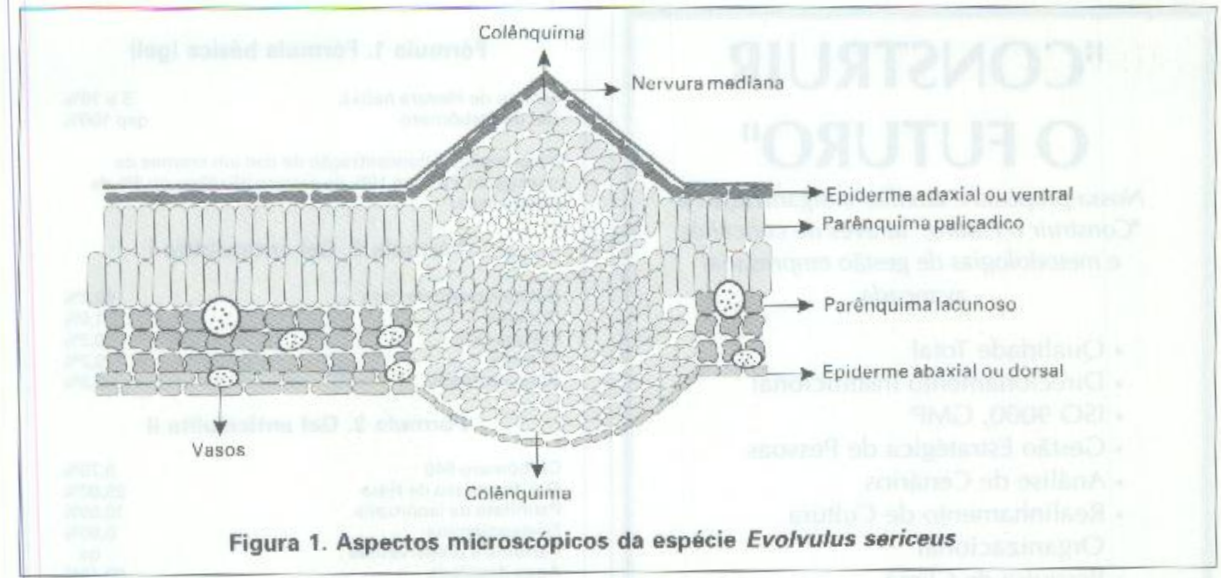
- Descrição microscópica: epiderme adaxial ou ventral constituída por uma camada de células de paredes retas, ondeadas, pouco desenvolvidas, Mesófilo heterogêneo assimétrico com duas camadas de células em paliçada.
Parênquima lacunoso ou esponjoso provido de vasos. A nervura mediana côncava sendo na epiderme adaxial mais aguda com um colênquima desenvolvido um ambas as faces. Conjunto xilema e floema em semicírculo protegido por um periciclo descontinuo.
A epiderme abaxial ou dorsal constituída de células de paredes retas e pouco desenvolvidas (Figura 1).
Constituintes Químicos
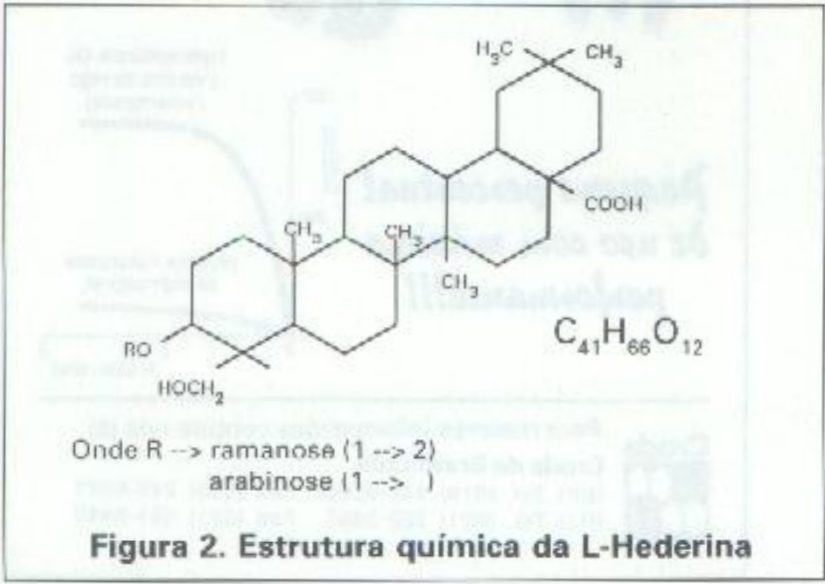
O principal constituinte da Hedera helix L. é um glucosídeo específico, a hederina (helixina).9-11 Pode-se encontrar, também, em toda a planta substâncias tânicas, resinosas e pécticas. As folhas, além da hederina, taninos e saponinas, possuem ainda ácidos orgânicos, iodo e hamamelitol. Os frutos possuem goma, ácido hedero-tânico, ácido hedérico, substância resinosa de sabor adocicado que depois torna-se acre e substância colorante vermelha.7 Nas sementes encontram-se óleo fixo e substância tânica.5,7
- Estrutura química (Figura 2): L-Hederina (Helixina)
- Preparo da planta: Para fins medicinais, são colhidas folhas, Folium hederaceae nos meses de março, abril e/ou agosto,7-8 apanhadas à mão. Segundo, Feller U,12 a hera é planta pouco exigente, que cresce em baixas condições naturais. Assim, os nutrientes, nos meses de fevereiro a maio — inverno europeu — se acumulam devido à necessidade de preservação da planta. De maio em diante, o que foi absorvido é transferido para as novas partes da planta, durante a primavera - cresci mento. Já no verão, a presença de nutrientes é mínima, sugerindo que não há aumento de exo e endopeptidases.
Nos meses de inverno, corre o aumento do conteúdo de carboidratos não-estruturais, devido ao acúmulo de gomas (amido) e açúcares solúveis, que diminuem na primavera.13,14
A floração ocorre nos meses de agosto, setembro e outubro.7,8
Após colhidas, observados os nutrientes que se querem preservar e as condições da planta, as folhas devem ser secas em finas camadas ao sol ou em local bem arejado, levadas à estufa em temperatura menor que 40°C, conservando a cor escura e o gosto amargo. Em seguida, devem ser finamente pulverizadas, procedendo à extração dos princípios ativos pelos métodos convencionais.7,8,11,19 O solvente de escolha deve ser uma mistura de água destilada, álcool etílico (15% ou mais), que é mais adequado devido ao fato de facilitar o uso, a incorporação e a posterior preservação da atividade do produto farmacêutico ou cosmético.19 As etapas após a extração são a descoloração, a desodorização e a concentração a vácuo à temperatura inferior a 50°Ce pressão reduzida, até obter cerca de 2-10 mg/ml.15-20
A 3ª edição do CTFA Cosmetic Ingredient Dictionary20-21 lista mais de cento e cinquenta extratos botânicos. A procura por ingredientes naturais aumenta nas formulações, não sendo apenas uma questão de marketing e sim de eficácia comprovada. A oferta no mercado de extratos tende a crescer, porém, nem sempre se preserva a qualidade do produto. Em busca da qualidade, os fabricantes devem recorrer a análises simples que garantam ao consumidor/produtor/fabricante a eficácia do extrato.22-24 As análises mais aceitas são:
• Cor e odor.
Embora sejam testes muito rudimentares, fornecem informações quanto aos danos sofridos pelas plantas no decorrer do preparo do extrato. Sua valia é grande, no sentido de que os extratos devem apresentar coloração e odor os mais próximos possíveis da planta de origem.
• Resíduo seco.
De fácil execução, relacionado com a concentração ou atividade do extrato, lembrando que, nem sempre, o de maior peso seco é o mais concentrado e de maior ou melhor atividade.
• Índice de refração.
Normalmente, quanto maior o resíduo seco, maior o índice de refração, devendo-se observar, também as diferenças relativas ao índice de retração de vários solventes usados na extração.
• Espectrofotometria UV.
Complementa o resíduo seco, pois permite detectar a presença de conservantes, contaminantes, aditivos, além do principio ativo e de sua concentração aproximada. Cada substância presente nas plantas absorve radiações UV em comprimento de onda determinado por sua estrutura química, o que define o aspecto da curva, permitindo avaliar a presença de componentes estranhos ou se todos os princípios ativos foram extraídos.
• Cromatografia em camada delgada.
É um teste comparativo, qualitativo ou semiqualitativo, avaliado pela presença de manchas, após a eluição com solventes adequados, comparados na placa de sílica a substâncias padrões, indicando a ausência ou a presença do principio ativo.25
Uma só análise não garante a presença do principio ativo, recomendam-se duas a três para ter-se prova de eficácia e melhor aceitação do extrato.
Ações Farmacológicas
A presença de elementos ativos anticelulite em Hedera helix L. foram isolados e comprovados em 1986 por M. Carini. 26
A celulite, como esse processo é conhecido, apresenta se externamente, tanto nos homens como nas mulheres, como uma mudança inestética da silhueta localizando-se principalmente nos membros inferiores, superiores, na região lombo-sacra, abdome, tronco, nuca e face.27-29
Embora não se conheçam as causas desse desequilíbrio bioquímico verifica-se, através de exame microscópico comparativo do tecido celulítico com tecido conjuntivo normal a presença de um menor número de fibras de elastina, maior volume de células adiposas, espessamento das fibras de colágeno, retenção de volume hídrico e consequentemente derme hiperatrofiada.26-30
O tratamento da celulite através de cremes cosméticos é prática comum associada a outros meios terapêuticos, principalmente após sessões de mesoterapia. Deve ser empregado o gel de hera, de modo a facilitar a drenagem linfática manual (DLM) através de massagens com movimentos suaves, circulantes, ascendentes, realizados com apoio das mãos ou de banhos de imersão ou, ainda, por compressas no abdome e regiões afetadas duas vezes ao dia, durante cinco minutos, com o objetivo de levar à dilatação da capilaridade sanguínea e à hiperemia, de forma a prestar uma ajuda aos sistemas de retomo, facilitando a eliminação de liquido intersticial e toxinas acumuladas no tecido. A hera (extrato) age, dessa forma, aumentando a microcirculação e diminuindo o intumescimento do tecido conjuntivo (Fórmulas 1-7).
|
Fórmula 1. Fórmula básica (gel) |
|
|
Extrato de Hedera helix L. |
5 a 10% |
|
Gel de carbômero |
qsp 100% |
|
Observação: A concentração de uso em cremes de |
|
|
|
|
|
Fórmula 2. Gel anticelulite I |
|
|
Gel de extrato de Hera |
90,0% |
|
Perfume |
1,0% |
|
Preservante |
0,2% |
|
Corante |
0,2% |
|
Água destilada |
0,8% |
|
|
|
|
Fórmula 3. Gel anticelulite II |
|
|
Carbômero 940 |
0,75% |
|
Gel de extrato de Hera |
25,00% |
|
Palmitato de isopropila |
10,00% |
|
Trietanolamina |
0,80% |
|
Perfume e preservantes |
qs |
|
Água destilada |
63,45% |
|
|
|
|
Fórmula 4. Gel reafirmante |
|
|
Extrato glicólico de Centella asiática |
1,0 g |
|
Extrato glicólico de Hedera helix |
3,9 g |
|
Propileno glicol |
5,0 g |
|
Carbômero 940 |
2,0 g |
|
Trietanolarina |
qs |
|
Metilparabeno |
0,1 g |
|
Propilparabeno |
0,1 g |
|
Água destilada |
qsp 100,0 g |
|
|
|
|
Fórmula 5. Creme anticelulite |
|
|
Lanolato de isopropila |
2,0% |
|
Palmitato de isopropila |
3,5% |
|
Óleo mineral 90 |
7,0% |
|
Ácido esteárico 30 |
2,5% |
|
Propilenoglicol |
5,0% |
|
Gel de extrato de Hera |
25,0% |
|
Monostarato de propilenoglicol |
3,0% |
|
Perfume e preservantes |
qs |
|
Água destilada |
52,0% |
|
|
|
|
Fórmula 6. Gel após mesoterapia |
|
|
A. Água desmineralizada |
qsp 100,00% |
|
Imidazolidinil ureia |
0,50% |
|
Carbômero 940 |
18,00% |
|
Extrato glicólico de castanha-da-Índia |
10,00% |
|
Extrato glicólico de Hera |
10,00% |
|
Extrato glicólico de Hamamelis |
10,00% |
|
B. Água desmineralizada |
5,00% |
|
Trietanolamina |
0,20% |
|
C. Metacrilato de poliglicerila + propileno glicol |
30,00% |
|
|
|
|
Fórmula 7. Gel rígido (L'Oreal) |
|
|
Carbômero 940 |
0,60% |
|
Goma de alcarroba |
0,02% |
|
Benzoato de metila |
0,02% |
|
Extrato de algas |
10,00% |
|
Extrato de Hera |
10.00% |
|
Imidazolidinil ureia |
0,20% |
|
Trietanolamina |
0,60% |
|
Água destilada |
qsp 100,00% |
Conclusão
Esta atualização técnica reúne dados sobre a eficácia/eficiência do extrato de hora (Hedera helix L.) e suas ações farmacológicas no combate à celulite.
Pretende, ainda, sugerir dados para facilitar a identificação da planta, a confecção, a preservação, a identificação do extrato glicólico e relata algumas formulações de uso em Farmácia e em Cosmetologia.
a A deusa Hera, esposa canônica de Zeus, traduz-se na guardiã dos amores legítimos, na fidelidade, na fecundidade e como protetora do casamento.
b Montanha polar, semelhante ao Montesalvat (Mons Salvationis), pico localizado nas longínquas bordas das quais nenhum mortal pode aproximar-se. É o eixo do mundo, simboliza pureza, a brancura.
c Deus egípcio, soberano e juiz dos mortos, deus supremo do culto funerário, rei da eternidade, soberano da perpetuidade, instrutor das artes e da agricultura.
d Baco ou Dionísio era o deus das árvores, em geral, da vegetação, deus do êxtase e do entusiasmo, que morre, renasce, frutifica, torna a morrer e retorna ciclicamente. Às vezes, metamorfoseado em touro ou bode, representa o espírito da vegetação, do grão que no momento da colheita se encarna num animal, cujo corpo encontra guarita. Durante as festas dionísicas, os participantes cobriam o rosto com máscaras e coroavam-se com a hera, cantando, dançando e bebendo vinho.
Carlos E. Lisboa é farmacêutico e professor de Farmacognosia da Escola de Farmácia da Universidade Federal de Ouro Preto, Ouro Preto MG.
Rosana Goncalves Rodrigues é farmacêutica da Escola de Farmácia da Universidade Federal de Ouro Preto, Ouro Preto MG.
Este artigo foi publicado na revista Cosmetics & Toiletries (Edição em Português) 9(5): 42-46, 1997.
1. Brandão JS. Mitologia Grega, vol 1, ed Vozes, Petrópolis, 1995.
2. Cirlot JE. Dicionário dos Símbolos, p.614, ed Moraes, São Paulo, 1984.
3. Shorter AW et alii. The Egyptian Gods. A Handbook, p.111, ed Cultrix, São Paulo, 1993.
4. Brandão JS. Mitologia Grega, v.2, ed. Vozes, Petrópolis, 1995.
5. Correa Pio M. Dicionário das Plantas Uteis do Brasil e das Exóticas Cultivadas. Ministério da Agricultura, v.2, Rio de Janeiro, 1978.
6. Font Quer Pio. Diccionario de Botánica. Editorial Labor, Barcelona, 1979.
7. Volak J et alii. Plantas Medicinais. Ed. Inquérito, p. 319, Lisboa, 1990.
8. Prihoda A. The Healing Powers of Nature. Hamlyn Publishing Group, p.191, London, 1989
9. Costa AF. Farmacognosia. Fundação Calouste Gulbekian, 1031p, Lisboa, 1986.
10. The Merck Index. An Encyclopedia of Chemicals, Drugs and Biologicals Rahway, Merck, 1989.
11. Teske Magrid et alii. Compendio de Fitoterapia. Herbarium Laboratório Botânico, p.317, Curitiba, 1995.
72. Feller U et alii. Seasonal Changes In The Pattern Of Assimilatory Enzimes And Of Proteolytic Activities In Leaves Or Juvenile lvy. Annals of Botanic 74(4):389-396, 1994.
13. Moora BD et alii. Hamamelitol Purification, Identification by Electrospraylanization Mass Spectrometry and Quantitation, In: Plants Leaves. Planta 195(3):418-425, 1995.
14. Korneeva TV at alii. Specific Protein Patterns of the Maristems and Leaves. In: Juvenile and Adult Hedera Helix Plants. Russian Journal of Plant Physiology 41(6):728-733, 1994.
15. Farmacopeia dos Estados Unidos do Brasil. 2a. Ed, p. 1265. Indústria Gráfica Siqueira, São Paulo, 1959.
16. Pharmacopée Française Redigée Par Ordre du Gouvemement. 7eme , Ed. Ministere de la Santé, Paris, 1949.
17. Där A. Tecnologia Farmacêutica. Zaragoza: Editorial Acribia, p.366, Barcelona, 1981.
18. Sampaio AC. Ingredientes Naturais para Cosméticos. Cosmetics & Toiletries (Edição em Português) 5(1): 28-33, 1993.
19. Hao Z.et alii. Eleito de Extratos Vegetais Chineses no Emagrecimento. Cosmetics & Toiletries (Edição em Português) 5(4):46-48, 1993.
20. Steinberg DC et Alii. Botanical Extracts and Preservation Issues. Cosmetics & Toiletries 106:73-74. 1991.
21. CIFA Cosmetic lgredient Dictionary. 3th.ed, The Cosmetic,Toiletry and Fragrances Association, Washington DC, 1991.
22. Richman A et alii. Analisando o mercado de ervas nos EUA. Revista Racine 6(30): 40-47, 1996.
23. Ollveira LC et alii. Extratos e Óleos Naturais Vagetais Funcionais. Cosmetics & Toiletries (Edição em Português) 7(2): 30-37, 1995.
24, Lab Report. Análise de Extratos Vegetais, Cosmetics & Toiletries (Edição em Português), 5(2): 12-14, 1993.
25. Wagner H. Plant Drug Analysis. A Thick Layer Chromatography. p.320. Ed. Atlas. Springer Verlag, New York, 1984.
26. Carini M. Anars do XIV Congresso da IFSCC, p.1573-7582. Barcelona 1986.
27. Prista LN et alii. Dermofarmácia e Cosmética, p.298. Ed. da Associação Nacional das Farmácias, Porto, 1992.
28. Viglioglia PA et alli. Cosmiatria II, p. 406. Americana de Publicaciones, Buenos Aires 1989.
29. Harmite R. Celulite. Cosmetic & Toiletries (Edição em Português) 1(11):61-68, 1987.
30. Garcia 10. Fundamentação Farmacológica em Mesoterapia. Mesoterapia Atual 1(3) :3-5, 1995.
31. Smith W et alil. NaturalCosmetic Ingredients: Enhanced Function, Cosmetic & Toiletries 106:65-71, 1991.
32. Gouvea CM. Seadweeds in Cosmetics. Cosmetics & Toiletries 95: 47-50. 1980.
33. Fox Charles. Novas Matérias Primas. Revisão de Literatura (1991-1992). Cosmetics & Toiletries 1(106): 65-67,71. 1991
34. Formulário BMS. Cosmetics & Toiletries 4[107):55, 1992.
35. Maury EA. O Livro dos Chás. Receitas de Medicina Natural, p.208, Martins Fontes, São Paulo, 1982.


Deixar comentário
Para comentar é preciso fazer login no sistema.